BзїЖиГЮеЬ®иЃЄе§ЪеЕНзЦЂдїЛеѓЉзЦЊзЧЕпЉИIMDsпЉЙзЪДеПСзЧЕжЬЇеИґдЄ≠еПСжМ•йЗНи¶БдљЬзФ®пЉМиАМBзїЖиГЮи°®йЭҐеПЧдљУпЉИBCRпЉЙиХіеРЂзЭА B зїЖиГЮеЕЛйЪЖжЉФеМЦгАБжКЧеОЯиѓЖеИЂеБПе•љз≠ЙеЕ≥йФЃдњ°жБѓпЉМжШѓиІ£иѓїеЕНзЦЂзЧЕжЬЇзРЖзЪДеЕ≥йФЃеѓЖз†БгАВ
еЙСж°•е§Іе≠¶з†Фз©ґеЫҐйШЯеПСи°®дЇОгАКNatureгАЛзЪДдЄАзѓЗжЦЗзЂ†йАЪињЗжЈ±еЇ¶BCRжµЛеЇПжКАжЬѓеѓєз≥їзїЯжАІзЇҐжЦСзЛЉзЦЃпЉИSLEпЉЙгАБANCAзЫЄеЕ≥и°АзЃ°зВОпЉИAAVпЉЙгАБеЕЛзљЧжБ©зЧЕпЉИCDпЉЙгАБзЩље°Юж∞ПзЧЕпЉИBDпЉЙгАБеЧЬйЕЄжАІиВЙиКљиВњжАІе§Ъи°АзЃ°зВОпЉИEGPAпЉЙеТМIgAи°АзЃ°зВОпЉИIgAVпЉЙињЩ6зІНIMDзЪДBCRеЇУе±ХеЉАеЕ®йЭҐеИЖжЮРпЉМжП≠з§ЇдЇЖзЦЊзЧЕеПСзЧЕжЬЇеИґеТМж≤їзЦЧеУНеЇФзЪДеЕ®жЦ∞иІЖиІТпЉМдЄЇеЕНзЦЂзЧЕз†Фз©ґеЄ¶жЭ•йЗНе§Із™Бз†ігАВ


иѓ•з†Фз©ґзЇ≥еЕ•6зІНIMDжВ£иАЕеЕ±209дЊЛеТМ19дЊЛеБ•еЇЈдЇЇдљЬдЄЇеѓєзЕІзїДгАВйЗЗзФ®
RNA+5race+UMIеїЇеЇУжЦєж≥ХињЫи°МBCR IGHжµЛеЇПпЉМдїОдЇЪеЮЛдљњзФ®гАБIGHVеЯЇеЫ†дљњзФ®гАБеЕЛйЪЖжЙ©еҐЮеТМе§Ъж†ЈжАІзЙєеЊБгАБеРМеЮЛиљђжНҐгАБж≤їзЦЧељ±еУНз≠Йе§ЪдЄ™иІТеЇ¶еЕ®йЭҐеЙЦжЮРIMDжВ£иАЕBCRеЇУзЙєеЊБгАВ
дЇЪеЮЛдљњзФ®еЈЃеЉВпЉЪ
дЄОеБ•еЇЈеѓєзЕІзЫЄжѓФпЉМIgAеЬ®зЦЊзЧЕзїДдЄ≠жЫійЂШпЉМе∞§еЕґжШѓеЬ®SLEеТМCDдЄ≠пЉЫIgEеЬ®EGPAдЄ≠жШОжШЊеНЗйЂШпЉЫAAVдЄ≠зЪДдЇЪеЮЛеИЖеЄГдЄОеБ•еЇЈеѓєзЕІзїДзЫЄдЉЉпЉИеЫЊ1пЉЙгАВиѓіжШОдЄНеРМIMDеЬ®дЇЪеЮЛеИЖеЄГдЄКе≠ШеЬ®жШЊиСЧеЈЃеЉВгАВ
еЬ®еГПCDињЩж†ЈзЪДиВ†йБУзЦЊзЧЕдЄ≠пЉМIgAеНЗйЂШжШѓйҐДжЬЯдЄ≠зЪДпЉМдљЖSLEйАЪеЄЄжґЙеПКIgGдЄОиЗізЧЕжЬЇеИґжЬЙеЕ≥пЉМеЕґIgAжѓФдЊЛзЪДеНЗйЂШжЙУз†ідЇЖвАЬIgGдЄїеѓЉSLEеПСзЧЕвАЭзЪДдЉ†зїЯиЃ§зЯ•пЉМжПРз§ЇйїПиЖЬзЫЄеЕ≥еЕНзЦЂжЬЇеИґеПѓиГљеЬ®еПСзЧЕжЬЇеИґдЄ≠жЙЃжЉФйЗНи¶БиІТиЙ≤пЉМдЄЇжΥ糥зЦЊзЧЕжЦ∞зЪДиЗізЧЕиЈѓеЊДжПРдЊЫдЇЖжЦєеРСгАВ
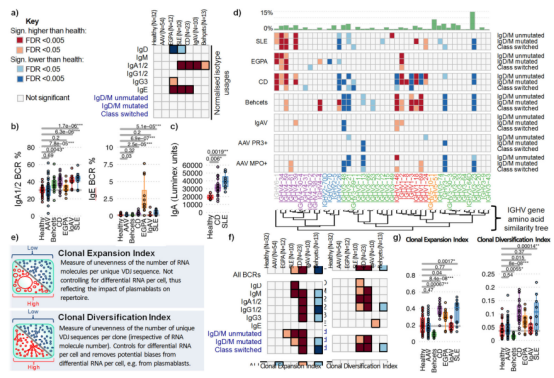
еЫЊ1
IGHVеЯЇеЫ†дљњзФ®еЈЃеЉВпЉЪ
BCRжШѓзФ±VDJеЯЇеЫ†зЙЗжЃµзЪДйЗНзїДжЮДжИРпЉМжЯРдЇЫIGHVеЯЇеЫ†дЉШеЕИзїУеРИеЊЃзФЯзЙ©жКЧеОЯжИЦдЄОиЗ™иЇЂеЕНзЦЂзЫЄеЕ≥гАВдЄОеБ•еЇЈдЇЇзЫЄжѓФпЉМIGHV4еЃґжЧПеЯЇеЫ†еТМIGHV6-1еЯЇеЫ†йҐСзОЗеЬ®CDгАБSLEгАБеТМEGPAдЄ≠жШОжШЊеҐЮеК†пЉИеЫЊ1dпЉЙгАВжЧҐеЊАз†Фз©ґиЃ§дЄЇIGHV4-34иГљзїУеРИиЗ™иЇЂжКЧеОЯеТМиВ†йБУеЕ±зФЯиПМпЉМеєґдЄОSLEжЬЙеЕ≥пЉЫV6-1еТМV4-59еЭЗдЄОиЗ™иЇЂеПНеЇФжАІжЬЙеЕ≥гАВеЬ®BDжВ£иАЕдЄ≠пЉМIGHV1-46гАБIGHV1-3гАБIGHV1-69з≠ЙдЄОжДЯжЯУзЫЄеЕ≥зЪДеЯЇеЫ†еѓМйЫЖпЉИеЫЊ1dпЉЙгАВињЩдЇЫзїУжЮЬжПРз§ЇпЉМеЊЃзФЯзЙ©еПѓиГљйАЪињЗдЄОиЗ™иЇЂжКЧеОЯзЪДдЇ§еПЙеПНеЇФпЉМиѓ±еПСжИЦеК†йЗНиЗ™иЇЂеЕНзЦЂзЧЕпЉМдЄЇ вАЬеЊЃзФЯзЙ© – еЕНзЦЂдЇТдљЬвАЭ иЗізЧЕжЬЇеИґжПРдЊЫдЇЖзЫіжО•иѓБжНЃгАВ
дЄФIGHV еЯЇеЫ†еЈЃеЉВеЬ® вАЬnaive B зїЖиГЮвАЭ еТМ вАЬжКЧеОЯзїПеОЖ B зїЖиГЮвАЭ дЄ≠еЭЗе≠ШеЬ®пЉМдЄФдЄНдїЕйЩРдЇОзЦЊзЧЕеПСзФЯеРОзЪДеЕЛйЪЖжЙ©еҐЮпЉМжПРз§ЇйГ®еИЖеЈЃеЉВеПѓиГљжШѓзЦЊзЧЕжШУжДЯеЫ†зі†гАВ
еЕЛйЪЖзЙєеЊБпЉЪ
CDгАБSLEзЪД BCR еЕЛйЪЖжЙ©еҐЮжШЊиСЧеҐЮеЉЇпЉМеЕЛйЪЖе§Ъж†ЈжАІжЫійЂШпЉИе∞§еЕґ IgAгАБIgG гАБIgMдЇЪеЮЛпЉЙпЉЫEPGAдєЯжШѓеРМж†ЈзЪДиґЛеКњпЉИIgEдЄЇдЄїпЉЙгАВBDдЄОдєЛзЫЄеПНпЉМеЕЛйЪЖжЙ©еҐЮеТМе§Ъж†ЈжАІеЭЗдљОдЇОеѓєзЕІзїДпЉЫAAVгАБIgAV дЄОеБ•еЇЈеѓєзЕІжЧ†жШОжШЊеЈЃеЉВпЉИеЫЊ1fгАБgпЉЙгАВ
еРМеЮЛиљђжНҐпЉЪ
йАЪињЗйЗПеМЦеЕ±дЇЂеФѓдЄАVDJеМЇеЯЯзЪД2дЄ™дЇЪеЮЛзЪДеЕЛйЪЖйҐСзОЗжЭ•иѓДдЉ∞еРМеЮЛиљђжНҐпЉИCSRпЉЙдЇЛдїґйҐСзОЗгАВIMDдЄ≠еРМеЮЛиљђжНҐеЈЃеЉВйАЪеЄЄеѓєеЇФдЇОдЇЪеЮЛдљњзФ®еЈЃеЉВгАВAAVеТМBDдЄ≠жЙАжЬЙиљђжНҐеЭЗеЗПе∞СпЉМIgVдЄ≠IgMдЄОIgGдєЛйЧізЪДиљђжНҐеЗПе∞СгАВSLEеТМCDдЄ≠IgAеТМIgEиљђжНҐеҐЮеК†гАВCDдЄ≠еРМеЮЛиљђжНҐеНЗйЂШдЄОеРМеЮЛйҐСзОЗжЧ†еЕ≥гАВEGPAдЄ≠жЙАжЬЙеРМеЮЛеРСIgEеИЗжНҐзЪДеҐЮеК†жШЊиСЧпЉИе∞§еЕґжШѓIgG3пЉЙпЉИеЫЊ2dпЉЙ.еРМеЮЛиљђжНҐзЪДз≥їзїЯеИЖжЮРжП≠з§ЇдЇЖзЦЊзЧЕзЙєеЉВжАІзЪДиљђжНҐж®°еЉПпЉМжѓФе¶ВEGPAдЄ≠IgG3-IgEзЪДиљђжНҐеҐЮеК†пЉМдї•еПКAAVеТМBDдЄ≠иљђжНҐеЗПе∞СпЉМжШѓжДПжЦЩдєЛе§ЦзЪДпЉМеПѓиГљдЄОзЦЊзЧЕеПСзЧЕжЬЇеИґзЫЄеЕ≥гАВ
IgEзЪДзЛђзЙєжЭ•жЇРпЉЪдЇЇз±ї IgE еЕЛйЪЖе§ЪжЭ•иЗ™еЙНдљУеРМзІНеЮЛзЪДиЃ∞ењЖ B зїЖиГЮпЉМIgEжЬАињСзЪДеЕЛйЪЖдЇ≤е±ЮиЊГе∞СпЉМдЄФе§ІеЮЛеЕЛйЪЖдЄ≠ IgE еПѓйАЪињЗе§Ъжђ°зЛђзЂЛиљђжНҐдЇЛдїґдЇІзФЯпЉМиІ£йЗКдЇЖ EGPA з≠ЙзЦЊзЧЕдЄ≠ IgE еНЗйЂШзЪДжЬЇеИґпЉИеЫЊ2e-gпЉЙгАВ
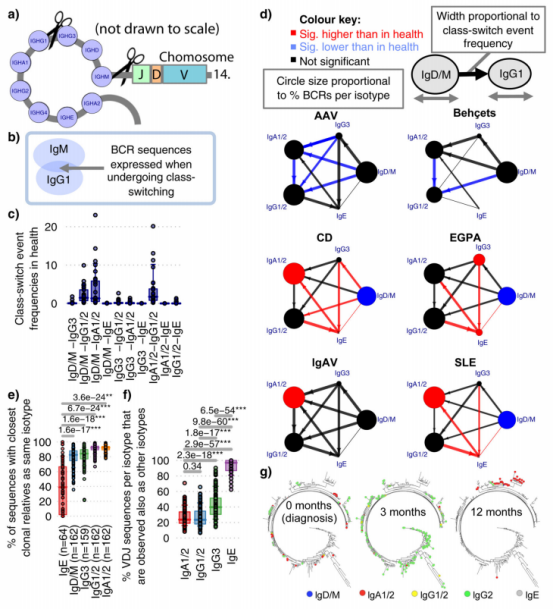
еЫЊ2
ж≤їзЦЧеѓєBCRеЇУзЪДељ±еУНпЉЪ
дљЬиАЕз†Фз©ґдЇЖдЄНеРМж≤їзЦЧеѓєSLEеТМAAVжВ£иАЕBCRеЇУзЪДељ±еУНпЉЪ
-
еȩ嶕жШФеНХжКЧпЉИRTXпЉМжКЧCD20иАЧзЂ≠BзїЖиГЮпЉЙпЉЪж≤їзЦЧеРОпЉМжЃЛзХЩзЪДBзїЖиГЮдї•еРМеЮЛиљђжНҐеРОгАБеЕЛйЪЖжЙ©еҐЮзЪДзїЖиГЮдЄЇдЄїпЉИAAV дЄ≠дї•IgAдЄЇдЄїпЉМSLEдЄ≠дї•IgG1/2дЄЇдЄїпЉЙпЉМдЄФIgD+/IgM+жЬ™з™БеПШзїЖиГЮзЪДйЗНеїЇзЉУжЕҐгАВ
-
еРЧжЫњйЇ¶иАГйЕЪйЕѓпЉИMMFпЉМжКСеИґеҐЮжЃЦзїЖиГЮпЉЙпЉЪж≤їзЦЧеРОжШЊиСЧеҐЮеК† IgM+/IgD+ B зїЖиГЮжѓФдЊЛпЉМеЗПе∞СеРМеЮЛиљђжНҐBзїЖиГЮзЪДжХ∞йЗПеТМеЕЛйЪЖжАІпЉМдњЭзХЩIgMеЕЛйЪЖпЉИжЧ†иЃЇжШѓеР¶еПСзФЯдљУзїЖиГЮйЂШйҐСз™БеПШпЉЙпЉМжПРз§ЇеЕґеѓєеҐЮжЃЦдЄ≠зЪДиљђжНҐеЮЛBзїЖиГЮжКСеИґдљЬзФ®жЫіеЉЇгАВдЇЪеЮЛиљђжНҐеЮЛеЕЛйЪЖзЇ¶еЬ®ж≤їзЦЧдЄАеєіеРОиЊЊеИ∞еБ•еЇЈж∞іеє≥гАВ
-
дЄіеЇКеЕ≥иБФпЉЪAAV жВ£иАЕдЄ≠пЉМиљђжНҐеЮЛеЕЛйЪЖзЪДдљОжМБзї≠жАІдЄО ANCA жїіеЇ¶йЩНдљОзЫЄеЕ≥пЉЫMMF еПѓеЗПе∞СиљђжНҐеЮЛеЕЛйЪЖпЉМжИЦеПѓзФ®дЇОйҐДйШ≤RTXж≤їзЦЧеРОзЪДе§НеПСгАВ
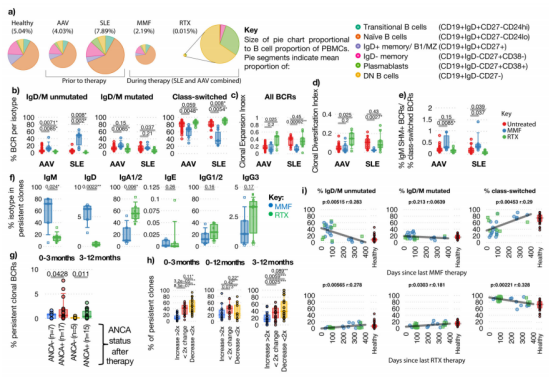
еЫЊ3

иѓ•з†Фз©ґеЕЕеИЖе±ХзО∞дЇЖBCRжµЛеЇПеЬ®еЕНзЦЂзЧЕз†Фз©ґдЄ≠зЪДеЈ®е§ІжљЬеКЫгАВеЃГдЄНдїЕжП≠з§ЇдЇЖе§ЪзІНIMDдЄ≠BCRеЇУзЪДе§НжЭВзїУжЮДпЉМдЄЇзРЖиІ£зЦЊзЧЕеПСзЧЕжЬЇеИґжПРдЊЫдЇЖеЕ®жЦ∞иІЖиІТпЉМињШеЬ®дЄіеЇКеЇФзФ®жЦєйЭҐе±ХзО∞еЗЇеєњйШФеЙНжЩѓпЉМжѓФе¶ВдЄНеРМиНѓзЙ©еѓєBCRеЇУзЪДеЈЃеЉВеМЦељ±еУНдЄЇдЄ™дљУеМЦж≤їзЦЧжПРдЊЫдЇЖеИЖе≠Ре±ВйЭҐзЪДеПВиАГпЉМеП¶е§ЦжЬ™жЭ•зїУеРИеЊЃзФЯзЙ©зїДеИЖжЮРеТМжКЧеОЯзЙєеЉВжАІй™МиѓБпЉМжЬЙжЬЫињЫдЄАж≠•жШОз°Ѓ вАЬеЊЃзФЯзЙ© – IGHV дЇ§еПЙеПНеЇФ – иЗ™иЇЂеЕНзЦЂвАЭ зЪДиЗізЧЕйУЊжЭ°пЉМдЄЇеЉАеПСжЦ∞зЪДж≤їзЦЧйЭґзº商еЃЪеЯЇз°АгАВ
еПВиАГжЦЗзМЃ
Bashford-Rogers RJM, et,al. Analysis of the B cell receptor repertoire in six immune-mediated diseases. Nature. 2019 Oct;574(7776):122-126. doi: 10.1038/s41586-019-1595-3. Epub 2019 Sep 25. PMID: 31554970; PMCID: PMC6795535.
иЙЊж≤РиТљдЄУж≥®дЇОеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯе§ЪеєіпЉМеЉАеПСзЪДImmuHub¬ЃжКАжЬѓеє≥еП∞жЦєж≥ХеЕ®йЭҐпЉМж£АжµЛзЙ©зІНе§Ъж†ЈпЉМеїЇеЇУжЦєж≥ХеЕЈжЬЙзБµжіїжАІпЉМиЗіеКЫдЇОдЄЇеРДе§ІйЂШж†°гАБеМїйЩҐгАБзІСз†ФжЬЇжЮДгАБдЉБдЄЪз≠ЙжПРдЊЫдЉШиЙѓзЪДзІСз†ФжЬНеК°гАВ

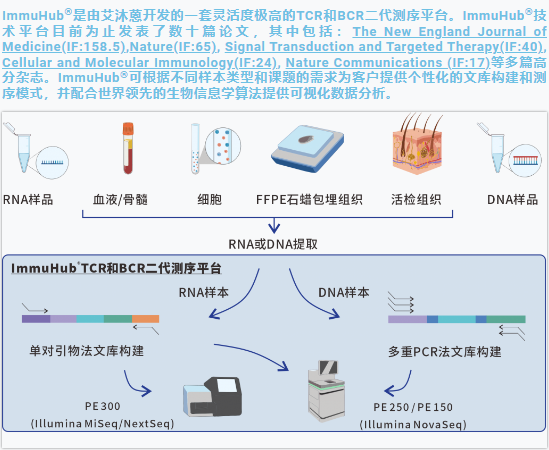
ImmuHub¬ЃйГ®еИЖзІСз†ФжЦєеРС

ImmuHub¬ЃйАВзФ®еЯЇеЫ†еЇІ
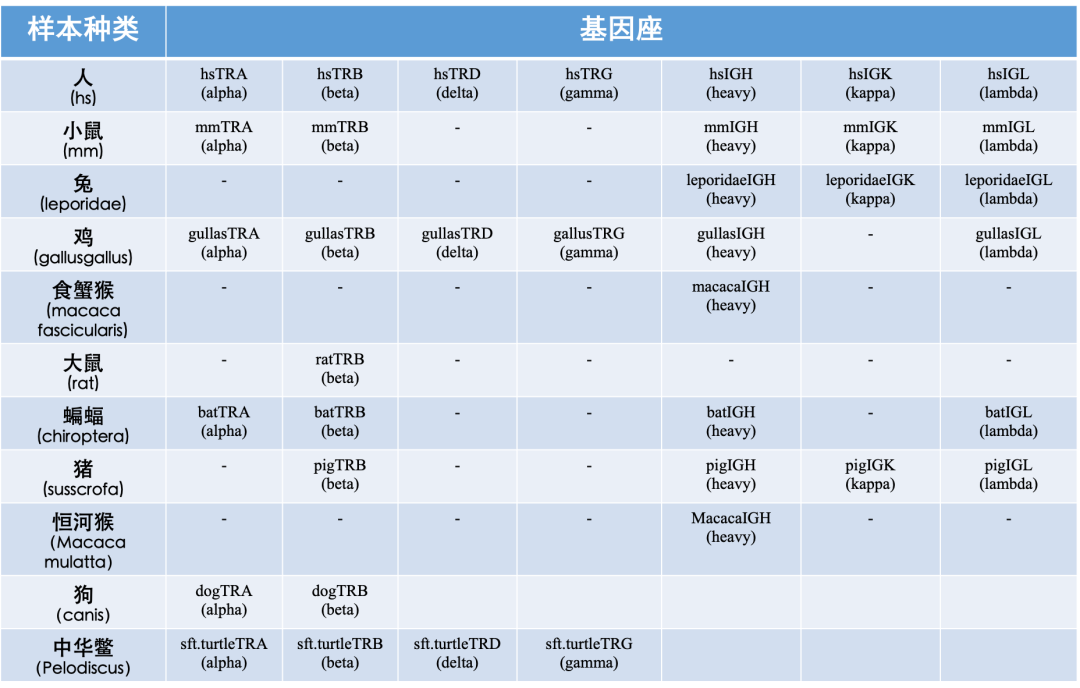
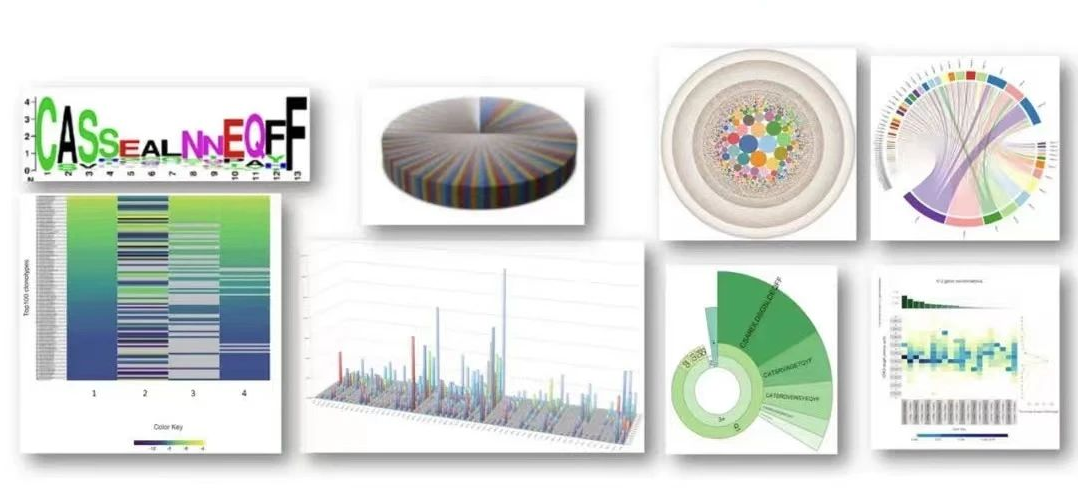
йГ®еИЖжХ∞жНЃеИЖжЮРзїУжЮЬе±Хз§Ї
жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄжИРзЂЛдЇО2016еєіпЉМжШѓеЫљйЩЕеЙНж≤њзЪДдЄУж≥®дЇОеЕНзЦЂй©±еК®еМїе≠¶жКАжЬѓзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪеТМдЄУз≤ЊзЙєжЦ∞дЉБдЄЪгАВеИЫеІЛдЇЇеЫҐйШЯжЭ•иЗ™зЊОеЫљиКЭеК†еУ•е§Іе≠¶пЉМеЬ®2010еєіеЉАеІЛдљњзФ®еЕНзЦЂзїДеЯЇеЫ†йЂШйАЪйЗПжµЛеЇПжКАжЬѓеЉАе±ХеРДзІНзЦЊзЧЕзЫЄеЕ≥з†Фз©ґпЉМдЇО2016еєійАЪињЗиЗ™дЄїз†ФеПСпЉМеЕ®еЫљй¶ЦеЃґжО®еЗЇNGS-MRDи°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛSeq-MRD¬ЃпЉМеєґжОИжЭГж≥ЫзФЯе≠РдљњзФ®гАВеРМжЧґпЉМеЕђеПЄжЛ•жЬЙImmun-Traq¬ЃиВњзШ§ж≤їзЦЧдЉійЪПиѓКжЦ≠гАБImmun-Cheq¬Ѓ¬†еЕНзЦЂеКЫжµЛиѓДдї•еПКImmuHub¬ЃеЕНзЦЂзїДжµЛеЇПзІСз†ФжЬНеК°дЇІеУБпЉМеєґеЄГе±АжЬЙеЯЇдЇОAIжЬЇеЩ®е≠¶дє†зЃЧж≥ХзЪДT-classifier¬ЃиВњзШ§жЧ©з≠ЫгАБеНХзїЖиГЮжµЛеЇПгАБжЦ∞жКЧеОЯгАБTCRеТМжКЧдљУеПСзО∞з≠Йеє≥еП∞зЃ°зЇњгАВзЫЃеЙНдЄЇж≠ҐеПСи°®дЇЖ50дљЩзѓЗиЃЇжЦЗпЉМеЕґдЄ≠еМЕжЛђпЉЪThe New England Journal of Medicine(IF:158.5), The Lancet(IF:98.4), Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24),¬†Nature Communications¬†(IF:17)з≠Йе§ЪзѓЗйЂШеИЖжЭВењЧгАВеЕђеПЄжЮДеїЇеЗ†еНБй°єеПСжШОдЄУеИ©еТМиљѓдїґиСЧдљЬжЭГдЄЇж†ЄењГзЪДиЗ™дЄїзЯ•иѓЖдЇІжЭГдљУз≥їпЉМдЄЇеМїйЩҐдЄіеЇКгАБзФЯеСљзІСе≠¶з†Фз©ґгАБжЦ∞иНѓеЉАеПСз≠ЙжПРдЊЫиІ£еЖ≥жЦєж°ИеТМдЇІеУБгАВиЙЊж≤РиТљдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХгАВ


