
利妥昔单抗(RTX)是一种广泛用于系统性红斑狼疮(SLE)的“非标签”治疗药物(尽管临床试验终点未完全达标,但临床常用),它通过靶向CD20耗竭B细胞来发挥作用。患者对RTX的反应存在高度异质性,且其药物作用分子机制尚不完全清楚。
近期剑桥桑格研究所和帝国理工学院的研究团队发表于《Arthritis & Rheumatology》上的一篇题为“Single-cell level characterization of B cell depletion and repopulation following rituximab in systemic lupus erythematosus”的研究,在单细胞水平系统性解析了SLE患者经RTX治疗后B细胞清除、重建的动态过程,明确了治疗有效与无效患者的核心免疫差异,为优化SLE靶向治疗、预测疗效提供了关键依据。

纳入9例SLE患者(5名应答者,4名非应答者)和8例健康对照。采集治疗前、治疗后早期(1-6个月,清除期)和治疗后晚期(7-15个月,重建期)等多个时间点样本,进行单细胞RNA-seq+BCR-seq+TCR-seq+CITE-seq和bulk BCR-seq,分析不同应答患者的细胞丰度差异、免疫组库多样性、差异基因、通路活性等。
研究揭示了B细胞亚群在治疗后的不同变化。在治疗早期,初始B细胞、记忆B细胞和年龄相关B细胞(ABCs)均显著减少,其他细胞类型如浆细胞/浆母细胞等基本不受影响。
-
早期清除:初始B、记忆B、年龄相关B细胞(ABC)显著减少;浆细胞/浆母细胞几乎不受影响(CD20低表达);过渡B细胞几乎不减少。
-
晚期重建:治疗晚期过渡B细胞、初始B细胞、未转换记忆B细胞、ABC等细胞数量较早期增加,说明患者体内的B细胞重建开始。
通过单细胞VDJ数据和bulk BCR IGH数据分析利妥昔单抗治疗前后BCR库的特征变化。在治疗后早期,多数患者BCR多样性下降,突变频率增加,类别转换序列增加,说明存活的多是抗原经历B细胞。治疗晚期这些指标恢复到治疗前水平。这与初始B细胞的减少及随后的重建过程一致。
在治疗前和治疗后至少1个时间点中均存在的克隆被定义为“持续性克隆”,持续性克隆在响应者和非响应者中均存在。这些持续性克隆主要是转换型记忆B细胞、浆母细胞和浆细胞,平均突变率更高,是治疗后残留的致病性克隆。
由于过渡期和初始B细胞会优先被清除并随后重建,因此对这些细胞的BCR进行了分析。与健康对照组相比,SLE患者的过渡期和初始B细胞CDR3长度均较短,且这一现象在治疗前和治疗后期均保持一致。
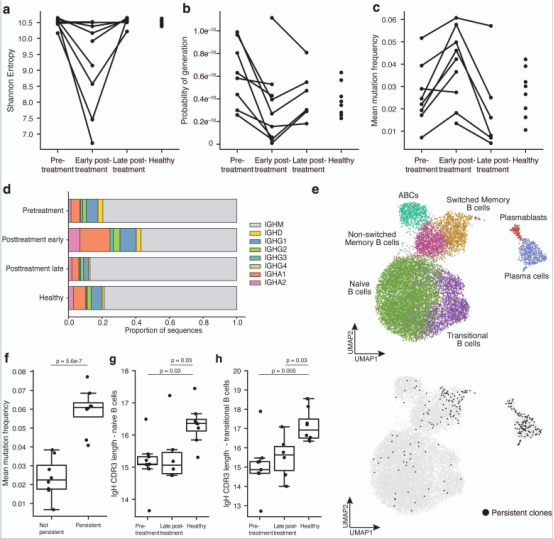
图1
比较治疗前后的基因表达变化。在7种非B细胞的免疫细胞亚型中共识别出27个差异基因,其中调节性 CD4 T(Treg)、双阴性 T(DN T) 拥有最多的差异表达基因。作者重点关注了干扰素相关基因的转录组变化。仅个别干扰素刺激基因下调,没有固定的干扰素通路评分在细胞亚型中均有变化。
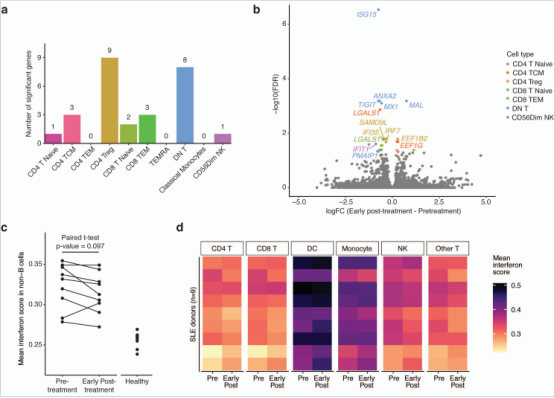
图2
清除程度:所有患者治疗后均显示出B细胞比例的降低,但4例非响应者中有3例发现了B细胞清除不完全的现象(治疗后早期B细胞占比>1%),该不完全耗竭现象并非源于治疗前CD20表面蛋白水平差异。治疗后期B细胞比例与治疗前无显著差异。治疗后早期,响应者中ABC、转换型记忆B细胞完全清除,而非响应者中未观察到这一现象,且浆细胞略有上升。
重建情况:治疗晚期,响应者以过渡B细胞为主,ABC/记忆B细胞持续低水平。与之一致的是,BCR数据显示IgM使用占主导地位。而非响应者各亚型无显著改变,但观察到IgA抗体富集趋势及持续性IgA克隆数量增加,提示抗原经历细胞残留。
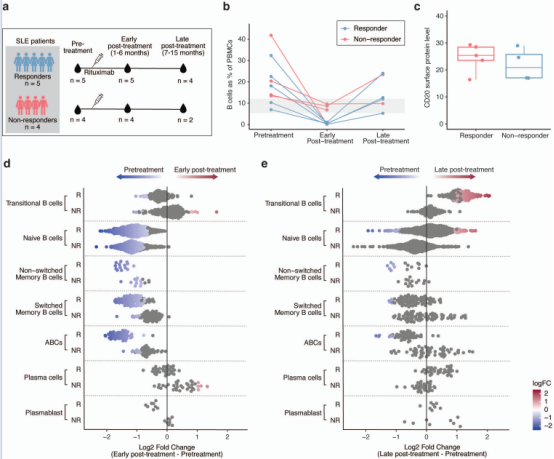
图3
比较响应者的治疗前与治疗晚期的初始B细胞基因表达差异。共有171个差异表达基因,集中在免疫调控、SLE风险基因(SOCS1/3、PTGER4等)。
鉴于NF-κB信号在免疫调控中的核心作用,重点分析了该通路。所有应答者中,治疗后期初始B细胞的NF-κB通路激活水平较治疗前显著降低,与健康对照组水平相似。而非应答者在治疗后期表现出更高的激活水平。
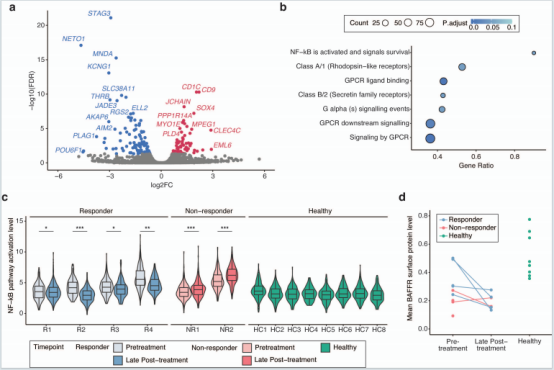
图4
通过比较治疗前至治疗早期的应答特异性效应,分析了非B细胞的基因表达变化。共有99个基因显示出基于利妥昔单抗反应的差异表达变化,集中在CD4中央记忆T(TCM)、DN T细胞,许多差异表达基因参与细胞毒性反应、MHC II类抗原呈递及T细胞活化过程。这些基因在应答者中大多呈现表达上调现象,且表达细胞比例更高。这表明非B细胞的转录组变化具有临床应答依赖性特征,响应者的T细胞更倾向清除致病性B细胞。
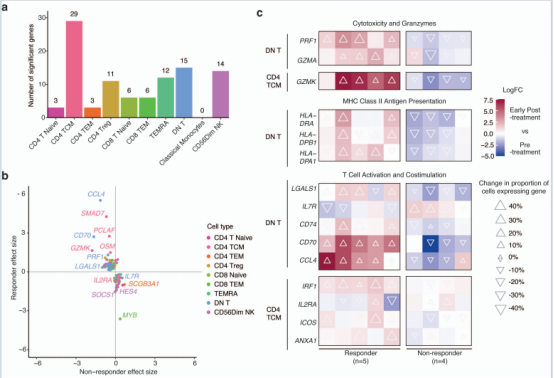
图5
这项研究通过高分辨率的单细胞多组学技术对系统性红斑狼疮(SLE)患者接受利妥昔单抗治疗后的免疫动态进行了纵向追踪,核心结论在于揭示了临床疗效与B细胞的“深度清除及良性重建”以及特定的免疫分子特征密切相关。这为理解利妥昔单抗的耐药机制及开发疗效预测标志物提供了关键的分子图谱。
文献来源:
Jang H, Buang N, Sutherland C, et al. Single-cell level characterization of B cell depletion and repopulation following rituximab in systemic lupus erythematosus. Arthritis Rheumatol. Published online March 5, 2026.
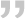
艾沐蒽专注于免疫驱动医学领域多年,开发的ImmuHub®技术平台方法全面,检测物种多样,建库方法具有灵活性,致力于为各大高校、医院、科研机构、企业等提供优良的科研服务。

ImmuHub®部分科研方向

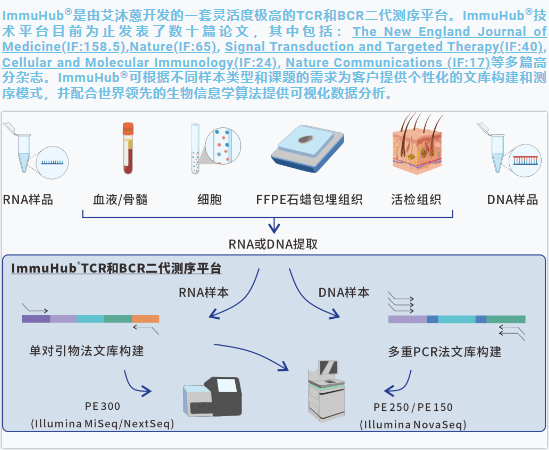
ImmuHub®适用基因座
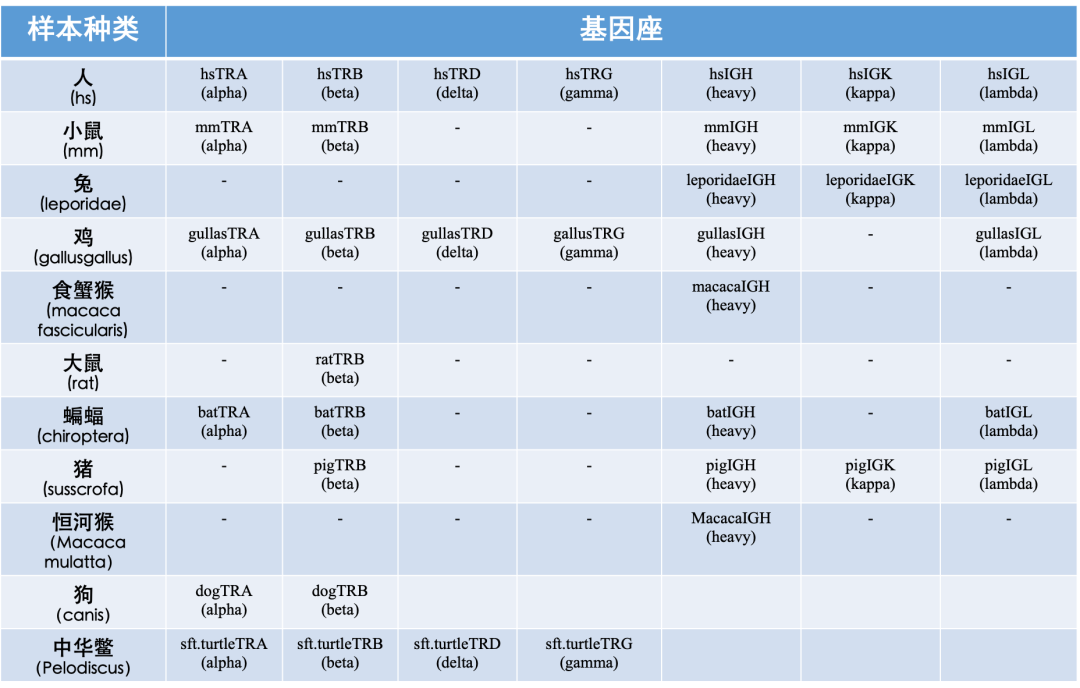
部分数据分析结果展示
杭州艾沐蒽生物科技有限公司成立于2016年,是国际前沿的专注于免疫驱动医学技术的国家高新技术企业和专精特新企业。创始人团队来自美国芝加哥大学,在2010年开始使用免疫组基因高通量测序技术开展各种疾病相关研究,于2016年通过自主研发,全国首家推出NGS-MRD血液肿瘤微小残留病(MRD)检测Seq-MRD®,并授权泛生子使用。同时,公司拥有Immun-Traq®肿瘤治疗伴随诊断、Immun-Cheq® 免疫力测评以及ImmuHub®免疫组测序科研服务产品,并布局有基于AI机器学习算法的T-classifier®肿瘤早筛、单细胞测序、新抗原、TCR和抗体发现等平台管线。目前为止发表了60余篇论文,其中包括:The New England Journal of Medicine(IF:158.5), The Lancet(IF:98.4), Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24), Nature Communications (IF:17)等多篇高分杂志。公司构建几十项发明专利和软件著作权为核心的自主知识产权体系,为医院临床、生命科学研究、新药开发等提供解决方案和产品。艾沐蒽专注于通过解码适应性免疫系统来改变疾病的诊断和治疗,并致力于推进免疫驱动医学领域发展。


