
目前的癌症免疫治疗仍受抗原呈递不足和免疫抑制性肿瘤微环境的限制,效果有限。
近日厦门大学专家团队在Science Advances杂志(IF:12.5)发表了题为“Cold atmospheric plasma–engineered nanovaccine with spatiotemporal sequential immunization reprograms antitumor immunity”的肿瘤免疫治疗重磅研究,该团队开发了一种基于冷大气等离子体(CAP)工程化的免疫重编程囊泡疫苗,通过结合时空序贯免疫策略,实现对肿瘤抗原高效递呈及免疫微环境重塑,解决传统癌症疫苗抗原呈递弱、依赖抗原提呈细胞、肿瘤免疫抑制、易免疫逃逸等痛点。
该研究采用了艾沐蒽ImmuHub® TCR测序分析平台,发现在多种小鼠肿瘤模型中注射该疫苗后,TCR克隆多样性增加,意味着免疫系统能识别更多种类的肿瘤抗原,克服了肿瘤异质性。

T细胞介导的免疫监视是消除恶性细胞的关键,其依赖于对MHC-I分子递呈的肿瘤特异性抗原的识别。肿瘤通过基因突变或表观遗传变化下调MHC-I逃避CD8+T细胞免疫监视,从而导致对检查点抑制剂、过继性T细胞疗法和常规疫苗的耐药性。
此外,肿瘤间异质性和肿瘤内克隆进化,使得癌症疫苗研究在抗原选择和免疫广度方面面临巨大挑战。传统疫苗递呈依赖于抗原递呈细胞(APC)吞噬、处理和交叉递呈抗原,这是一个多步骤的过程,在肿瘤微环境(TME)中容易受免疫抑制干扰而效率低下。因此,建立兼具高效抗原递呈与广谱免疫应答的疫苗策略是肿瘤免疫治疗取得突破的关键。
该研究团队开发的CAPTURE(Cold Atmospheric Plasma-engineered Tumor cell–derived Immune Reprogramming Nanovesicles)是一种结合了物理技术(冷大气等离子体,CAP)与生物工程的仿生纳米疫苗。它由三部分核心逻辑构成:
-
CAP处理:利用物理手段处理肿瘤细胞。
-
“全谱抗原”呈递:激活p62介导的自噬通路,大幅上调 MHC-I,呈递全谱胞内+膜肿瘤抗原。
-
“自带共刺激”信号:绕过传统抗原呈递细胞(APC),直接激活T细胞。
在此作用机制基础上,团队进一步提出了一种将皮下预免(淋巴靶向)与静脉增强(肿瘤归巢)相结合的时空序贯免疫(SSI)策略:先通过皮下注射靶向淋巴结,启动免疫,激活 T 细胞;再通过静脉注射靶向同源肿瘤,利用CAP诱导表达的融合蛋白(如v-SNARE)实现与同源肿瘤细胞的高效融合,将MHC-I抗原复合物和抗CD28分子转移至肿瘤细胞表面,重塑肿瘤免疫原性,招募T细胞浸润。一 “诱” 一 “攻”,实现全身免疫激活+局部肿瘤清除。
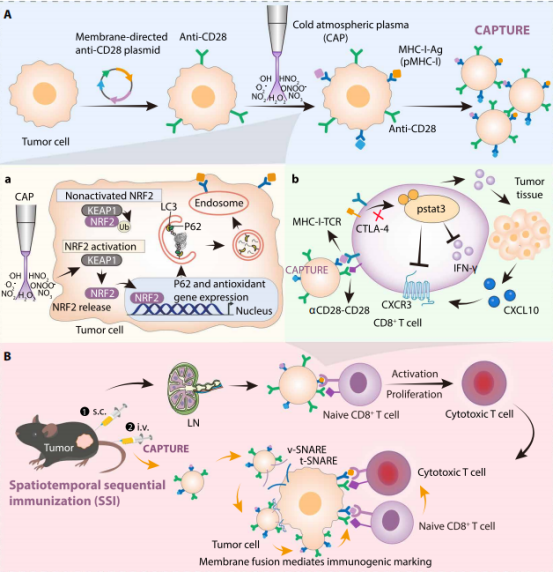

CAP产生的活性氧(主要是·OH)激活了细胞内的KEAP1-Nrf2-p62信号轴, Nrf2入核,上调p62,增强自噬流, 降解胞内蛋白,MHC-I抗原呈递全面增强。经验证,p62 敲低后,MHC-I上调被显著抑制。与IFN-γ对比,CAP上调MHC-I效果相当,但不诱导PD-L1。

传统疫苗依赖APC激活T细胞,但APC表面的B7分子一旦结合T细胞上的CTLA-4,就会抑制T细胞免疫效应。而CAPTURE在纳米囊泡表面直接修饰抗CD28抗体(αCD28),这种设计让疫苗能直接与杀伤性T细胞(CD8+ T)表面的CD28结合,绕过了B7-CTLA-4通路,直接激活T细胞。

CXCR3-CXCL10轴驱动T细胞浸润
CAPTURE还上调了CD8+ T细胞的趋化因子受体CXCR3表达,同时刺激肿瘤组织分泌趋化因子CXCL10,引导大量CXCR3+ CD8+ T细胞高效浸润至肿瘤内部。这是疫苗从“激活免疫”到“杀伤肿瘤”的关键桥梁。
在黑色素瘤(B16-OVA)、肝癌(H22)和结肠癌(MC38)的小鼠模型中,CAPTURE展现了惊人的效果:
-
肿瘤生长:接近完全抑制,显著优于传统疫苗和PD-1/CTLA-4抗体治疗。
-
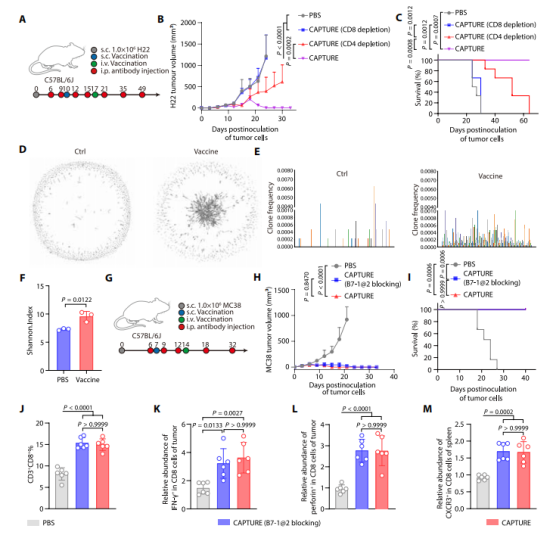
T细胞反应:CD8+ T细胞大量扩增、浸润肿瘤;Treg显著减少。通过TCR测序发现,与对照组相比,疫苗组TCR克隆聚类更显著,可能代表着更强的抗原特异性克隆应答(图D)。同时疫苗组TCR克隆多样性也显著更高(图E、F),意味着更能应对肿瘤的异质性。
-
免疫浸润:肿瘤内部杀伤性T细胞(CTL)大量浸润,且表达高水平的IFN-γ和颗粒酶。
-
微环境:肿瘤相关巨噬细胞(TAMs)从促癌的M2型逆转为抑癌的M1型。
该研究利用低温大气等离子体工程化改造肿瘤细胞纳米囊泡,构建CAPTURE疫苗,通过p62自噬增强全谱抗原呈递+αCD28直接激活T细胞+时空序贯靶向递送,彻底重编程抗肿瘤免疫,在小鼠模型实现近乎完全的肿瘤抑制,为克服肿瘤免疫逃逸、开发个性化广谱肿瘤疫苗提供了全新技术与理论。
文献来源
Li S, Wang P, Wu Z, et al. Cold atmospheric plasma-engineered nanovaccine with spatiotemporal sequential immunization reprograms antitumor immunity. Sci Adv. 2026;12(13):eaeb5894.
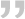
艾沐蒽专注于免疫驱动医学领域多年,开发的ImmuHub®技术平台方法全面,检测物种多样,建库方法具有灵活性,致力于为各大高校、医院、科研机构、企业等提供优良的科研服务。
ImmuHub®部分科研方向

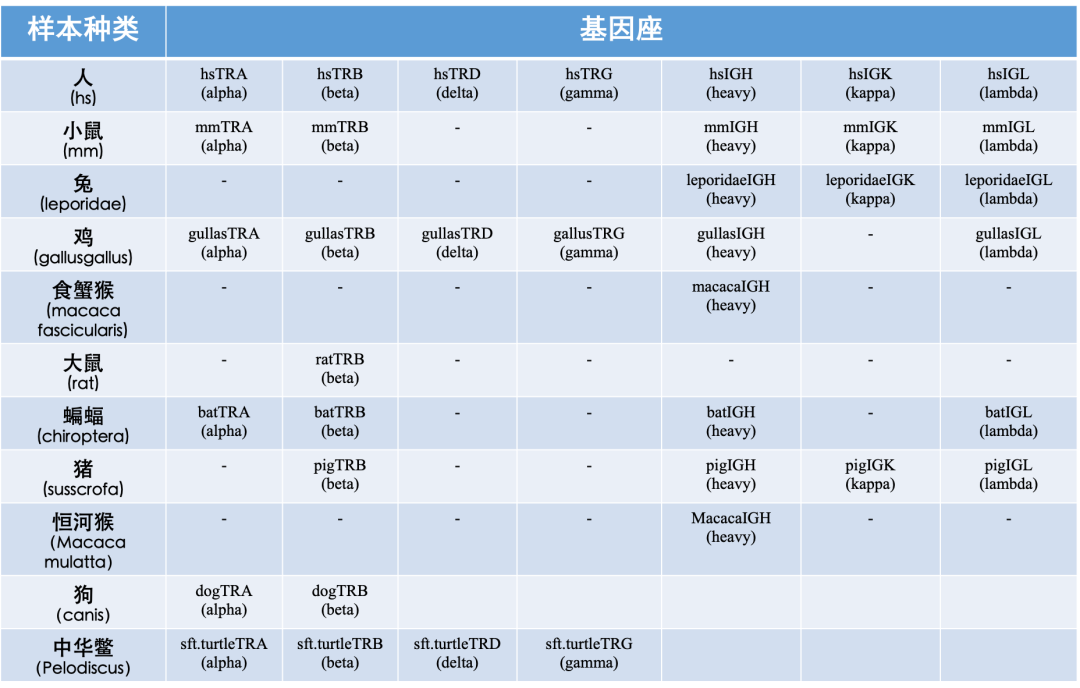
ImmuHub®适用基因座
部分数据分析结果展示
杭州艾沐蒽生物科技有限公司成立于2016年,是国际前沿的专注于免疫驱动医学技术的国家高新技术企业和专精特新企业。创始人团队来自美国芝加哥大学,在2010年开始使用免疫组基因高通量测序技术开展各种疾病相关研究,于2016年通过自主研发,全国首家推出NGS-MRD血液肿瘤微小残留病(MRD)检测Seq-MRD®,并授权泛生子使用。同时,公司拥有Immun-Traq®肿瘤治疗伴随诊断、Immun-Cheq® 免疫力测评以及ImmuHub®免疫组测序科研服务产品,并布局有基于AI机器学习算法的T-classifier®肿瘤早筛、单细胞测序、新抗原、TCR和抗体发现等平台管线。目前为止发表了60余篇论文,其中包括:The New England Journal of Medicine(IF:158.5), The Lancet(IF:98.4), Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24), Nature Communications (IF:17)等多篇高分杂志。公司构建几十项发明专利和软件著作权为核心的自主知识产权体系,为医院临床、生命科学研究、新药开发等提供解决方案和产品。艾沐蒽专注于通过解码适应性免疫系统来改变疾病的诊断和治疗,并致力于推进免疫驱动医学领域发展。


