
еЬ®B-ALLзЪДNGS MRDж£АжµЛдЄ≠пЉМIGйЗНйУЊпЉИIGHпЉЙдїЈеАЉжЫіе§ІпЉМжЫіеЕЈжЬЙйҐДеРОжДПдєЙпЉМињЩдЄАзВєеЈ≤襀е§ЪзѓЗжЦЗзМЃжЙАиѓБеЃЮпЉМдєЯйАРжЄРжИРдЄЇи°МдЄЪеЖЕдЄУеЃґеЕ±иѓЖгАВиљїйУЊIGL/IGK/IGKDEзЪДзЛђзЙєжАІдЄНе¶ВIGHпЉМжШѓзЫЄеѓєдЄНеПѓйЭ†зЪДйҐДеРОж†ЗењЧзЙ©пЉМдљЖе¶ВдљХеМЇеИЖиљїйУЊдЄ≠жЬЙдїЈеАЉзЪДзЩМзїЖиГЮеЕЛйЪЖдЄОиГМжЩѓеЕЛйЪЖпЉМзЫЃеЙНе∞ЪжЧ†еЃЪиЃЇгАВ
ињСжЧ•иЙЊж≤РиТљиБФеРИжµЩж±Яе§Іе≠¶еМїе≠¶йЩҐйЩДе±ЮеДњзЂ•еМїйЩҐи°Ажґ≤зІСеЊРжЩУеЖЫжХЩжОИеЫҐйШЯеЬ®annals of laboratory medicineжЭВењЧеПСи°®дЇЖйҐШдЄЇвАЬNon-specific Clones Hamper the Reliability of Ig Light Chain Gene Rearrangements in Next-Generation Sequencing-Based Measurable Residual Disease Monitoring in Pediatric B-Cell ALL: A Single-Center Cohort StudyвАЭзЪДжЦЗзЂ†пЉМиѓ•з†Фз©ґйЗЗзФ®зЪДжШѓиЙЊж≤РиТљзЪДSeq-MRD¬ЃжКАжЬѓпЉМз≥їзїЯеИЖжЮРдЇЖIGK/IGKDEйЗНжОТдЄ≠йЭЮзЩљи°АзЧЕзЙєеЉВжАІеЕЛйЪЖзЪДзЙєеЊБпЉМжПРеЗЇD-JдєЛйЧізЪДNеМЇйХњеЇ¶гАБеЬ®дЇЇзЊ§дЄ≠зЪДеИЖеЄГж¶ВзОЗз≠ЙеЫ†зі†жЬЙеК©дЇОињЗжї§йЭЮзЙєеЉВжАІеЕЛйЪЖгАВињЩе∞ЖжПРйЂШеЯЇдЇОIGKйЗНжОТзЫСжµЛMRDзЪДеПѓйЭ†жАІпЉМеѓєдЇОдЉШеМЦNGS MRDзЫСжµЛеТМдЉШеМЦеРОзї≠ж≤їзЦЧеЖ≥з≠ЦиЗ≥еЕ≥йЗНи¶БгАВ
иѓ•жЦЗзЂ†жШѓиЙЊж≤РиТљSeq-MRD¬Ѓеє≥еП∞еПСи°®зЪДзђђ5зѓЗе≠¶жЬѓжИРжЮЬпЉМжЬ™жЭ•иЙЊж≤РиТље∞ЖзїІзї≠еЬ®и°Ажґ≤иВњзШ§NGS MRDж£АжµЛйҐЖеЯЯжЈ±иАХдЄНиЊНгАБжМБзї≠жΥ糥пЉМдї•еЙНж≤њжКАжЬѓиµЛиГљз≤ЊеЗЖиѓКзЦЧпЉМдЄЇи°Ажґ≤иВњзШ§жВ£иАЕзЪДеЇЈе§НдєЛиЈѓж≥®еЕ•жЫіеЭЪеЃЮзЪДеКЫйЗПпЉБ




иѓ•з†Фз©ґзЇ≥еЕ•540дЊЛеДњзЂ•B-ALLжВ£иАЕпЉМ506дЊЛпЉИ93.7%пЉЙжВ£иАЕеИЭиѓКжЧґйЙіеЃЪеИ∞иЗ≥е∞С1дЄ™еПѓињљиЄ™еЕЛйЪЖгАВеЬ®иѓ±еѓЉж≤їзЦЧзїУжЭЯпЉИEOIпЉЙжЧґеТМеЈ©еЫЇж≤їзЦЧзїУжЭЯпЉИEOCпЉЙжЧґйЗЗйЫЖй™®йЂУж†ЈжЬђињЫи°МNGS MRDињљиЄ™ж£АжµЛпЉМеЈ©еЫЇж≤їзЦЧеРОMRDзЫСжµЛжѓП2-3дЄ™жЬИињЫи°МдЄАжђ°пЉМзЫіиЗ≥иљђйШіжИЦжЬАйХњ12дЄ™жЬИгАВдЄїи¶БзїИзВєдЄЇжЧ†е§НеПСзФЯе≠ШжЬЯпЉИRFSпЉЙпЉМжђ°и¶БзїИзВєеМЕжЛђжАїзФЯе≠ШжЬЯпЉИOSпЉЙеТМзіѓиЃ°е§НеПСеПСзФЯзОЗгАВдЄїи¶БйҐДжµЛеЫ†е≠РжШѓдљНзВєзЙєеЉВжАІNGS MRDж∞іеє≥еПКйҐДиЃЊжЧґйЧізВєзЪДMRDжМБзї≠ж®°еЉПпЉМе∞§еЕґйТИеѓєIGHдЄОIGK/IGKDEеЕЛйЪЖеЮЛзЪДжѓФиЊГгАВ



жМБзї≠жАІIGH MRDеПѓйҐДжµЛе§НеПСпЉМжМБзї≠жАІIGK/IGKDEдЄОе§НеПСжЧ†еЕ≥
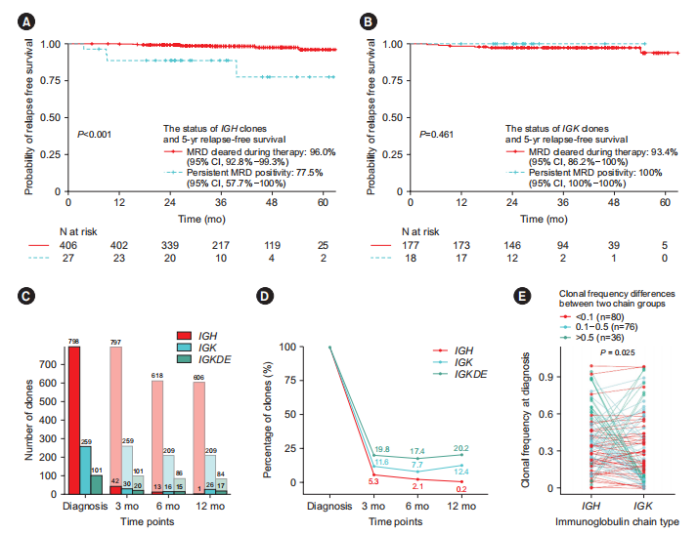
е∞ЖеПѓињљиЄ™еЕЛйЪЖеЬ®EOCжЧґеИЖз±їдЄЇвАЬжЄЕйЩ§вАЭзїДдЄОвАЬжМБзї≠вАЭзїДгАВIGHжЄЕйЩ§зїДеТМжМБзї≠зїДзЪД5еєіRFSзОЗеИЖеИЂдЄЇ96%еТМ77.5%пЉИPпЉЬ0.001пЉЫеЫЊ1AпЉЙпЉЫиАМIGKжЄЕйЩ§зїДеТМжМБзї≠зїДзЪД5еєіRFSзОЗеИЖеИЂдЄЇ93.4%еТМ100%пЉИеЫЊ1BпЉЙгАВињЩи°®жШОжМБзї≠жАІIGH MRDеПѓдљЬдЄЇжШОз°ЃзЪДйЂШй£ОйЩ©ж†ЗењЧпЉМиАМIGKдЄНжШѓгАВ
е∞ЖжВ£иАЕеИЖдЄЇжМБзї≠еЃМеЕ®зЉУиІ£пЉИCCRпЉЙзїДеТМе§НеПСзїДгАВеЬ®CCRзїДдЄ≠пЉМIGHеЕЛйЪЖжХ∞йЗПеЬ®еЙНдЄЙдЄ™жЬИжА•еЙІдЄЛйЩНиЗ≥еЯЇзЇњзЪД5.3%пЉМ6дЄ™жЬИеПК12дЄ™жЬИжЧґињЫдЄАж≠•еЗПе∞СиЗ≥дїЕеЙ©1дЄ™пЉИ0.1%пЉЙпЉИеЫЊ1CпЉЙгАВIGKеТМIGKDEеЕЛйЪЖеЬ®еЙН3дЄ™жЬИеЖЕдєЯжА•еЙІдЄЛйЩНпЉМдљЖйЪПеРОжЄЕйЩ§зОЗиґЛдЇОз®≥еЃЪпЉМиЗ≥12дЄ™жЬИжЧґпЉМдїНжЬЙ12.4%зЪДIGKеЕЛйЪЖеТМ20.2%зЪДIGKDEеЕЛйЪЖеПѓж£АжµЛеИ∞пЉМдЄФеЬ®6иЗ≥12дЄ™жЬИжЬЯйЧіеЗЇзО∞иљїеЊЃеПНеЉєпЉИеЫЊ1DпЉЙгАВињЩдЇЫзїУжЮЬи°®жШОе≠ШеЬ®ж≤їзЦЧиАРиНѓзЪДйЭЮзЩљи°АзЧЕеЕЛйЪЖпЉМиАМйЭЮзЬЯж≠£зЪДMRDгАВ
еѓєеРМжЧґеЕЈжЬЙIGHеТМIGKдЄ§зІНйЗНжОТзЪДжВ£иАЕеЬ®иѓКжЦ≠жЧґзЪДIGHеТМIGKеЕЛйЪЖйҐСзОЗињЫи°МдЇЖйЕНеѓєеИЖжЮРгАВеИЖеЄГеЈЃеЉВжШЊиСЧпЉЪйЭЮзЙєеЉВжАІIGKеЕЛйЪЖжЬ™дЄОеМєйЕНзЪДIGHеЕЛйЪЖ嚥жИРеѓєеЇФеЕ≥з≥їпЉМињЩеЗЄжШЊдЇЖIGHеТМIGKйЬАи¶БеИЖеИЂињЫи°МMRDеИЖжЮРзЪДењЕи¶БжАІпЉИеЫЊ1EпЉЙгАВ
еЫЊ1

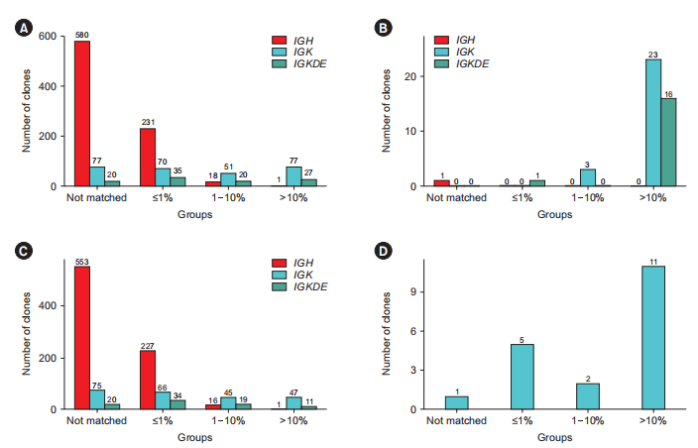
е∞ЖжѓПдЄ™еПѓињљиЄ™еЕЛйЪЖеЇПеИЧдЄОеБ•еЇЈдЇЇIGжХ∞жНЃеЇУпЉИиЙЊж≤РиТљиЗ™еїЇпЉЙињЫи°МжѓФеѓєпЉМеЕЛйЪЖеЮЛжМЙзЕІеЬ®еБ•еЇЈзЊ§дљУдЄ≠зЪДеМєйЕНж¶ВзОЗеИЖдЄЇдЄЙзїДпЉИвЙ§1%гАБ1%вАУ10%еТМ>10%пЉЙгАВдїЕжЬЙ2.4%зЪДIGHеЇПеИЧеМєйЕНж¶ВзОЗиґЕињЗ1%пЉМдїЕжЬЙдЄАдЄ™IGHеЇПеИЧиґЕињЗ10%пЉИеЫЊ2AпЉЙгАВзЫЄжѓФдєЛдЄЛпЉМ46.5%зЪДIGKеТМ46.1%зЪДIGKDEеЕЛйЪЖеЮЛеЬ®еБ•еЇЈIGжХ∞жНЃеЇУдЄ≠еМєйЕНж¶ВзОЗиґЕињЗ1%гАВ
зДґеРОдљЬиАЕз†Фз©ґдЇЖCCRжВ£иАЕеЬ®12дЄ™жЬИжЧґжЄЕйЩ§еТМжМБзї≠йШ≥жАІеЕЛйЪЖеЬ®еБ•еЇЈжХ∞жНЃеЇУдЄ≠еМєйЕНзЪДж¶ВзОЗгАВжМБзї≠йШ≥жАІеЕЛйЪЖдЄ≠пЉМжЙАжЬЙIGHеЭЗжЬ™дЄОеБ•еЇЈжХ∞жНЃеЇУеМєйЕНпЉМиАМ88.5%зЪДIGKеЕЛйЪЖеТМ94.1%зЪДIGKDEеЕЛйЪЖеМєйЕНж¶ВзОЗпЉЮ10%пЉИеЫЊ2BпЉЙгАВеЬ®12дЄ™жЬИжЧґеЈ≤жЄЕйЩ§зЪДеЕЛйЪЖдЄ≠пЉМIGKгАБIGKDEдЄОеБ•еЇЈжХ∞жНЃеЇУеМєйЕНзЪДж¶ВзОЗдєЯињЬйЂШдЇОIGHеЕЛйЪЖпЉИеЫЊ2CпЉЙгАВеЬ®19дЊЛEOIеТМEOCеЭЗIGKйШ≥жАІзЪДжВ£иАЕдЄ≠пЉМ11дЊЛжВ£иАЕзЪДIGKеЇПеИЧдЄОеБ•еЇЈжХ∞жНЃеЇУеМєйЕНзЪДж¶ВзОЗпЉЮ10%пЉИеЫЊ2DпЉЙгАВ
дї•дЄКиѓіжШОзЫЄељУдЄАйГ®еИЖзЪДIGK/IGKDEеПѓињљиЄ™еЕЛйЪЖеЬ®еБ•еЇЈдЇЇдЄ≠дєЯеєњж≥Ые≠ШеЬ®пЉМиАМйЭЮзЩљи°АзЧЕзЙєеЉВжАІеЕЛйЪЖгАВ
еЫЊ2

дљЬиАЕе∞ЖеПѓињљиЄ™зЪДеЕЛйЪЖеИЖдЄЇвАЬзЙєеЉВжАІвАЭеТМвАЬйЭЮзЙєеЉВжАІвАЭдЄ§з±їпЉЪеѓєдЇОзїіжМБCCRвЙ•2еєізЪДжВ£иАЕпЉМиЛ•еЕЛйЪЖеЬ®еМЦзЦЧеРО3дЄ™жЬИеЖЕжґИ姱дЄФеЕґдЄОеБ•еЇЈжХ∞жНЃеЇУзЪДеМєйЕНж¶ВзОЗвЙ§1%пЉМеИЩж†ЗиЃ∞дЄЇзЙєеЉВжАІеЕЛйЪЖпЉЫиЛ•еЕЛйЪЖжМБзї≠вЙ•12дЄ™жЬИдЄФдЄОеБ•еЇЈжХ∞жНЃеЇУзЪДеМєйЕНж¶ВзОЗ>10%пЉМеИЩеИ§еЃЪдЄЇйЭЮзЙєеЉВжАІеЕЛйЪЖгАВдїїдљХеЬ®жЄЕйЩ§еРОе§НеПСжЧґйЗНжЦ∞еЗЇзО∞зЪДеЕЛйЪЖеРМ憣襀ељТз±їдЄЇзЙєеЉВжАІеЕЛйЪЖгАВ
еЇФзФ®иѓ•ж†ЗеЗЖпЉМеЕ±йЙіеЃЪеЗЇзЙєеЉВжАІеЕЛйЪЖIGHжЬЙ699дЄ™гАБIGK 124дЄ™гАБIGKDE 47дЄ™пЉМжЬ™еПСзО∞йЭЮзЙєеЉВжАІIGHеЕЛйЪЖпЉМжЬЙ24дЄ™IGKеЕЛйЪЖеТМ16дЄ™ IGKDEеЕЛйЪЖзђ¶еРИйЭЮзЙєеЉВжАІеЕЛйЪЖеЃЪдєЙгАВ
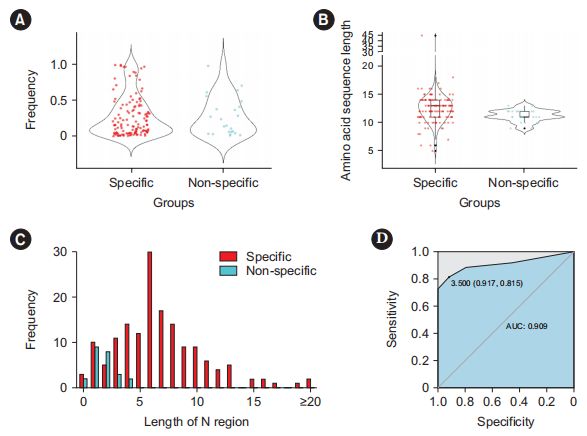
зДґеРОдљЬиАЕжѓФиЊГдЇЖзЙєеЉВжАІдЄОйЭЮзЙєеЉВжАІIGKеЕЛйЪЖзЪДеИЭиѓКеЕЛйЪЖйҐСзОЗеТМеЇПеИЧзїУжЮДгАВеИЭиѓКжЧґзЪДеЕЛйЪЖйҐСзОЗжЧ†жШЊиСЧеЈЃеЉВпЉИеЫЊ3AпЉЙпЉМCDR3йХњеЇ¶иЩљзДґе≠ШеЬ®жШЊиСЧеЈЃеЉВпЉМдљЖдїЕеЗ≠CDR3йХњеЇ¶жЧ†ж≥ХеМЇеИЖIGKзЩљи°АзЧЕеЕЛйЪЖдЄОиГМжЩѓеЕЛйЪЖпЉЪйЭЮзЙєеЉВжАІеЕЛйЪЖдЄїи¶БиБЪйЫЖеЬ®9-13дЄ™ж∞®еЯЇйЕЄеМЇеЯЯпЉМдљЖжШѓдєЯжЬЙ62.4%зЪДзЙєеЉВжАІеЕЛйЪЖжШѓеЬ®иѓ•еМЇеЯЯеЖЕпЉИеЫЊ3BпЉЙгАВ
жЧҐеЊАжЬЙз†Фз©ґеПСзО∞ињЮжО•VеМЇдЄОJеМЇзЪДNеМЇйХњеЇ¶еЬ®зЩљи°АзЧЕеЕЛйЪЖдЄОйЭЮзЩљи°АзЧЕеЕЛйЪЖдЄ≠еЈЃеЉВеЊИе§ІпЉМеЫ†ж≠§дљЬиАЕдєЯеѓєж≠§ињЫи°МдЇЖеИЖжЮРгАВеПСзО∞йЭЮзЙєеЉВжАІеЕЛйЪЖзЪДNеМЇйХњеЇ¶дЄЇ0-4дЄ™ж†ЄиЛЈйЕЄпЉМиАМзЙєеЉВжАІеЕЛйЪЖзЪДNеМЇйХњеЇ¶жЧ†еЫЇеЃЪеАЉпЉМ81.5%зЪДеЕЛйЪЖеЕЈжЬЙвЙ•4дЄ™ж†ЄиЛЈйЕЄпЉИеЫЊ3CпЉЙгАВROCжЫ≤зЇњеИЖжЮРи°®жШОпЉМеИ©зФ®NеМЇйХњеЇ¶йҐДжµЛзЙєеЉВжАІеЕЛйЪЖеЕЈжЬЙйЂШеЗЖз°ЃжАІпЉИеЫЊ3DпЉЙгАВеѓєдЇОEOIеТМEOCжЧґжМБзї≠йШ≥жАІзЪДIGKеЕЛйЪЖпЉМеЯЇдЇОNеМЇйХњеЇ¶пЉЬ4зЪДиІДеИЩеПѓињЗжї§жОЙ63.2%зЪДеЕЛйЪЖгАВ
еЫЊ3

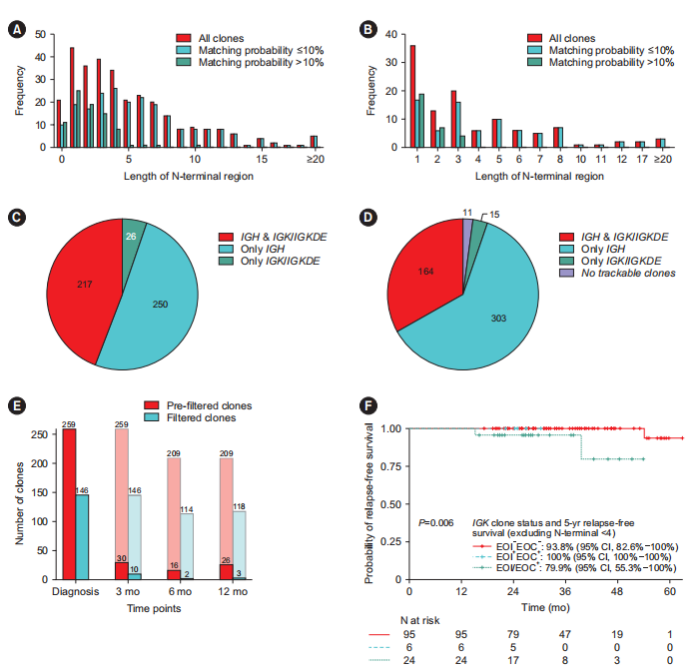
е¶ВеЫЊ4AжЙАз§ЇпЉМеИЭиѓКжЧґ45.9%зЪДIGKеЕЛйЪЖзЪДNеМЇйХњеЇ¶пЉЬ4дЄ™ж†ЄиЛЈйЕЄпЉМдЄОеБ•еЇЈжХ∞жНЃеЇУеМєйЕНж¶ВзОЗпЉЮ10%зЪДIGKеЕЛйЪЖдЄїи¶БеСИзО∞0-3дЄ™ж†ЄиЛЈйЕЄзЪДNеМЇйХњеЇ¶пЉИ85.4%пЉЙпЉМиАМеМєйЕНж¶ВзОЗвЙ§10%зЪДеЕЛйЪЖдЄ≠дїЕжЬЙ31.4%зЪДNеМЇйХњеЇ¶пЉЬ4дЄ™ж†ЄиЛЈйЕЄпЉИP
йЗЗзФ®NеМЇйХњеЇ¶пЉЬ4дЄ™ж†ЄиЛЈйЕЄдЄЇйШИеАЉињЫи°МињЗжї§еРОпЉМжЬЙ11дЊЛжВ£иАЕдЄНеЖНе≠ШеЬ®еПѓињљиЄ™еЕЛйЪЖпЉИеЫЊ4C-DпЉЙпЉМзФ®дЇОMRDзЫСжµЛзЪДIGKеЕЛйЪЖжАїжХ∞дїО278дЄ™йЩНиЗ≥155дЄ™пЉМCCRжВ£иАЕеЬ®12дЄ™жЬИйЪПиЃњжЧґIGKжМБзї≠еЕЛйЪЖзЪДжѓФдЊЛдїО12.4%жШЊиСЧдЄЛйЩНиЗ≥2.5%пЉИеЫЊ4EпЉЙгАВж≠§е§ЦпЉМеЇФзФ®жЦ∞ж†ЗеЗЖеРОпЉМ EOI+EOC+гАБEOIвАУEOCвАУеТМEOI/EOC+зїДзЪДIGKеЕЛйЪЖжХ∞йЗПеЭЗйЩНдљОпЉМеРМжЧґдњЭзХЩдЇЖEOIвАУEOCвАУзїДдЄОEOI/EOC+зїДдєЛйЧізЪДйҐДеРОеЈЃеЉВпЉИеЫЊ4FпЉЙгАВ
еЫЊ4



йЂШзБµжХПеЇ¶зЪДNGS MRDж£АжµЛжО®еК®B-ALLж≤їзЦЧињЫеЕ•вАЬз≤ЊеЗЖеМЦжЧґдї£вАЭпЉМдљЖеЕґдЄіеЇКдїЈеАЉдЊЭиµЦдЇОдЄ•ж†ЉгАБеЗЖз°ЃзЪДзїУжЮЬиІ£иѓїгАВжЬђз†Фз©ґеЖНжђ°иѓБеЃЮдЇЖIGHзЪДйҐДеРОдїЈеАЉдЉШдЇОIGK/IGKDEпЉМињЫдЄАж≠•жΥ糥еПСзО∞дЄАдЇЫIGK/IGKDEеЬ®еБ•еЇЈзЊ§дљУдЄ≠дєЯеЊИеЄЄиІБпЉМињЩдЇЫйЭЮзЩљи°АзЧЕзЙєеЉВжАІеЕЛйЪЖеЙКеЉ±дЇЖиљїйУЊеЬ®MRDзЫСжµЛдЄ≠зЪДдїЈеАЉгАВйАЪињЗV-JдєЛйЧізЪДNеМЇйХњеЇ¶гАБеЬ®еБ•еЇЈдЇЇдЄ≠зЪДеИЖеЄГж¶ВзОЗз≠ЙзЙєеЊБжЬЙеК©дЇОиѓЖеИЂеТМињЗжї§йЭЮзЙєеЉВжАІеЕЛйЪЖгАВиѓ•еПСзО∞еѓєдЇОеЗЖз°ЃеИ©зФ®NGS MRDзїУжЮЬжМЗеѓЉдЄіеЇКж≤їзЦЧеЕЈжЬЙйЗНи¶БжДПдєЙпЉМињЫдЄАж≠•жПРеНЗдЇЖMRDзЫСжµЛзЪДз≤ЊеЗЖеЇ¶пЉМйБњеЕНвАЬеБЗйШ≥жАІвАЭеѓЉиЗізЪДињЗеЇ¶ж≤їзЦЧгАВ

жЦЗзЂ†жЭ•жЇРпЉЪ
Chen H, Miao J, Fan L, et al. Non-specific Clones Hamper the Reliability of Ig Light Chain Gene Rearrangements in Next-Generation Sequencing-Based Measurable Residual Disease Monitoring in Pediatric B-Cell ALL: A Single-Center Cohort Study. Ann Lab Med. Published online February 12, 2026.

иЙЊж≤РиТљдЄУж≥®дЇОеЕНзЦЂзїДдЇМдї£жµЛеЇПйҐЖеЯЯе§ЪеєіпЉМжШѓдЇО2016еєіеЕ®еЫљй¶ЦеЃґжО®еЗЇи°Ажґ≤иВњзШ§NGS MRDж£АжµЛдЇІеУБSeq-MRD¬ЃзЪДеЕђеПЄгАВSeq-MRD¬ЃйАВзФ®дЇОB/Tз≥їзЩљи°АзЧЕгАБB/Tз≥їжЈЛеЈізШ§гАБе§ЪеПСжАІй™®йЂУзШ§пЉМиГље§ЯеЄЃеК©дЄіеЇКеМїзФЯйҐДжµЛйХњжЬЯзЦЧжХИгАБиѓДдЉ∞ж≤їзЦЧжХИжЮЬгАБзЫСжµЛзЉУиІ£зКґжАБдї•еПКзЫСжµЛжЧ©жЬЯе§НеПСгАВзїПињЗе§ЪеєізЪДзІѓзіѓеТМеПСе±ХпЉМSeq-MRD¬ЃеЬ®дЄіеЇКж£АжµЛеТМзІСе≠¶з†Фз©ґдЄКеЭЗеПЦеЊЧдЄНе∞СжИРжЮЬпЉМеєґиОЈеЊЧеЫљйЩЕеЄВеЬЇиЃ§еПѓгАВ


иЙЊж≤РиТљеИЫеІЛдЇЇеПВдЄОдЇЖдЄ≠еНОеМїе≠¶дЉЪеДњзІСе≠¶еИЖдЉЪи°Ажґ≤е≠¶зїДз≠ЙжЭГе®БжЬЇжЮДиБФеРИеПСеЄГзЪДгАКеДњзЂ•зЩљи°АзЧЕеЊЃе∞ПжЃЛзХЩзЧЕзЫСжµЛдЄОдЄіеЇКеЇФзФ®жМЗеНЧпЉИ2026пЉЙгАЛзЪДжТ∞еЖЩпЉМдЄЇNGS MRDжМЗеѓЉдЄіеЇКж≤їзЦЧзЪДж†ЗеЗЖеМЦдЄОиІДиМГеМЦжПРдЊЫйЗНи¶БжМЗеѓЉжДПиІБгАВ


Seq-MRD¬ЃиОЈеЊЧжђІзЫЯCEиµДиі®пЉИж≥®еЖМеПЈпЉЪDE/CA20/01-IVD-Luxuslebenswelt-190/22пЉЙпЉМиОЈжЙєзЪДжШѓдЇЇжЈЛеЈіBзїЖиГЮеЊЃе∞ПжЃЛзХЩзЧЕеЯЇеЫ†ж£АжµЛиѓХеЙВзЫТпЉИеПѓйАЖжЬЂзЂѓзїИж≠ҐжµЛеЇПж≥ХпЉЙгАВ¬†


иЙЊж≤РиТљжО®еЗЇзЪДSeq-MRD¬Ѓи°Ажґ≤зЩМзЧЗMRDж£АжµЛжШѓжЬАжЧ©жЙєеЃЮзО∞еХЖдЄЪеМЦзЪДдЇІеУБпЉМиЗ™2016еєіз†ФеПСдЄУеИ©жКАжЬѓиЗ≥дїКпЉМиЙЊж≤РиТљSeq-MRD¬ЃеЈ≤зїПиОЈеЊЧ3й°єеЫљеЃґеПСжШОдЄУеИ©пЉЪ
[1]вАЬдЄАзІНеЇФзФ®дЇОйЂШйАЪйЗПжµЛеЇПж£АжµЛTзїЖиГЮзЩљи°АзЧЕеЊЃе∞ПжЃЛзХЩзЧЕзЪДеЉХзЙ©зїДеРИеПКиѓХеЙВзЫТвАЭпЉИдЄУ еИ© еПЈ: 2016 11204857.0пЉМжОИжЭГеЕђеСКеПЈ:CN 106957906 BпЉЙ
[2]вАЬдЄАзІНж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕMRDзЪДиѓХеЙВзЫТвАЭпЉИдЄУ еИ© еПЈ: 2018 1 1550133.0пЉМжОИжЭГеЕђеСКеПЈ: CN 109652518 BпЉЙ
[3]вАЬдЄАзІНж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕMRDзЪДжЦєж≥ХвАЭпЉИдЄУ еИ© еПЈ: 2018 1 1549203.0пЉМжОИжЭГеЕђеСКеПЈ: CN 109680062 BпЉЙ


иЙЊж≤РиТљжЛ•жЬЙиЗ™дЄїз†ФеПСзЪДзФЯдњ°еИЖжЮРеє≥еП∞пЉМиЙЊж≤РиТљSeq-MRD¬Ѓ¬†еЈ≤зїПиОЈеЊЧ3й°єеЫљеЃґиЃ°зЃЧжЬЇиљѓдїґиСЧдљЬпЉЪ
[1]вАЬеЕНзЦЂзїДеЇУMRDж£АжµЛиЗ™еК®еМЦжК•еСКз≥їзїЯ[зЃАзІ∞ImmuReport] V1.0вАЭпЉИзЩїиЃ∞еПЈпЉЪ2019SR0916207пЉЙ
[2]вАЬSeq-MRDж£АжµЛиЗ™еК®еМЦеИЖжЮРз≥їзїЯпЉИDiscTermiteпЉЙ[зЃАзІ∞пЉЪDiscTermite]0.4.6вАЬпЉИзЩїиЃ∞еПЈпЉЪ2019SR1131517пЉЙ
[3]вАЬеЯЇдЇОеЕНзЦЂзїДеЇУдЇМдї£жµЛеЇПзЪДеЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛжХ∞жНЃе§ДзРЖз≥їзїЯвАЭпЉИзЩїиЃ∞еПЈпЉЪ2020SR0507594пЉЙ


1гАБиЙЊж≤РиТљиБФеРИжµЩе§ІйЩДдЄАйїДж≤≥жХЩжОИеЃМжИРзЪДгАКжЦ∞еЮЛCAR-TзїЖиГЮз†ФеПСеПКеЕґж≤їзЦЧжБґжАІи°Ажґ≤зЧЕдЄіеЇКиљђеМЦеИЫжЦ∞дљУз≥їеїЇзЂЛгАЛиОЈ2023еєіеЇ¶жµЩж±ЯзЬБзІСе≠¶жКАжЬѓињЫж≠•е•ЦдЄАз≠Йе•ЦгАВSeq-MRD¬ЃеЬ®иѓ•жКАжЬѓзЪДеИЫжЦ∞дЄОеЇФзФ®дЄ≠иµЈеИ∞дЇЖеЕ≥йФЃжАІдљЬзФ®гАВ

2гАБиЙЊж≤РиТљзФ≥жК•зЪДвАЬеЕНзЦЂзїДTCR/IgйЂШйАЪйЗПжµЛеЇПжКАжЬѓ/и°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛ/Seq-MRD¬ЃвАЭеЫ†еЕґеИЫжЦ∞жАІгАБеЙНж≤њжАІгАБеЄВеЬЇеЃЮзФ®жАІиН£иОЈвАЬ2022еєіеЇ¶CCTBдЄ≠еЫљиВњзШ§ж†ЗењЧзЙ©дЇІдЄЪеИЫжЦ∞е§ІдЉЪеИЫжЦ∞жКАжЬѓ/дЇІеУБиѓДйАЙвАЭй°єзЫЃдЇМз≠Йе•ЦгАВ


2023еєіиОЈжЙєдЇЖгАРеЕ®и°А/й™®йЂУеЯЇеЫ†зїДDNAжПРеПЦиѓХеЙВзЫТгАСпЉИз¶їењГеРЄйЩДжЯ±ж≥ХпЉЙе§Зж°ИзЉЦеПЈпЉЪжµЩжЭ≠жҐ∞е§З20230798 пЉМиѓХеЙВзЫТеИЖеИЂйАВзФ®дЇОдЇЇе§ЦеС®и°АгАБй™®йЂУж†ЈжЬђзЪДж†ЄйЕЄзЪДжПРеПЦгАВ

Seq-MRD¬ЃеПСи°®зЫЄеЕ≥жЦЗзМЃ
1гАБHuang Y, Zhao H, Shao M, Zhou L, Li X, Wei G, Wu W, Cui J, Chang AH, Sun T, Hu Y, Huang H.¬†Predictive value of next-generation sequencing-based minimal residual disease after CAR-T cell therapy. Bone Marrow Transplant.¬†2022 Jun 1. doi: 10.1038/s41409-022-01699-2. Epub ahead of print. PMID: 35650329.пЉИзВєеЗїйУЊжО•еПѓжЯ•зЬЛжЦЗзЂ†еЖЕеЃєпЉЙ

2гАБChen H, Gu M, Liang J, Song H, Zhang J, Xu W, Zhao F, Shen D, Shen H, Liao C, Tang Y, Xu X.¬†Minimal residual disease detection by next-generation sequencing of different immunoglobulin gene rearrangements in pediatric B-ALL.¬†Nat Commun. 2023 Nov 17;14(1):7468. doi: 10.1038/s41467-023-43171-9. пЉИзВєеЗїйУЊжО•еПѓжЯ•зЬЛжЦЗзЂ†еЖЕеЃєпЉЙ

3гАБMin’er Gu,Yahong Xia, Jingying Zhang, Yongmin Tang, Weiqun Xu, Hua Song ¬†Xiaojun Xu.¬†The effectiveness of blinatumomab in clearing measurable residual disease in pediatric B-cell acute lymphoblastic leukemia patients detected by next-generation sequencing.¬† Cancer Med. 2023 Dec;12(24):21978-21984. doi:10.1002/cam4.6771. пЉИзВєеЗїйУЊжО•еПѓжЯ•зЬЛжЦЗзЂ†еЖЕеЃєпЉЙ

4гАБYan N, Wang ZL, Wang XJ, etпЉМal.¬†Measurable residual disease testing by next generation sequencing is more accurate compared with multiparameter flow cytometry in adults with B-cell acute lymphoblastic leukemia.¬†Cancer Lett. 2024 Jul 4;598:217104. doi: 10.1016/j.canlet.2024.217104.

5гАБCHEN HP, MIAO J, FAN LY, et al. Non-specific clones hamper the reliability of Ig light chain gene rearrangements in next-generation sequencing-based measurable residual disease monitoring in pediatric B-cell ALL: A single-center cohort study[J]. Annals of Laboratory Medicine, 2026.


2023еєіDelveInsightеЕђеПЄеПСеЄГзЪДMRDеЫљйЩЕеЄВеЬЇз†Фз©ґжК•еСКдЄ≠пЉМиЙЊж≤РиТљ/Seq-MRD¬ЃжШѓдЄ≠еЫљеФѓдЄАдЄАеЃґеЕђеПЄ/дЇІеУБињЫеЕ•еЫљйЩЕи∞Гз†ФеЄВеЬЇжК•еСКгАВDelveInsightжШѓдЄАеЃґйҐЖеЕИзЪДеМїзЦЧдњЭеБ•еЄВеЬЇз†Фз©ґеТМеХЖдЄЪеҮ胥еЕђеПЄпЉМдї•еЕґзО∞жИРзЪДиБФеРИеЄВеЬЇз†Фз©ґжК•еСКдї•еПКдЄЇеМїзЦЧдњЭеБ•и°МдЄЪзЪДеЕђеПЄжПРдЊЫзЪДеЃЪеИґиІ£еЖ≥жЦєж°ИиАМйЧїеРНгАВ

жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄжИРзЂЛдЇО2016еєіпЉМжШѓеЫљйЩЕеЙНж≤њзЪДдЄУж≥®дЇОеЕНзЦЂй©±еК®еМїе≠¶жКАжЬѓзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪеТМдЄУз≤ЊзЙєжЦ∞дЉБдЄЪгАВеИЫеІЛдЇЇеЫҐйШЯжЭ•иЗ™зЊОеЫљиКЭеК†еУ•е§Іе≠¶пЉМеЬ®2010еєіеЉАеІЛдљњзФ®еЕНзЦЂзїДеЯЇеЫ†йЂШйАЪйЗПжµЛеЇПжКАжЬѓеЉАе±ХеРДзІНзЦЊзЧЕзЫЄеЕ≥з†Фз©ґпЉМдЇО2016еєійАЪињЗиЗ™дЄїз†ФеПСпЉМеЕ®еЫљй¶ЦеЃґжО®еЗЇNGS-MRDи°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛSeq-MRD¬ЃпЉМеєґжОИжЭГж≥ЫзФЯе≠РдљњзФ®гАВеРМжЧґпЉМеЕђеПЄжЛ•жЬЙImmun-Traq¬ЃиВњзШ§ж≤їзЦЧдЉійЪПиѓКжЦ≠гАБImmun-Cheq¬Ѓ¬†еЕНзЦЂеКЫжµЛиѓДдї•еПКImmuHub¬ЃеЕНзЦЂзїДжµЛеЇПзІСз†ФжЬНеК°дЇІеУБпЉМеєґеЄГе±АжЬЙеЯЇдЇОAIжЬЇеЩ®е≠¶дє†зЃЧж≥ХзЪДT-classifier¬ЃиВњзШ§жЧ©з≠ЫгАБеНХзїЖиГЮжµЛеЇПгАБжЦ∞жКЧеОЯгАБTCRеТМжКЧдљУеПСзО∞з≠Йеє≥еП∞зЃ°зЇњгАВзЫЃеЙНдЄЇж≠ҐеПСи°®дЇЖ50дљЩзѓЗиЃЇжЦЗпЉМеЕґдЄ≠еМЕжЛђпЉЪThe New England Journal of Medicine(IF:158.5), The Lancet(IF:98.4), Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24), Nature Communications (IF:17)з≠Йе§ЪзѓЗйЂШеИЖжЭВењЧгАВеЕђеПЄжЮДеїЇеЗ†еНБй°єеПСжШОдЄУеИ©еТМиљѓдїґиСЧдљЬжЭГдЄЇж†ЄењГзЪДиЗ™дЄїзЯ•иѓЖдЇІжЭГдљУз≥їпЉМдЄЇеМїйЩҐдЄіеЇКгАБзФЯеСљзІСе≠¶з†Фз©ґгАБжЦ∞иНѓеЉАеПСз≠ЙжПРдЊЫиІ£еЖ≥жЦєж°ИеТМдЇІеУБгАВиЙЊж≤РиТљдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХгАВ


