
иљЃзКґзЧЕжѓТпЉИRVпЉЙжШѓдЄАзІНеЕ®зРГжАІдЉ†жТ≠зЪДдЇЇзХЬеЕ±жВ£зЧЕзЧЕжѓТпЉМдЄїи¶БеЉХеПС 5 е≤Бдї•дЄЛеДњзЂ•еПКеєЉйЊДеУЇдє≥еК®зЙ©зЪДжА•жАІиГГиВ†зВОеТМиЕєж≥їпЉМеЬ®дЄ≠дљОжФґеЕ•еЫљеЃґж≠їдЇ°зОЗиЊГйЂШпЉМдљЬдЄЇдЄАзІНдЄ•йЗНзЪДдЉ†жЯУзЧЕпЉМз†Фз©ґеЕґеѓєеЕНзЦЂз≥їзїЯзЪДеПНеЇФе∞§дЄЇйЗНи¶БгАВ
ињСжЧ•еРЙжЮЧеЖЬдЄЪе§Іе≠¶еЕљеМїеМїе≠¶йЩҐзЪДдЄУеЃґеЫҐйШЯеЬ®Veterinary MicrobiologyжЭВењЧеПСи°®йҐШдЄЇвАЬRotavirus induces mucosal B-cell responses through the TLR3/TRIF and MAVS pathwaysвАЭзЪДжЦЗзЂ†пЉМжП≠з§ЇдЇЖиљЃзКґзЧЕжѓТйАЪињЗTLR3/TRIFеТМRIG-I/MAVSдњ°еПЈйАЪиЈѓиѓ±еѓЉBзїЖиГЮеЕНзЦЂеЇФз≠ФзЪДеИЖе≠РжЬЇеИґгАВиѓ•з†Фз©ґйЗЗзФ®дЇЖиЙЊж≤РиТљзЪДImmuHub¬Ѓ¬†TCRжµЛеЇПеИЖжЮРжКАжЬѓеє≥еП∞пЉМжП≠з§ЇдЇЖTRIFйАЪиЈѓдЉЪељ±еУНCD4+TзїЖиГЮеѓєBзїЖиГЮзЪДиЊЕеК©еКЯиГљпЉМдїОиАМи∞ГиКВBзїЖиГЮеЕНзЦЂгАВиѓ•з†Фз©ґзїУжЮЬдЄЇеЉАеПСеєњи∞±гАБйХњжХИзЪДRVзЦЂиЛЧжПРдЊЫдЇЖзРЖиЃЇдЊЭжНЃгАВ

иѓ•з†Фз©ґдї•C57BL/6JиГМжЩѓзЪДйЗОзФЯеЮЛпЉИWTпЉЙгАБTLR3вБї/вБїгАБTRIFвБї/
вБїгАБMAVSвБї/вБїеПКTLR3вБї/вБїMAVSвБї/вБїеПМжХ≤йЩ§е∞ПйЉ†дЄЇз†Фз©ґеѓєи±°пЉМйЗЗзФ®RVзЧЕжѓТжДЯжЯУзЪДйЫМжАІе∞ПйЉ†пЉМжДЯжЯУеРО10姩жФґйЫЖиДЊиДПгАБиВ†з≥їиЖЬжЈЛеЈізїУпЉИMLNsпЉЙгАБжіЊе∞ФйЫЖеРИжЈЛеЈізїУпЉИPPsпЉЙз≠Йж†ЈжЬђгАВ
йАЪињЗTCRќ≤йУЊйЂШйАЪйЗПжµЛеЇПеИЖжЮРCD4+TзїЖиГЮеПЧдљУзЪДеЕЛйЪЖе§Ъж†ЈжАІеПКV/JеЯЇеЫ†дљњзФ®йҐСзОЗпЉЫйЗЗзФ®жµБеЉПзїЖиГЮжЬѓж£АжµЛдЄНеРМз±їеЮЛBзїЖиГЮжѓФдЊЛпЉЫйАЪињЗElisaеЃЪйЗПи°АжЄЕжКЧдљУж∞іеє≥пЉЫеЕНзЦЂиНІеЕЙиІВеѓЯе∞ПиВ†CD138+IgA+зїЖиГЮеИЖеЄГпЉЫйАЪињЗй™®йЂУзІїж§НеЃЮй™Мй™МиѓБTRIFйАЪиЈѓзЪДзїЖиГЮеЖЕеЬ®дљЬзФ®гАВ

еѓєRVжДЯжЯУеРОзЪДе∞ПйЉ†CD4+TзїЖиГЮињЫи°МTCRжµЛеЇПгАВиЬЧзЙЫеЫЊжШЊз§ЇпЉМдЄОWTе∞ПйЉ†зЫЄжѓФпЉМTRIFвБї/вБїе∞ПйЉ†зЪДвАЬ1вАЭзОѓе±ВжѓФдЊЛпЉИеНХеЕЛйЪЖTзїЖиГЮжѓФдЊЛпЉЙеЗПе∞СпЉМи°®жШОTRIFжХ≤йЩ§еРОзЪДCD4+TзїЖиГЮеПСзФЯеПШеМЦпЉИиІБеЫЊ1AпЉЙгАВCDR3ж∞®еЯЇйЕЄйХњеЇ¶еИЖеЄГе¶ВеЫЊ1BжЙАз§ЇпЉМдЄїи¶БйЫЖдЄ≠еЬ®10-18дЄ™AAдєЛйЧігАВTRIFвБї/вБїе∞ПйЉ†¬†CD4+TзїЖиГЮзЪДCDR3еЕЛйЪЖйҐСзОЗжШЊиСЧжФєеПШпЉИеЫЊ1CпЉЙпЉМTRBV13-2гАБTRBJ1-2 з≠ЙV/JеЯЇеЫ†зЙЗжЃµзЪДдљњзФ®йҐСзОЗйЩНдљОпЉИеЫЊ1D-FпЉЙгАВ
еРМжЧґпЉМеЬ®RVжДЯжЯУеРОжµЛеЃЪдЇЖWTеТМTRIFвБї/вБїе∞ПйЉ†PPsеТМиДЊиДПдЄ≠жї§ж≥°иЊЕеК©жАІTзїЖиГЮпЉИTfhзїЖиГЮпЉМBзїЖиГЮжњАжіїзЪДеЕ≥йФЃиЊЕеК©зїЖиГЮпЉЙзЪДйҐСзОЗгАВPPsдЄ≠TfhзїЖиГЮжѓФдЊЛжШЊиСЧдљОдЇОWTе∞ПйЉ†пЉИеЫЊ1E-FпЉЙгАВдї•дЄКзїУжЮЬжПРз§ЇTRIFйАЪ裃犯姱дЉЪељ±еУНCD4+TзїЖиГЮеѓєBзїЖиГЮзЪДиЊЕеК©еКЯиГљгАВ
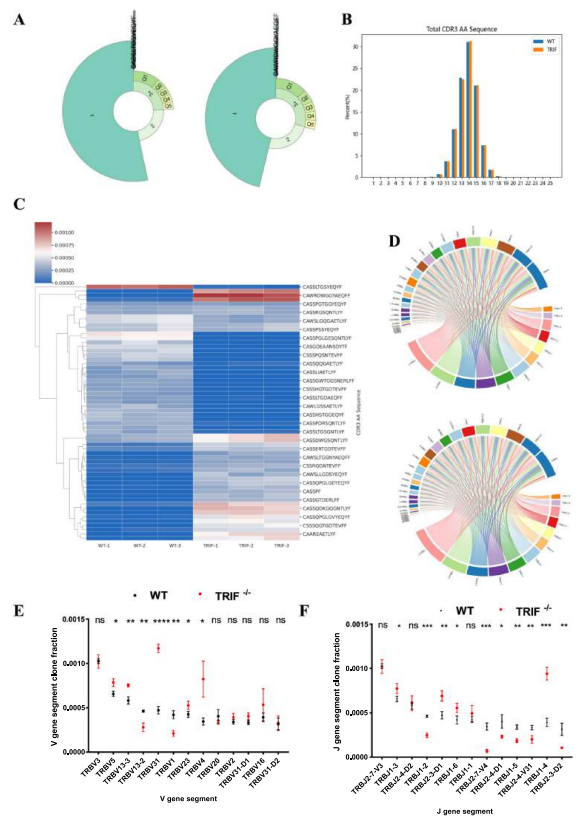
еЫЊ1

RVжДЯжЯУеРОпЉМTLR3вБї/вБїеТМTRIFвБї/вБїе∞ПйЉ†зЪДиДЊиДПгАБMLNsгАБPPsдЄ≠пЉМзФЯеПСдЄ≠ењГпЉИGCпЉЙжњАжіїеЮЛBзїЖиГЮжѓФдЊЛжШЊиСЧдЄЛйЩНпЉИеЫЊ2пЉЙпЉЫи°АжЄЕдЄ≠жАїIgAгАБIgG1гАБIgG2aпЉИTRIFвБї/вБїпЉЙеПК IgGгАБIgG1пЉИTLR3вБї/вБїпЉЙжКЧдљУж∞іеє≥жШЊиСЧйЩНдљОпЉМе∞ПиВ†еНБдЇМжМЗиВ†гАБз©ЇиВ†гАБеЫЮиВ†зЪДCD138+IgA+жµЖзїЖиГЮжХ∞йЗПеЗПе∞СпЉИеЫЊ3пЉЙгАВи°®жШОTLR3/TRIFйАЪиЈѓжШѓBзїЖиГЮеИЖеМЦдЄЇжµЖзїЖиГЮеєґеИЖж≥МжКЧдљУзЪДеЕ≥йФЃпЉМиѓ•йАЪиЈѓзЪД犯姱дЉЪеЙКеЉ±BзїЖиГЮеИЖж≥МжКЧдљУзЪДиГљеКЫгАВ
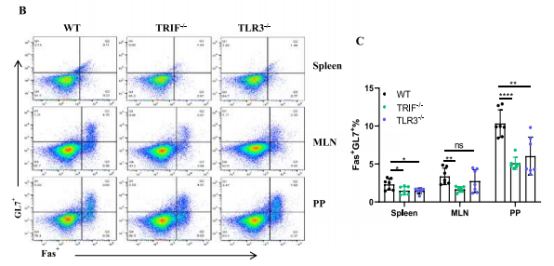
еЫЊ2
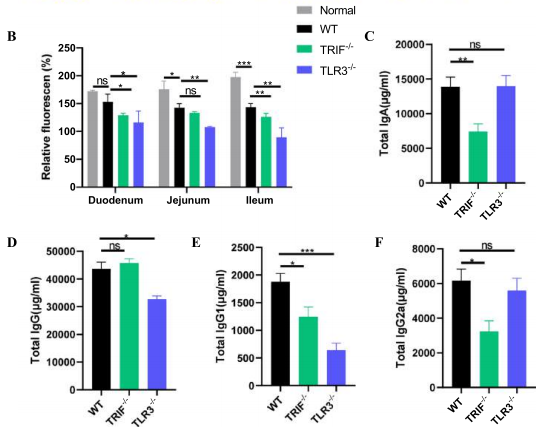
еЫЊ3

й™®йЂУзІїж§НеЃЮй™МжШЊз§ЇпЉМжО•еПЧTRIFвБї/вБїдЊЫдљУй™®йЂУзЪДеПЧдљУе∞ПйЉ†пЉМжДЯжЯУRVеРО MLNsдЄ≠GC BзїЖиГЮзЪДзїЭеѓєжХ∞йЗПжШЊиСЧдљОдЇОWTдЊЫдљУзїДпЉИеЫЊ4пЉЙпЉМиЩљйҐСзОЗжЧ†еЈЃеЉВпЉМдљЖиѓБеЃЮTRIFйАЪиЈѓеѓєдЇОRVзЙєеЉВжАІBзїЖиГЮзЪДзІѓзіѓиЗ≥еЕ≥йЗНи¶БгАВ
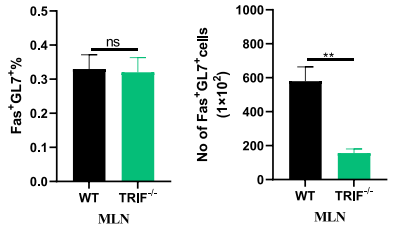
еЫЊ4

MAVSвБї/вБїе∞ПйЉ†жДЯжЯУеРОпЉМMLNsеТМPPsдЄ≠GCжњАжіїеЮЛBзїЖиГЮжѓФдЊЛгАБPPs дЄ≠B220вБЇIgAвБЇзїЖиГЮжѓФдЊЛпЉМдї•еПКиДЊиДПгАБMLNsдЄ≠CD138вБЇIgAвБЇжµЖзїЖиГЮжѓФдЊЛеЭЗжШЊиСЧйЩНдљОпЉИеЫЊ5пЉЙпЉМжПРз§ЇMAVSйАЪиЈѓдЄОTLR3/TRIFйАЪиЈѓз±їдЉЉпЉМжШѓBзїЖиГЮеЕНзЦЂжњАжіїзЪДйЗНи¶Би∞ГжОІеЫ†е≠РгАВ
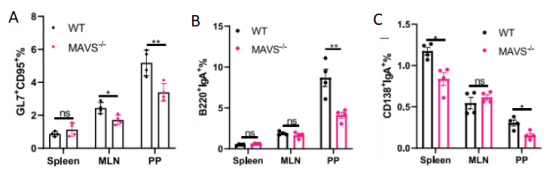
еЫЊ5

TLR3вБї/вБїMAVSвБї/вБїеПМжХ≤йЩ§е∞ПйЉ†зЪДPPsдЄ≠GC BзїЖиГЮгАБB220вБЇIgAвБЇгАБB220вБЇIgG2aвБЇзїЖиГЮжѓФдЊЛгАБи°АжЄЕIgG1ж∞іеє≥гАБдї•еПКе∞ПиВ†еРДжЃµ CD138вБЇIgAвБЇзїЖиГЮжХ∞йЗПеЭЗињЫдЄАж≠•дЄЛйЩНпЉЫдЄФиДЊиДПеТМPPsдЄ≠Ki67вБЇеҐЮжЃЦеЮЛBзїЖиГЮжѓФдЊЛжШЊиСЧдљОдЇОWTе∞ПйЉ†пЉИеЫЊ6пЉЙгАВиѓБеЃЮдЄ§жЭ°йАЪиЈѓеНПеРМи∞ГжОІBзїЖиГЮеҐЮжЃЦиГљеКЫпЉМеŴ犯姱дЉЪеѓЉиЗі B зїЖиГЮеЕНзЦЂеКЯиГљзЪДеП†еК†жНЯдЉ§гАВ
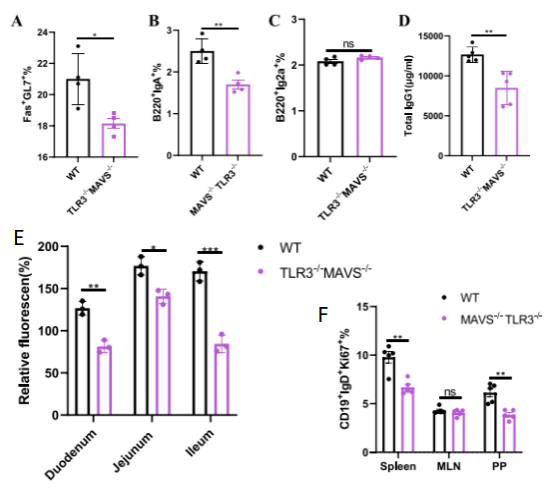
еЫЊ6
жЬђз†Фз©ґиѓБеЃЮдЇЖиљЃзКґзЧЕжѓТйАЪињЗTLR3/TRIFеТМMAVSдЄ§жЭ°дњ°еПЈйАЪиЈѓеНПеРМи∞ГжОІBзїЖиГЮдїЛеѓЉзЪДдљУжґ≤еЕНзЦЂпЉЪдЄАжЦєйЭҐйАЪињЗељ±еУНCD4+TзїЖиГЮзЪДV/JеЯЇеЫ†йЗНжОТеТМTfhзїЖиГЮеКЯиГљпЉМдЄЇBзїЖиГЮжПРдЊЫеЕЕиґ≥иЊЕеК©дњ°еПЈпЉЫеП¶дЄАжЦєйЭҐзЫіжО•и∞ГжОІGC BзїЖиГЮзЪДжњАжіїгАБжµЖзїЖиГЮеИЖеМЦеПКжКЧдљУеИЖж≥МпЉМеРМжЧґзїіжМБBзїЖиГЮзЪДеҐЮжЃЦиГљеКЫпЉМжЬАзїИеПВдЄОзЧЕжѓТжЄЕйЩ§еТМжКЧжДЯжЯУеЕНзЦЂгАВиѓ•з†Фз©ґдЄЇиЃЊиЃ°йЭґеРСињЩдЄ§жЭ°йАЪиЈѓзЪДеЕНзЦЂдљРеЙВжИЦжЦ∞еЮЛRVзЦЂиЛЧжПРдЊЫдЇЖзРЖиЃЇйЭґзВєгАВ
жЦЗзМЃжЭ•жЇР
Rong-Rong Zhang,et,al.Rotavirus induces mucosal B-cell responses through the TLR3/TRIF and MAVS pathways. Veterinary Microbiology,Volume 314,2026,110910,ISSN 0378-1135.
иЙЊж≤РиТљдЄУж≥®дЇОеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯе§ЪеєіпЉМеЉАеПСзЪДImmuHub¬ЃжКАжЬѓеє≥еП∞жЦєж≥ХеЕ®йЭҐпЉМж£АжµЛзЙ©зІНе§Ъж†ЈпЉМеїЇеЇУжЦєж≥ХеЕЈжЬЙзБµжіїжАІпЉМиЗіеКЫдЇОдЄЇеРДе§ІйЂШж†°гАБеМїйЩҐгАБзІСз†ФжЬЇжЮДгАБдЉБдЄЪз≠ЙжПРдЊЫдЉШиЙѓзЪДзІСз†ФжЬНеК°гАВ

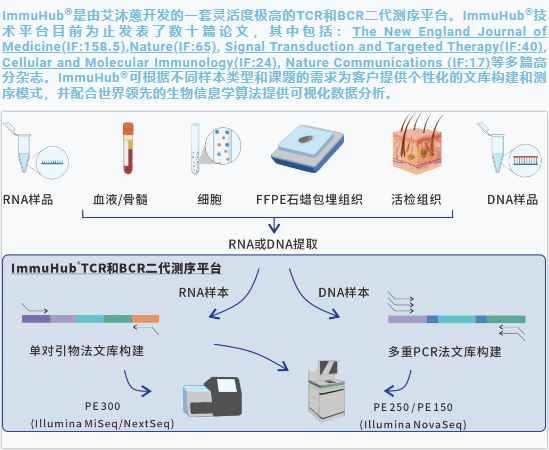
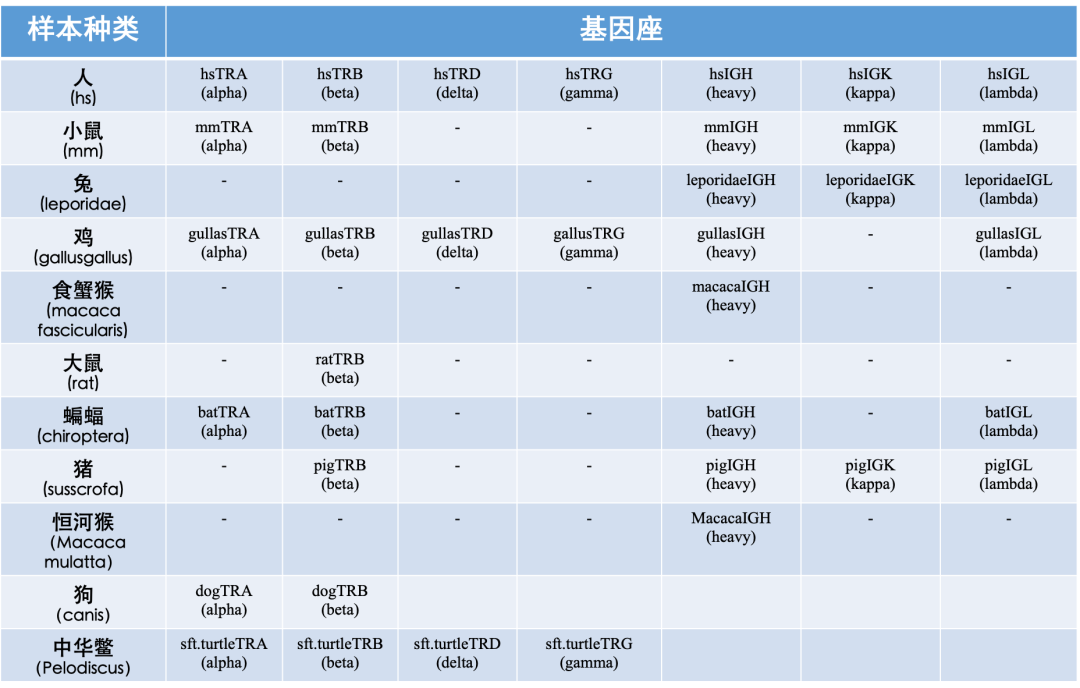
ImmuHub¬ЃйГ®еИЖзІСз†ФжЦєеРС

ImmuHub¬ЃйАВзФ®еЯЇеЫ†еЇІ
йГ®еИЖжХ∞жНЃеИЖжЮРзїУжЮЬе±Хз§Ї
жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄжИРзЂЛдЇО2016еєіпЉМжШѓеЫљйЩЕеЙНж≤њзЪДдЄУж≥®дЇОеЕНзЦЂй©±еК®еМїе≠¶жКАжЬѓзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪеТМдЄУз≤ЊзЙєжЦ∞дЉБдЄЪгАВеИЫеІЛдЇЇеЫҐйШЯжЭ•иЗ™зЊОеЫљиКЭеК†еУ•е§Іе≠¶пЉМеЬ®2010еєіеЉАеІЛдљњзФ®еЕНзЦЂзїДеЯЇеЫ†йЂШйАЪйЗПжµЛеЇПжКАжЬѓеЉАе±ХеРДзІНзЦЊзЧЕзЫЄеЕ≥з†Фз©ґпЉМдЇО2016еєійАЪињЗиЗ™дЄїз†ФеПСпЉМеЕ®еЫљй¶ЦеЃґжО®еЗЇNGS-MRDи°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛSeq-MRD¬ЃпЉМеєґжОИжЭГж≥ЫзФЯе≠РдљњзФ®гАВеРМжЧґпЉМеЕђеПЄжЛ•жЬЙImmun-Traq¬ЃиВњзШ§ж≤їзЦЧдЉійЪПиѓКжЦ≠гАБImmun-Cheq¬Ѓ¬†еЕНзЦЂеКЫжµЛиѓДдї•еПКImmuHub¬ЃеЕНзЦЂзїДжµЛеЇПзІСз†ФжЬНеК°дЇІеУБпЉМеєґеЄГе±АжЬЙеЯЇдЇОAIжЬЇеЩ®е≠¶дє†зЃЧж≥ХзЪДT-classifier¬ЃиВњзШ§жЧ©з≠ЫгАБеНХзїЖиГЮжµЛеЇПгАБжЦ∞жКЧеОЯгАБTCRеТМжКЧдљУеПСзО∞з≠Йеє≥еП∞зЃ°зЇњгАВзЫЃеЙНдЄЇж≠ҐеПСи°®дЇЖ50дљЩзѓЗиЃЇжЦЗпЉМеЕґдЄ≠еМЕжЛђпЉЪThe New England Journal of Medicine(IF:158.5), The Lancet(IF:98.4), Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24),¬†Nature Communications¬†(IF:17)з≠Йе§ЪзѓЗйЂШеИЖжЭВењЧгАВеЕђеПЄжЮДеїЇеЗ†еНБй°єеПСжШОдЄУеИ©еТМиљѓдїґиСЧдљЬжЭГдЄЇж†ЄењГзЪДиЗ™дЄїзЯ•иѓЖдЇІжЭГдљУз≥їпЉМдЄЇеМїйЩҐдЄіеЇКгАБзФЯеСљзІСе≠¶з†Фз©ґгАБжЦ∞иНѓеЉАеПСз≠ЙжПРдЊЫиІ£еЖ≥жЦєж°ИеТМдЇІеУБгАВиЙЊж≤РиТљдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХгАВ


