еЉ•жЉЂе§ІBзїЖиГЮжЈЛеЈізШ§пЉИDLBCLпЉЙжШѓжЬАеЄЄиІБзЪДйЭЮйЬНе•ЗйЗСжЈЛеЈізШ§дЇЪеЮЛгАВиЩљзДґRвАСCHOPжЦєж°ИиГљдљњиґЕињЗ60%зЪДжВ£иАЕиОЈеЊЧйХњжЬЯзЉУиІ£пЉМдљЖдїНжЬЙзЇ¶1/3зЪДжВ£иАЕйЭҐдЄіе§НеПСжИЦйЪЊж≤їгАВе¶ВдљХеЬ®жЦ∞иѓКжЦ≠жЧґе∞±иГљеЗЖз°ЃиѓЖеИЂйЂШеН±дЇЇзЊ§гАБжМЗеѓЉдЄ™дљУеМЦж≤їзЦЧпЉМдЄАзЫіжШѓдЄіеЇКдЄКзЪДйЪЊзВєгАВдЉ†зїЯзїДзїЗжіїж£АиЩљзДґиГљжПРдЊЫиВњзШ§зЪДеЯЇеЫ†дњ°жБѓпЉМдљЖе≠ШеЬ®жЬЙеИЫгАБеПЦж†ЈеЫ∞йЪЊгАБйЪЊдї•еК®жАБзЫСжµЛз≠Йе±АйЩРгАВжґ≤дљУжіїж£АвАФвАФйАЪињЗж£АжµЛи°АжµЖдЄ≠зЪДеЊ™зОѓиВњзШ§DNAпЉИctDNAпЉЙвАФвАФж≠£еЬ®жФєеПШињЩдЄАе±АйЭҐгАВ
ињСжЬЯпЉМдЄАй°єеПСи°®дЇО гАКBlood AdvanceгАЛ зЪДеЙНзЮїжАІз†Фз©ґдЄЇжИСдїђеЄ¶жЭ•дЇЖжЦ∞жАЭиЈѓпЉЪctDNAдЄНдїЕиГљиѓДдЉ∞иВњзШ§иіЯиНЈпЉМињШиГљеПѓйЭ†еЬ∞ињЫи°МеИЖе≠РеИЖеЮЛпЉМе∞ЖдЄ§иАЕзїУеРИеПѓжШЊиСЧжПРйЂШDLBCLжВ£иАЕзЪДйҐДеРОйҐДжµЛиГљеКЫгАВ


DLBCLеЕЈжЬЙйЂШеЇ¶еЉВиі®жАІпЉМињСеєіжЭ•зЪДеЯЇеЫ†зїДе≠¶з†Фз©ґеЈ≤е∞ЖеЕґеИТеИЖдЄЇе§ЪдЄ™еЕЈжЬЙдЄНеРМеЯЇеЫ†з™БеПШеТМдЄіеЇКйҐДеРОзЪДеИЖе≠РдЇЪеЮЛпЉМе¶ВMCDгАБEZBгАБBN2гАБST2гАБA53з≠ЙгАВињЩдЇЫеИЖеЮЛдЉ†зїЯдЄКдЊЭиµЦзїДзїЗжіїж£АпЉМдљЖзїДзїЗжіїж£Ае≠ШеЬ®дї•дЄЛйЧЃйҐШпЉЪ
-
жЬЙеИЫжУНдљЬпЉМйГ®еИЖжВ£иАЕеПЦж†ЈеЫ∞йЪЊ
-
жЧ†ж≥ХеПНжШ†иВњзШ§жЧґз©ЇеЉВиі®жАІ
-
йЪЊдї•зФ®дЇОеК®жАБзЫСжµЛ
ctDNAдљЬдЄЇжґ≤дљУжіїж£АзЪДдї£и°®пЉМеЈ≤襀иѓБеЃЮеПѓзФ®дЇОиѓДдЉ∞иВњзШ§иіЯиНЈгАБзЫСжµЛеЊЃе∞ПжЃЛзХЩзЧЕгАВдљЖжШѓпЉМctDNAиГљеР¶еЗЖз°ЃйЗНзО∞зїДзїЗжіїж£АдЄ≠зЪДеИЖе≠РеИЖеЮЛпЉЯctDNAж∞іеє≥дЄОеИЖе≠РеИЖеЮЛиГљеР¶еНПеРМжПРйЂШйҐДеРОйҐДжµЛпЉЯ ињЩж≠£жШѓжЬђз†Фз©ґиѓХеЫЊеЫЮз≠ФзЪДйЧЃйҐШгАВ

-
166дЊЛеИЭж≤їгАБжЬ™зїПж≤їзЦЧзЪДDLBCLпЉИйЭЮзЙєжМЗеЮЛпЉЙжВ£иАЕ
-
еЭЗжО•еПЧRвАСCHOPжЦєж°ИпЉИеȩ嶕жШФеНХжКЧ+зОѓз£ЈйЕ∞иГЇ+е§ЪжЯФжѓФжШЯ+йХњжШ•жЦ∞祱+ж≥Ље∞ЉжЭЊпЉЙж≤їзЦЧ
-
дЄ≠дљНйЪПиЃњ49.1дЄ™жЬИ
-
еЙНзЮїжАІгАБе§ЪдЄ≠ењГгАБзЬЯеЃЮдЄЦзХМйШЯеИЧ
-
ж£АжµЛжКАжЬѓпЉЪCAPPвАСseqпЉИзЩМзЧЗдЄ™дљУеМЦжЈ±еЇ¶жµЛеЇПпЉЙпЉМйЭґеРС109дЄ™жЈЛеЈізШ§зЫЄеЕ≥еЯЇеЫ†пЉИеМЕжЛђзВєз™БеПШеТМжЛЈиіЭжХ∞еПШеЉВпЉЙ
-
ctDNAеЃЪйЗПпЉЪдї•logвВБвВА hGE/mLпЉИеНХеАНдљУеЯЇеЫ†зїДељУйЗП/жѓЂеНЗи°АжµЖпЉЙи°®з§ЇпЉМйЗЗзФ®жЧҐеЊАй™МиѓБзЪД2.5 logвВБвВА hGE/mLдљЬдЄЇйЂШдљОиіЯиНЈйШИеАЉ
-
еИЖе≠РеИЖеЮЛеЈ•еЕЈпЉЪLymphGenпЉИеЯЇдЇОеЯЇеЫ†з™БеПШеТМжЛЈиіЭжХ∞еПШеЉВе∞ЖDLBCLеИЖдЄЇMCDгАБEZBгАБBN2гАБST2гАБA53з≠Йз∞ЗпЉЙ
-
й™МиѓБйЫЖпЉЪ77дЊЛеРМжЧґжЬЙзїДзїЗжіїж£АеТМctDNAзЪДжВ£иАЕпЉМзФ®дЇОиѓДдЉ∞дЄ§зІНжЭ•жЇРеИЖеЮЛзЪДдЄАиЗіжАІ
-
зФЯе≠ШеИЖжЮРпЉЪKaplanвАСMeierж≥Х + logвАСrankж£Ай™М
-
йАТељТеИЖеЙ≤ж≥ХпЉЪжΥ糥ctDNAж∞іеє≥дЄОеИЖе≠Рз∞ЗзЪДжЬАдљ≥зїДеРИ
-
е§ЪеПШйЗПCoxеЫЮељТпЉЪиѓДдЉ∞зЛђзЂЛйҐДеРОеЫ†зі†
-
CзїЯиЃ°йЗПпЉЪжѓФиЊГж®°еЮЛйҐДжµЛжАІиГљ

еЬ®77дЊЛеРМжЧґжЬЙзїДзїЗеТМctDNAж†ЈжЬђзЪДжВ£иАЕдЄ≠пЉЪ
-
зїДзїЗеТМctDNAеЭЗеПѓеИЖеЮЛзЪД24дЊЛжВ£иАЕдЄ≠пЉМеИЖеЮЛдЄАиЗізОЗйЂШиЊЊ95.8%пЉИfig.2пЉЙ
-
еЯЇдЇОctDNAжИЦзїДзїЗеИЖеЮЛжВ£иАЕзЪДдЄіеЇКзїУе±АжЧ†жШЊиСЧеЈЃеЉВ
и°®жШОпЉЪctDNAеЃМеЕ®еПѓдї•дљЬдЄЇзїДзїЗжіїж£АзЪДжЧ†еИЫжЫњдї£пЉМзФ®дЇОDLBCLеИЖе≠РеИЖеЮЛгАВ
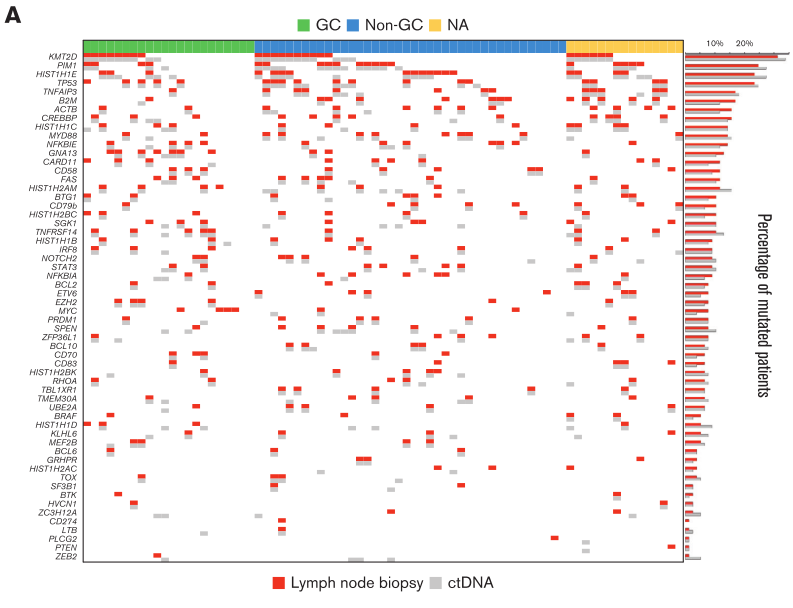
fig. 1 77дЊЛжВ£иАЕеЯЇдЇОзїДзїЗеТМctDNAзЪДеЯЇеЫ†з™БеПШи∞±зГ≠еЫЊ
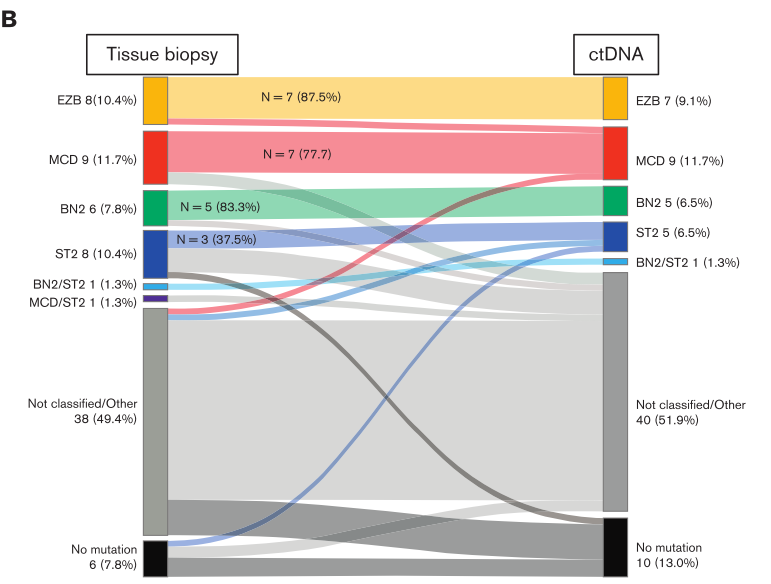
fig. 2 зїДзїЗжіїж£АдЄОctDNAеИЖе≠Рз∞ЗеИЖйЕНзЪДдЄАиЗіжАІеѓєжѓФ
-
дљОctDNAзїДпЉИ71.7%пЉМ4еєіOS¬†85.7%
-
йЂШctDNAзїДпЉИвЙ•2.5 logвВБвВА hGE/mLпЉМ67дЊЛпЉЙпЉЪ4еєіPFS¬†50.3%пЉМ4еєіOS¬†61.0%
-
еЈЃеЉВеЕЈжЬЙзїЯиЃ°е≠¶жДПдєЙпЉИPFS: P=0.0018пЉЫOS: P=0.0017пЉЙ
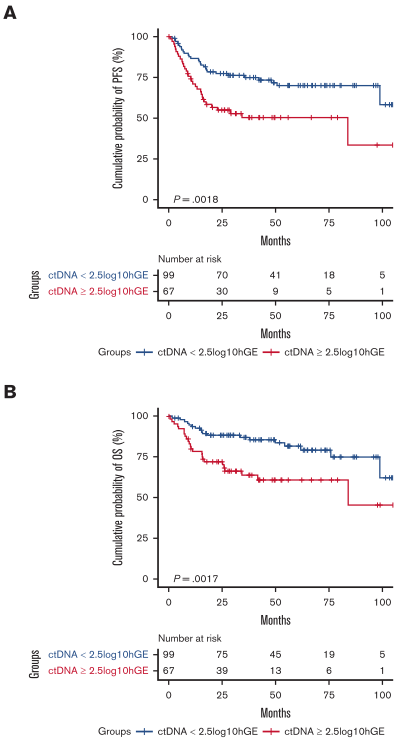
fig. 3 еЯЇдЇОctDNAж∞іеє≥зЪДPFSдЄОOS KaplanвАСMeierжЫ≤зЇњ
йАЪињЗйАТељТеИЖеЙ≤еИЖжЮРпЉИfig.¬†4пЉЙеПСзО∞пЉЪ
-
дљОctDNAзїДдЄНеЖН襀еИЖе≠Рз∞ЗињЫдЄАж≠•еИЖе±В
-
йЂШctDNAзїДдЄ≠пЉМ襀ељТдЄЇST2жИЦBN2з∞ЗзЪДжВ£иАЕйҐДеРОжШЊиСЧжЫіе•љпЉЪ
-
-
ST2/BN2жВ£иАЕпЉИ16дЊЛпЉЙпЉЪ4еєіPFS¬†87.5%пЉМ4еєіOS¬†100%
-
йЭЮST2/BN2жВ£иАЕпЉИ51дЊЛпЉЙпЉЪ4еєіPFS¬†38.0%пЉМ4еєіOS¬†47.1%
-
PFS: P=0.003пЉЫOS: P=0.001
зїУжЮЬи°®жШОпЉЪйЂШиВњзШ§иіЯиНЈвЙ†йҐДеРОеЈЃвАФвАФйЂШctDNAдљЖе±ЮдЇОST2/BN2дЇЪеЮЛзЪДжВ£иАЕпЉМеѓєRвАСCHOPеПНеЇФжЮБдљ≥гАВ
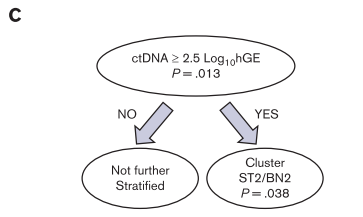
fig. 4 йАТељТеИЖеЙ≤жµБз®ЛеЫЊ
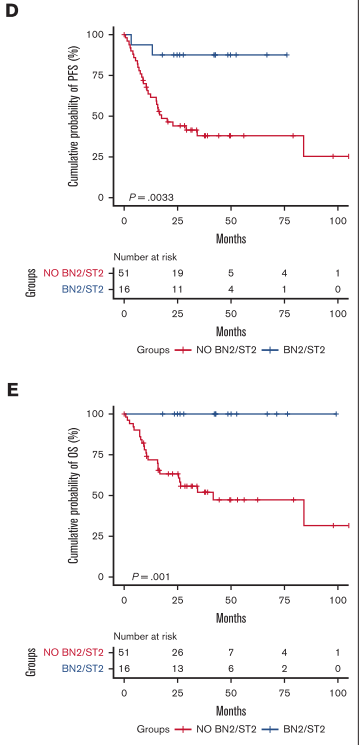
fig. 5 йЂШctDNAзїДдЄ≠ж†єжНЃжШѓеР¶ST2/BN2зЪДPFSдЄОOSжЫ≤зЇњ
з†Фз©ґе∞ЖжВ£иАЕеИЖдЄЇдЄ§зїДпЉЪ
-
дљОй£ОйЩ©зїДпЉИ51дЊЛпЉЙпЉЪctDNAжИЦе±ЮдЇОST2/BN2з∞З
вЖТ 4еєіPFS¬†75.3%пЉМ4еєіOS87.8% -
йЂШй£ОйЩ©зїДпЉИ115дЊЛпЉЙпЉЪctDNAвЙ•2.5дЄФдЄНе±ЮдЇОST2/BN2з∞З
вЖТ 4еєіPFS¬†38.0%пЉМ4еєіOS¬†47.1%
дЄОдїЕдљњзФ®ctDNAж∞іеє≥зЫЄжѓФпЉМеК†еЕ•ST2/BN2еИЖеЮЛеРОпЉЪ
-
PFSзЪДCзїЯиЃ°йЗПпЉЪ0.599 вЖТ¬†0.635
-
OSзЪДCзїЯиЃ°йЗПпЉЪ0.631 вЖТ¬†0.687
е§ЪеПШйЗПеИЖжЮРпЉИж†°ж≠£IPIиѓДеИЖгАБзїЖиГЮиµЈжЇРеРОпЉЙжШЊз§ЇпЉЪ
-
е±ЮдЇОST2/BN2дЄОжЫіе•љзЪДPFSпЉИHR=0.24пЉМP=0.02пЉЙеТМOSпЉИHR=0.07пЉМP=0.011пЉЙзЛђзЂЛзЫЄеЕ≥
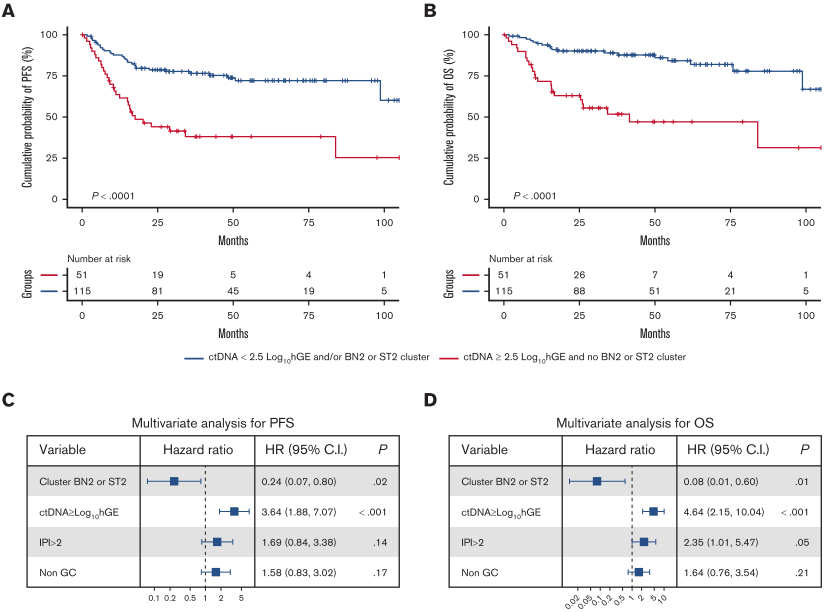
fig.6 ctDNAж∞іеє≥еТМST2/BN2еИЖе≠Рз∞ЗеѓєйҐДеРОзЪДељ±еУН

1. ctDNAеПѓеЗЖз°ЃйЗНзО∞DLBCLеИЖе≠РеИЖеЮЛпЉЪдЄОзїДзїЗжіїж£АдЄАиЗізОЗйЂШиЊЊ95.8%пЉМеПѓдљЬдЄЇжЧ†еИЫжЫњдї£еЈ•еЕЈгАВ
2. ctDNAж∞іеє≥жШѓзЛђзЂЛйҐДеРОжМЗж†ЗпЉЪ2.5 logвВБвВА hGE/mLйШИеАЉеПѓжЬЙжХИеМЇеИЖйЂШдљОй£ОйЩ©жВ£иАЕгАВ
3. еИЖе≠РеИЖеЮЛеЬ®йЂШctDNAжВ£иАЕдЄ≠еЕЈжЬЙвАЬиІ£жѓТвАЭдљЬзФ®пЉЪеН≥дљњиВњзШ§иіЯиНЈйЂШпЉМST2/BN2дЇЪеЮЛжВ£иАЕдїНеѓєRвАСCHOPеПНеЇФиЙѓе•љгАВ
4. иБФеРИctDNAж∞іеє≥еТМST2/BN2еИЖеЮЛжШЊиСЧжПРеНЗйҐДжµЛеЗЖз°ЃжАІпЉЪдЄЇдЄіеЇКжПРдЊЫжЫіз≤ЊеЗЖзЪДй£ОйЩ©еИЖе±ВеЈ•еЕЈгАВ
еѓєдЇОдљОй£ОйЩ©жВ£иАЕпЉИctDNAдљОжИЦдЄЇST2/BN2пЉЙиАМи®АпЉМеПѓеЃЙењГжО•еПЧж†ЗеЗЖRвАСCHOPж≤їзЦЧпЉМйБњеЕНињЗеЇ¶ж≤їзЦЧгАВ
еѓєдЇОйЂШй£ОйЩ©жВ£иАЕпЉИctDNAйЂШдЄФйЭЮST2/BN2пЉЙиАМи®АпЉМеЇФзЇ≥еЕ•жЫіеѓЖеИЗзЪДзЫСжµЛжИЦжΥ糥жЦ∞еЮЛиБФеРИж≤їзЦЧз≠ЦзХ•пЉИе¶ВйЭґеРСиНѓзЙ©гАБCARвАСTз≠ЙпЉЙгАВ
жґ≤дљУжіїж£АвАЬдЄАзЃ°и°АвАЭеН≥еПѓеРМжЧґиОЈеЊЧиВњзШ§иіЯиНЈеТМеИЖе≠РдЇЪеЮЛдњ°жБѓпЉМдЊњжНЈдЄФеПѓйЗНе§НпЉМйАВеРИеК®жАБзЫСжµЛгАВ
жЬ™жЭ•пЉМеПѓе∞ЖctDNAеИЖе≠РеИЖеЮЛдЄОељ±еГПзїДе≠¶пЉИPET/CTпЉЙгАБзЙЗжЃµзїДе≠¶з≠ЙжЫіе§Ъжґ≤дљУжіїж£АзїіеЇ¶зїУеРИпЉМжЮДеїЇжЫіеЉЇе§ІзЪДйҐДжµЛж®°еЮЛпЉМеЬ®ж≤їзЦЧињЗз®ЛдЄ≠еК®жАБзЫСжµЛctDNAеИЖе≠РжЉФеПШпЉМеПКжЧґеПСзО∞иАРиНѓеЕЛйЪЖгАВ
Moia R, et al. Molecular clustering on ctDNA improves the prognostic stratification of patients with DLBCL compared with ctDNA levels alone. Blood Adv 2025 9 (7). DOI: 10.1182/blood.2024024456
иЙЊж≤РиТљзФЯзЙ©зІСжКАиЗ™дЄїз†ФеПСз†ФеПСзЪДSeq-LMPж£АжµЛдљУз≥їпЉМињРзФ®йЭґеРСжНХиОЈиБФеРИдЇМдї£жµЛеЇПжКАжЬѓпЉМдїЕйЬАдЄАжђ°жКљи°АеН≥еПѓеИЖжЮРDLBCLжВ£иАЕи°Ажґ≤дЄ≠йЗКжФЊзЪДиВњзШ§жЭ•жЇРDNAпЉМжґµзЫЦдЄ§зЩЊе§ЪзІНBзїЖиГЮжЈЛеЈізШ§еЕ≥йФЃеЯЇеЫ†зЪДзЉЦз†БеМЇпЉМиГље§Яз≤ЊеЗЖиѓЖеИЂзВєз™БеПШгАБзЯ≠зЙЗ恵犯姱жПТеЕ•еПКжЯУиЙ≤дљУйЗНжОТз≠ЙеПШеЉВз±їеЮЛгАВиѓ•жЦєж°ИжФѓжМБдїОеИЭиѓКеНПеК©гАБж≤їзЦЧеЇФз≠ФеИ§жЦ≠гАБеИЖе≠РжЃЛзХЩзЧЕзБґињљиЄ™еИ∞зЦЊзЧЕињЫе±ХжПРеЙНйҐДи≠¶зЪДеЕ®еС®жЬЯжЧ†еИЫзЃ°зРЖгАВзЫЄеЕ≥ж£АжµЛз≠ЦзХ•еЈ≤襀2025зЙИNCCNжМЗеНЧжО®иНРпЉМдЄЇжЈЛеЈізШ§зЪДдЄ™дљУеМЦиѓКзЦЧжПРдЊЫдЇЖеЭЪеЃЮзЪДжКАжЬѓжФѓжТСгАВ

