иГґиі®жѓНзїЖиГЮзШ§пЉИGBMпЉЙзі†жЬЙиДСзЩМдєЛзОЛдєЛзІ∞пЉМжБґжАІз®ЛеЇ¶жЮБйЂШгАБеЕНзЦЂжКСеИґжЮБеЉЇпЉМжШѓеЕЄеЮЛзЪДеЖЈиВњзШ§вАФвАФT зїЖиГЮињЫдЄНеОїгАБжЭАдЄНеК®пЉМеЕНзЦЂж≤їзЦЧе±°е±°зҐ∞е£БгАВ
¬† ¬† ¬†еНХжђ°зШ§еЖЕж≥®е∞ДжЇґзШ§зЧЕжѓТrQNestin34.5v.2пЉМе∞±иГљиЃ©иГґиі®жѓНзїЖиГЮзШ§иљђеПШдЄЇзГ≠иВњзШ§пЉМиѓ±еѓЉжЈ±еЇ¶гАБжМБдєЕзЪДTзїЖиГЮжњАжіїдЄОиВњзШ§жЭАдЉ§пЉМдЄФзЦЧжХИдЄОTзїЖиГЮеЕЛйЪЖжЙ©еҐЮзЫіжО•зЫЄеЕ≥пЉБ

иГґиі®жѓНзїЖиГЮзШ§пЉИGBMпЉЙжШѓжБґжАІз®ЛеЇ¶жЮБйЂШзЪДдЄ≠жЮҐз•ЮзїПз≥їзїЯиВњзШ§пЉМеЕНзЦЂжКСеИґеЊЃзОѓеҐГжШѓж≤їзЦЧж†ЄењГзУґйҐИгАВ
¬Ј¬†иВњзШ§еЖЕTзїЖиГЮ浪洶жЮБе∞СпЉМдЄФе§ЪжїЮзХЩдЇОи°АзЃ°еС®еЫіпЉМжЧ†ж≥ХжЈ±еЕ•иВњзШ§еЃЮиі®пЉЫ
¬Ј¬†еЕНзЦЂж£АжЯ•зВєжКСеИґеЙВеЬ®GBMдЄ≠е§Ъжђ°дЄіеЇК姱еИ©пЉМдЉ†зїЯзЦЧж≥Хе§НеПСзОЗйЂШгАБйҐДеРОжЮБеЈЃпЉЫ
¬Ј¬†жЇґзШ§зЧЕжѓТеПѓйАЙжЛ©жАІи£ВиІ£иВњзШ§зїЖиГЮгАБиѓ±еПСеЕНзЦЂеОЯжАІж≠їдЇ°пЉМжШѓе∞ЖеЖЈиВњзШ§иљђдЄЇзГ≠иВњзШ§зЪДжљЬеКЫжЦєж°ИпЉМдљЖдЇЇз±їиГґиі®зШ§дЄ≠йХњжХИеЕНзЦЂжњАжіїжЬЇеИґдїНдЄНжШОз°ЃгАВ

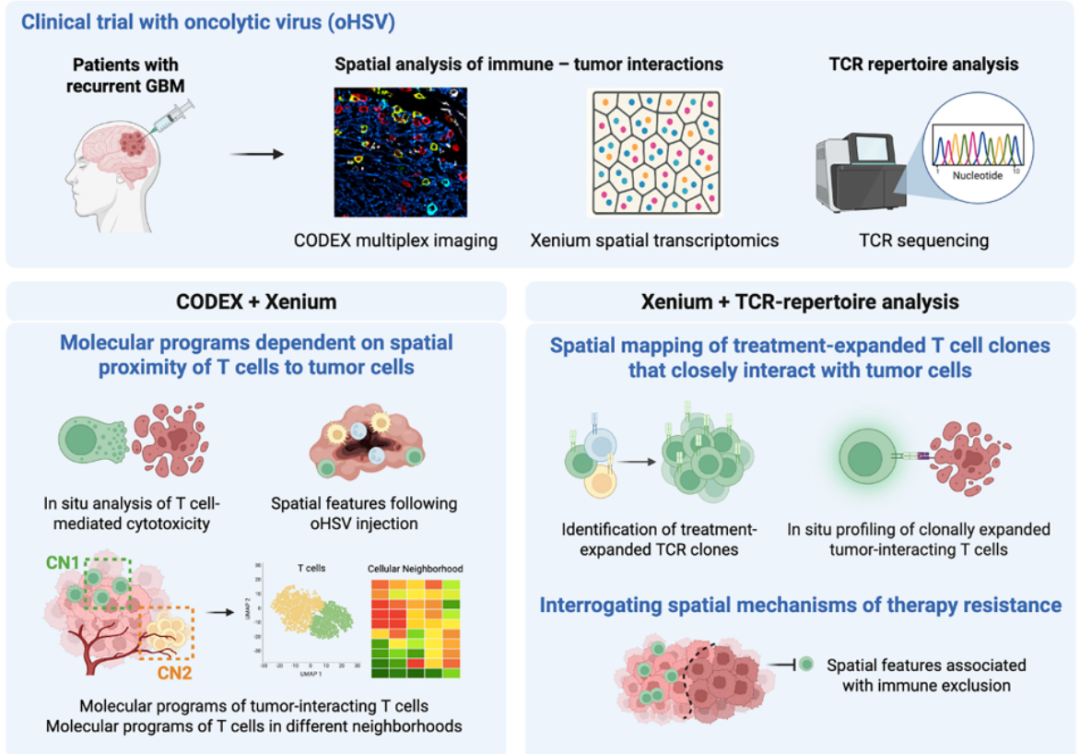
з†Фз©ґйЗЗзФ®е§ЪзїДе≠¶+з©ЇйЧіеОЯдљНжКАжЬѓиБФеРИиІ£жЮРпЉМеЃМжХіи¶ЖзЫЦзїДзїЗгАБзїЖиГЮгАБеЕЛйЪЖгАБеИЖе≠Ре±ВйЭҐпЉЪ
1. дЄіеЇКж†ЈжЬђпЉЪеЕ±иЃ°16дЊЛе§НеПСGBMжВ£иАЕпЉМеНХжђ°зШ§еЖЕж≥®е∞ДжЇґзШ§зЧЕжѓТпЉМйЕНеѓєж≤їзЦЧеЙНжіїж£А/ж≤їзЦЧеРОжЙЛжЬѓж†ЗжЬђпЉЫ
2. з©ЇйЧіиЫЛзЩљзїДпЉЪCODEXе§ЪйЗНеЕНзЦЂиНІеЕЙпЉМ27дЄ™ж†ЗењЧзЙ©пЉМиІ£жЮРзїЖиГЮи°®еЮЛдЄОз©ЇйЧідЇТдљЬпЉЫ
3. з©ЇйЧіиљђељХзїДпЉЪ10X Genomics XeniumпЉМ380дЄ™иВњзШ§еЕНзЦЂеЯЇеЫ†+100дЄ™еЃЪеИґжОҐйТИпЉМеЃЪдљНTзїЖиГЮжіїеМЦгАБиВњзШ§еИЖеЮЛгАБзЧЕжѓТжЃЛзХЩпЉЫ
4. TCRжµЛеЇПпЉЪеѓє33дЊЛжВ£иАЕиВњзШ§зїДзїЗ+е§ЦеС®и°АињЫи°МTCRќ≤йУЊйЂШйАЪйЗПжµЛеЇПпЉМеИЖжЮРеЕЛйЪЖжЙ©еҐЮгАБеЕЛйЪЖеЮЛгАБж≤їзЦЧеЙНеРОеПШеМЦпЉЫ
5. еНХзїЖиГЮRNA-seqпЉЪй™МиѓБTзїЖиГЮеКЯиГљзКґжАБдЄОTCRеЕЛйЪЖеѓєеЇФеЕ≥з≥їпЉЫ
6. зїЯиЃ°еИЖжЮРпЉЪз©ЇйЧійВїињСеИЖжЮРгАБзїЖиГЮйВїеЯЯпЉИCNпЉЙгАБзФЯе≠ШеЕ≥иБФгАБеЕЛйЪЖеѓМйЫЖеИЖжЮРгАВ

¬Ј¬†ж≤їзЦЧеРОCD8вБЇ TгАБCD4вБЇ TзїЖиГЮеѓЖеЇ¶жШЊиСЧеНЗйЂШпЉМCD8/TregжѓФдЊЛжПРеНЗпЉЫ
¬Ј¬†TзїЖиГЮеПѓжЈ±еЕ•иВњзШ§еЃЮиі®пЉМзЦЧжХИзїіжМБиґЕ6дЄ™жЬИпЉМжЬАйХњиЊЊ2еєідї•дЄКпЉЫ
¬Ј¬†ељҐжИРжЈЛеЈіиБЪйЫЖдљУпЉМдЄЇеЕНзЦЂеЇФз≠ФжПРдЊЫеЯЇз°АгАВ
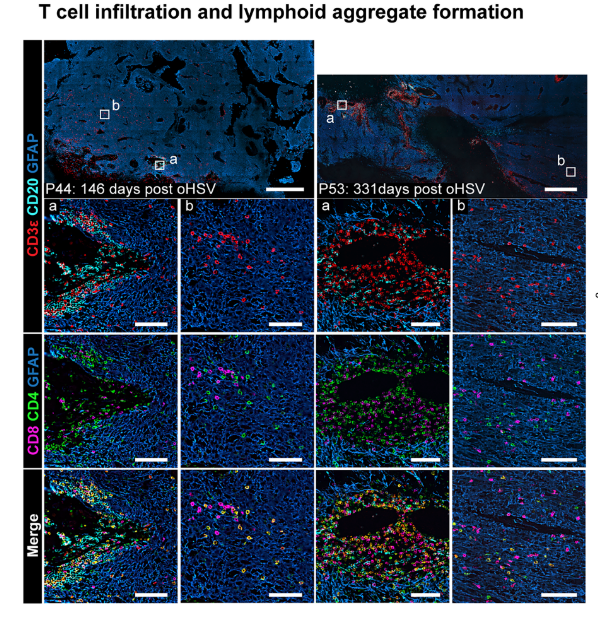
fig. 2¬†TзїЖиГЮ棱寶浪洶дЄОжЈЛеЈіиБЪйЫЖдљУ
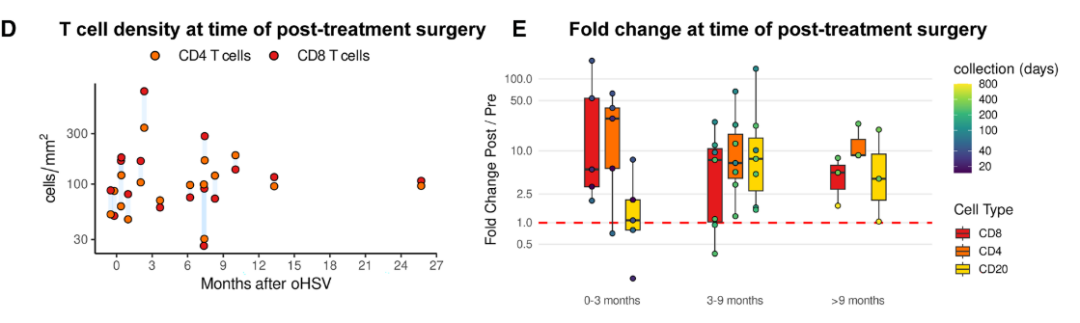
fig. 3¬†TзїЖиГЮеѓЖеЇ¶йЪПжЧґйЧі/еЙВйЗПеПШеМЦжХ£зВєеЫЊ
¬Ј¬†GZMBвБЇ CD8вБЇ TзїЖиГЮдЄО cl-Casp3вБЇеЗЛдЇ°иВњзШ§зїЖиГЮз©ЇйЧійЂШеЇ¶йВїињСпЉЫ
¬Ј¬†дЄ§иАЕиЈЭз¶їиґКињСпЉМжЧ†ињЫе±ХзФЯе≠ШжЬЯиґКйХњгАБиВњзШ§зФЯйХњиґКжЕҐгАВ
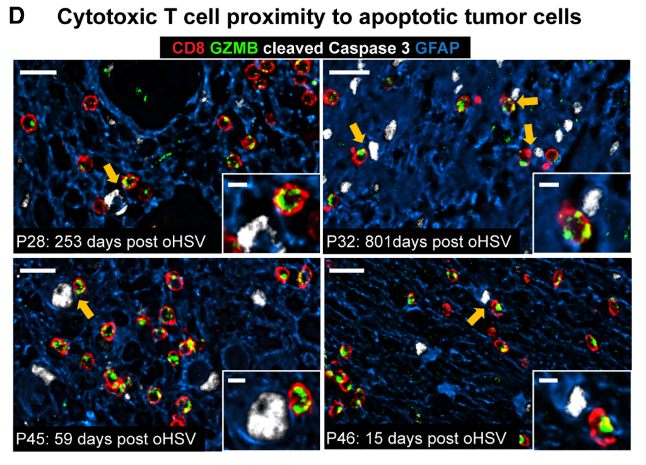
fig. 4¬†GZMBвБЇTзїЖиГЮзіІйВїеЗЛдЇ°иВњзШ§зїЖиГЮеОЯдљНеЫЊ
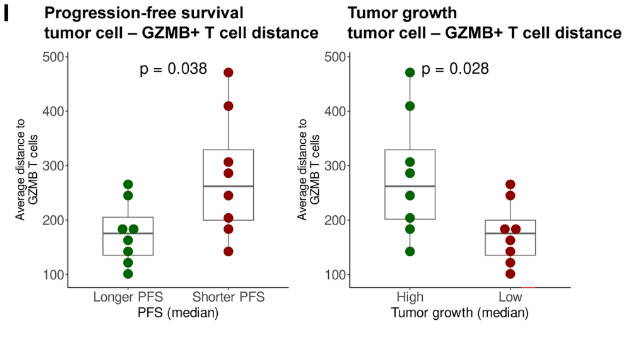
fig. 5¬†TзїЖиГЮ-иВњзШ§иЈЭз¶їдЄОPFSгАБиВњзШ§зФЯйХњйАЯзОЗеЕ≥иБФеЫЊ
¬Ј¬†иВњзШ§ињСзЂѓпЉЪжЧ©жЬЯжіїеМЦпЉИNR4A1гАБCD69пЉЙ+зїДзїЗй©їзХЩпЉИCD103гАБHOBITпЉЙ+йЂШзїЖиГЮжѓТжАІпЉЫ
¬Ј¬†жЈЛеЈіеМЇеЯЯпЉЪеє≤зїЖиГЮж†ЈTзїЖиГЮпЉМиіЯиі£жМБзї≠и°•еЕЕжХИеЇФTзїЖиГЮгАВ
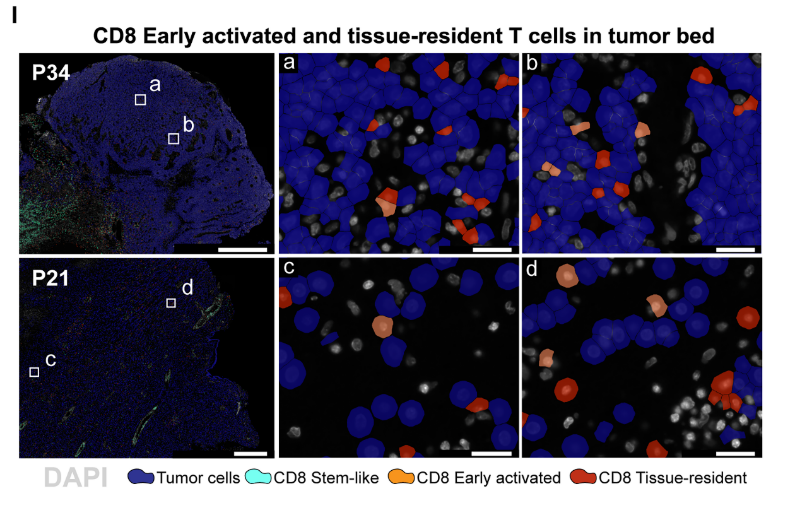
fig. 6¬†Xenium жШЊз§ЇжіїеМЦ T зїЖиГЮзіІиііиВњзШ§зїЖиГЮ
йАЪињЗTCRжµЛеЇПжП≠з§ЇпЉЪ
¬Ј¬†иВњзШ§еЖЕTзїЖиГЮеЕЛйЪЖжАІжШЊиСЧдЄКеНЗпЉМи°Ажґ≤жЧ†жШОжШЊеПШеМЦпЉМеПНеЇФйЂШеЇ¶е±АеЯЯеМЦпЉЫ
¬Ј¬†ж≤їзЦЧеЙНеЈ≤е≠ШеЬ®зЪДTзїЖиГЮеЕЛйЪЖ襀姲иІДж®°жЙ©еҐЮпЉМиАМйЭЮжЦ∞еЕЛйЪЖдЇІзФЯпЉЫ
¬Ј¬†еЕЛйЪЖжЙ©еЉ†з®ЛеЇ¶дЄОжАїзФЯе≠ШжЬЯжШЊиСЧж≠£зЫЄеЕ≥пЉЫ
¬Ј¬†жЙ©еҐЮеЕЛйЪЖеЗ†дєОжЧ†HSVзЧЕжѓТзЙєеЉВжАІпЉМдї•иВњзШ§еПНеЇФжАІдЄЇдЄїгАВ
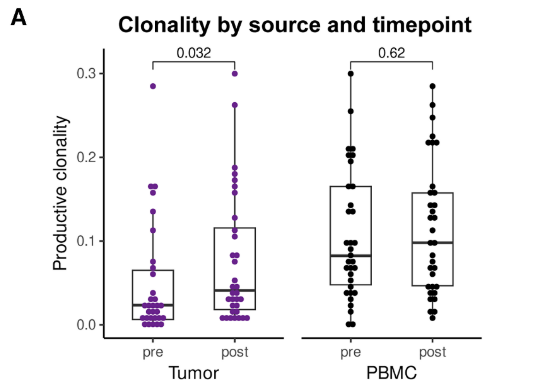
fig. 7¬†ж≤їзЦЧеЙНеРОиВњзШ§/и°Ажґ≤TCRеЕЛйЪЖжАІеѓєжѓФ
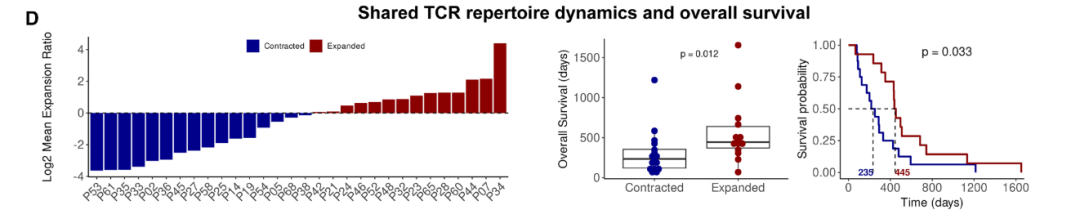
fig. 8¬†еЕЛйЪЖжЙ©еЉ†зїДvsжФґзЉ©зїДзФЯе≠ШжЬЯKMжЫ≤зЇњ
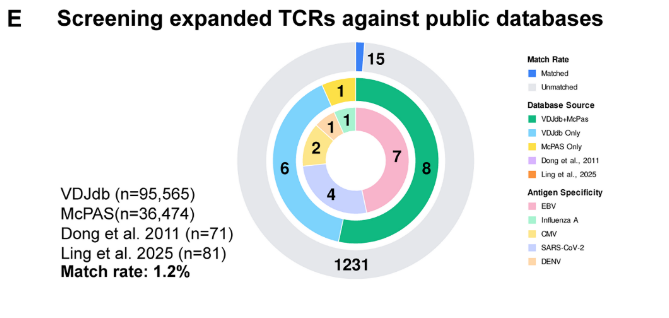
fig. 9¬†TCRеЕЛйЪЖжКЧеОЯзЙєеЉВжАІжѓФеѓєз΃嚥еЫЊ
¬Ј¬†ж≤їзЦЧеРОе§НеПСж†ЈжЬђдЄ≠зЉЇж∞ІеЮЛMES-like 2дЇЪзЊ§жШЊиСЧжЙ©еЉ†пЉЫ
¬Ј¬†йЂШи°®иЊЊCA9гАБVEGFAпЉМ嚥жИРTзїЖиГЮжОТжЦ•е±ПйЪЬпЉЫ
¬Ј¬†йХњжЬЯеЬ∞е°Юз±≥жЭЊдљњзФ®дЉЪеЙКеЉ±TзїЖиГЮеЕЛйЪЖжЙ©еҐЮгАВ
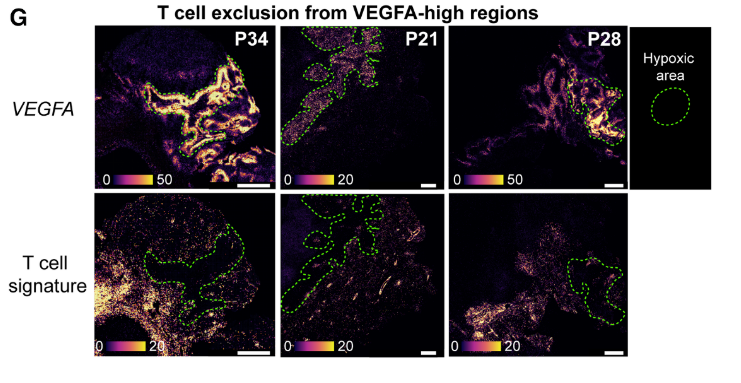
fig. 10¬†VEGFAвБЇзЉЇж∞ІеМЇжОТжЦ• T зїЖиГЮз©ЇйЧіеЫЊ

иѓ•з†Фз©ґй¶Цжђ°еЬ®дЇЇGBMдЄ≠иѓБеЃЮпЉЪ
еНХжђ°жЇґзШ§зЧЕжѓТеН≥еПѓиІ¶еПСжМБдєЕгАБжЈ±еЇ¶зЪДTзїЖиГЮжКЧиВњзШ§еЕНзЦЂпЉЫ
з©ЇйЧіе§ЪзїДе≠¶зЫіжО•еПСзО∞TзїЖиГЮеОЯдљНжЭАдЉ§пЉМиЈЭз¶їжМЗж†ЗеПѓйҐДжµЛзЦЧжХИпЉЫ
TCRжµЛеЇПжШОз°Ѓж†ЄењГжЬЇеИґпЉЪжФЊе§ІеОЯжЬЙиВњзШ§еПНеЇФжАІTзїЖиГЮеЕЛйЪЖпЉМиАМйЭЮжКЧзЧЕжѓТеЕНзЦЂгАВ
еЬ®дЄіеЇКз†Фз©ґжЦєйЭҐпЉМжЇґзШ§зЧЕжѓТеПѓдљЬдЄЇGBMеЕНзЦЂеЯЇзЯ≥зЦЧж≥ХпЉМеНХжђ°зїЩиНѓеН≥еПѓеЃЮзО∞йХњжХИеЕНзЦЂпЉЫTCRеЕЛйЪЖжЙ©еҐЮеПѓдљЬдЄЇзЦЧжХИйҐДжµЛзФЯзЙ©ж†ЗењЧзЙ©пЉМжМЗеѓЉжВ£иАЕеИЖе±ВпЉЫдЄіеЇКеЇФе∞љйЗПзЉ©зЯ≠еЬ∞е°Юз±≥жЭЊдљњзФ®жЧґйХњпЉМдњЭжК§TзїЖиГЮеЇФз≠ФгАВ
жЬ™жЭ•пЉМеПѓеЉАе±ХжЇґзШ§зЧЕжѓТ+еЕНзЦЂж£АжЯ•зВєжКСеИґеЙВдЄіеЇКиѓХй™МпЉМжПРеНЗе§НеПСжАІGBMзФЯе≠ШзОЗгАВ
еПВиАГжЦЗзМЃпЉЪMeylan M, Tian Y, Wu L, et al., Persistent T cell activation and cytotoxicity against glioblastoma following single oncolytic virus treatment in a clinical trial,¬†Cell, 2026, 189, 1287-1304.
иЙЊж≤РиТљдЄУж≥®дЇОеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯе§ЪеєіпЉМеЉАеПСзЪДImmuHub¬ЃжКАжЬѓеє≥еП∞жЦєж≥ХеЕ®йЭҐпЉМж£АжµЛзЙ©зІНе§Ъж†ЈпЉМеїЇеЇУжЦєж≥ХеЕЈжЬЙзБµжіїжАІпЉМиЗіеКЫдЇОдЄЇеРДе§ІйЂШж†°гАБеМїйЩҐгАБзІСз†ФжЬЇжЮДгАБдЉБдЄЪз≠ЙжПРдЊЫдЉШиЙѓзЪДзІСз†ФжЬНеК°гАВ

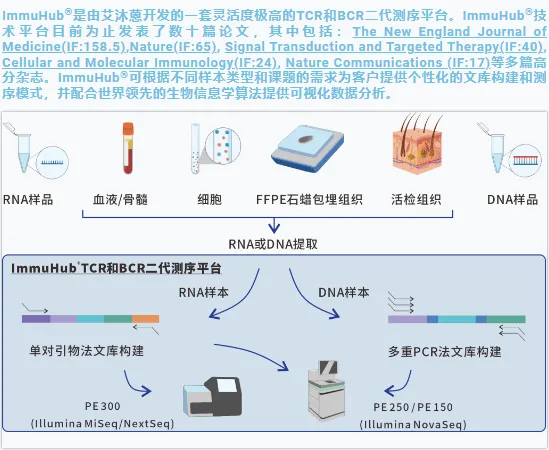
ImmuHub¬ЃйГ®еИЖзІСз†ФжЦєеРС

ImmuHub¬ЃйАВзФ®еЯЇеЫ†еЇІ
йГ®еИЖжХ∞жНЃеИЖжЮРзїУжЮЬе±Хз§Ї
жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄжИРзЂЛдЇО2016еєіпЉМжШѓеЫљйЩЕеЙНж≤њзЪДдЄУж≥®дЇОеЕНзЦЂй©±еК®еМїе≠¶жКАжЬѓзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪеТМдЄУз≤ЊзЙєжЦ∞дЉБдЄЪгАВеИЫеІЛдЇЇеЫҐйШЯжЭ•иЗ™зЊОеЫљиКЭеК†еУ•е§Іе≠¶пЉМеЬ®2010еєіеЉАеІЛдљњзФ®еЕНзЦЂзїДеЯЇеЫ†йЂШйАЪйЗПжµЛеЇПжКАжЬѓеЉАе±ХеРДзІНзЦЊзЧЕзЫЄеЕ≥з†Фз©ґпЉМдЇО2016еєійАЪињЗиЗ™дЄїз†ФеПСпЉМеЕ®еЫљй¶ЦеЃґжО®еЗЇNGS-MRDи°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛSeq-MRD¬ЃпЉМеєґжОИжЭГж≥ЫзФЯе≠РдљњзФ®гАВеРМжЧґпЉМеЕђеПЄжЛ•жЬЙImmun-Traq¬ЃиВњзШ§ж≤їзЦЧдЉійЪПиѓКжЦ≠гАБImmun-Cheq¬Ѓ¬†еЕНзЦЂеКЫжµЛиѓДдї•еПКImmuHub¬ЃеЕНзЦЂзїДжµЛеЇПзІСз†ФжЬНеК°дЇІеУБпЉМеєґеЄГе±АжЬЙеЯЇдЇОAIжЬЇеЩ®е≠¶дє†зЃЧж≥ХзЪДT-classifier¬ЃиВњзШ§жЧ©з≠ЫгАБеНХзїЖиГЮжµЛеЇПгАБжЦ∞жКЧеОЯгАБTCRеТМжКЧдљУеПСзО∞з≠Йеє≥еП∞зЃ°зЇњгАВзЫЃеЙНдЄЇж≠ҐеПСи°®дЇЖ60дљЩзѓЗиЃЇжЦЗпЉМеЕґдЄ≠еМЕжЛђпЉЪThe New England Journal of Medicine(IF:158.5), The Lancet(IF:98.4), Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24),¬†Nature Communications¬†(IF:17)з≠Йе§ЪзѓЗйЂШеИЖжЭВењЧгАВеЕђеПЄжЮДеїЇеЗ†еНБй°єеПСжШОдЄУеИ©еТМиљѓдїґиСЧдљЬжЭГдЄЇж†ЄењГзЪДиЗ™дЄїзЯ•иѓЖдЇІжЭГдљУз≥їпЉМдЄЇеМїйЩҐдЄіеЇКгАБзФЯеСљзІСе≠¶з†Фз©ґгАБжЦ∞иНѓеЉАеПСз≠ЙжПРдЊЫиІ£еЖ≥жЦєж°ИеТМдЇІеУБгАВиЙЊж≤РиТљдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХгАВ



