еЦЬиЃѓпЉБ
ињСжЧ•пЉМзФ±еЕђеПЄиЗ™дЄїз†ФеПСзЪДMRDж£АжµЛжЦєж≥ХеПИдЄАй°єеПСжШОдЄУеИ©иОЈеЊЧеЫљеЃґзЯ•иѓЖдЇІжЭГе±АеПСжШОдЄУеИ©иѓБдє¶пЉИжОИжЭГеЕђеСКжЧ•пЉЪ2022еєі12жЬИ2жЧ•пЉЙгАВ
иЙЊж≤РиТљжО®еЗЇзЪДSeq-MRD¬Ѓи°Ажґ≤зЩМзЧЗMRDж£АжµЛжШѓжЬАжЧ©жЙєеЃЮзО∞еХЖдЄЪеМЦзЪДдЇІеУБпЉМиЗ™2016еєіз†ФеПСдЄУеИ©жКАжЬѓдї•жЭ•пЉМжИ™иЗ≥зЫЃеЙНпЉМиЙЊж≤РиТљSeq-MRD¬ЃеЈ≤зїПиОЈеЊЧ3й°єеЫљеЃґеПСжШОдЄУеИ©пЉЪ
вАЬдЄАзІНеЇФзФ®дЇОйЂШйАЪйЗПжµЛеЇПж£АжµЛTзїЖиГЮзЩљи°АзЧЕеЊЃе∞ПжЃЛзХЩзЧЕзЪДеЉХзЙ©зїДеРИеПКиѓХеЙВзЫТвАЭпЉИжОИжЭГеЕђеСКжЧ•пЉЪ2020еєі4жЬИ28жЧ•пЉЙпЉЫ
вАЬдЄАзІНж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕMRDзЪДиѓХеЙВзЫТвАЭпЉИжОИжЭГеЕђеСКжЧ•пЉЪ2022еєі7жЬИ19жЧ•пЉЙпЉЫ
вАЬдЄАзІНж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕMRDзЪДжЦєж≥ХвАЭпЉИжОИжЭГеЕђеСКжЧ•пЉЪ2022еєі12жЬИ2жЧ•пЉЙгАВ
Seq-MRD¬ЃдЄУеИ©иѓБдє¶дЄАиІИ

дїАдєИжШѓSeq-MRD¬Ѓ
еЯЇдЇОеЕНзЦЂзїД(lg/TCR) дЇМдї£жµЛеЇП(next generation sequencingпЉМNGS)жКАжЬѓпЉМзїУеРИзФЯзЙ©дњ°жБѓе≠¶еИЖжЮРпЉМеЗЖз°ЃжЯ•жЙЊзїЖиГЮеЕЛйЪЖеЇПеИЧйЂШзБµжХПеЬ∞ињљиЄ™ж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕ(MRD)ж∞іеє≥пЉМеЄЃеК©дЄіеЇКйҐДжµЛйХњжЬЯзЦЧжХИгАБиѓДдЉ∞ж≤їзЦЧжХИжЮЬгАБзЫСжµЛзЉУиІ£зКґжАБдї•еПКж£АжµЛжЧ©жЬЯе§НеПСгАВ
Seq-MRD¬ЃжКАжЬѓеОЯзРЖ
жѓПзІНB/TжЈЛеЈізїЖиГЮи°®йЭҐеЭЗе≠ШеЬ®дЄАзІНзЙєеЉВжАІBзїЖиГЮеПЧдљУ B cell receptor,BCR/la)TзїЖиГЮеПЧдљУ (T cell receptor,TCR)пЉМзФ±дЇОBCR/TCRеЫ†дЄ≠VгАБDгАБJеЯЇеЫ†зЙЗжЃµйЗНзїДдЄО祱еЯЇзЪДйЪПжЬЇжПТеЕ•гАБеИ†еЗПпЉМеѓЉиЗіBCR/TCRеЕЈжЬЙйЂШеЇ¶е§Ъж†ЈжАІзЪДзЙєзВєпЉМдїОиАМBCR/TCRеПѓдљЬдЄЇжѓПдЄ™BTжЈЛеЈізїЖиГЮеФѓдЄАзЪДеИЖе≠Рж†Зз≠ЊгАВ
жЈЛз≥їи°Ажґ≤зЩМзЧЗжВ£иАЕеЫ†BTжЈЛеЈізїЖиГЮеПСзФЯзЩМеПШпЉМзЩМзїЖиГЮзїІиАМиЗ™жИСе§Неȴ嚥жИРеЕЛйЪЖжАІеҐЮжЃЦпЉМеЫ†ж≠§пЉМйАЪињЗж£АжµЛB/TжЈЛеЈізїЖиГЮи°®йЭҐеПЧдљУBCR/TCRеПѓдї•йЙіеЃЪзЩМзїЖиГЮеєґињљиЄ™ж£АжµЛзЩМзїЖиГЮзЪДеК®жАБеПШеМЦгАВ
Seq-MRD¬Ѓж£АжµЛз±їеЮЛ
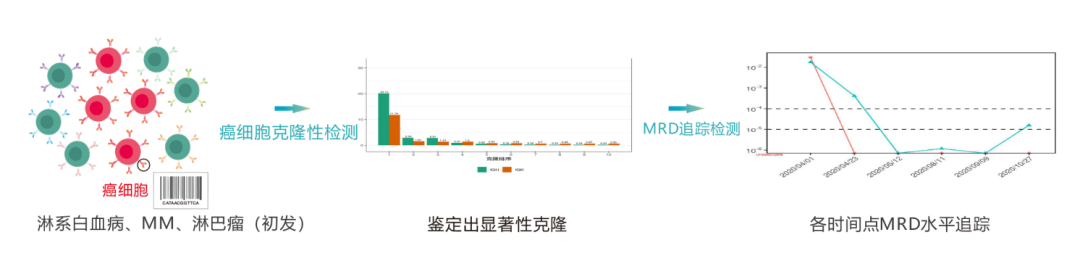
1.зЩМзїЖиГЮеЕЛйЪЖжАІж£АжµЛ
йАЪињЗжВ£иАЕеИЭиѓКжИЦзЩМзїЖиГЮйЂШиіЯиНЈжЧґзЪДй™®йЂУж†ЈжЬђпЉМжЙЊеИ∞зЩМзїЖиГЮзЙєжЬЙзЪДDNAвАЬж†Зз≠ЊвАЭеЇПеИЧгАВ
2.MRDињљиЄ™ж£АжµЛ
еИ©зФ®з≠ЫжЯ•еЗЇзЪДDNAвАЬж†Зз≠ЊвАЭеЇПеИЧпЉМеЬ®ж≤їзЦЧжЬЯйЧіжИЦж≤їзЦЧеРОиѓДдЉ∞MRDж∞іеє≥пЉМзЫСжµЛзЩМзїЖиГЮеРЂйЗПпЉМеРМжЧґж£АжµЛиѓЖеИЂжЦ∞еЗЇзО∞зЪДзЩМзїЖиГЮеЇПеИЧгАВ
Seq-MRD¬ЃйАВзФ®дЇЇзЊ§
1. Bз≥їи°Ажґ≤з≥їзїЯзЩМзЧЗ
жА•жАІ/жЕҐжАІBжЈЛеЈізїЖиГЮзЩљи°АзЧЕгАБе§ЪеПСжАІй™®йЂУзШ§гАБBеЮЛжЈЛеЈізШ§гАВ
2. Tз≥їи°Ажґ≤з≥їзїЯзЩМзЧЗ
жА•жАІ/жЕҐжАІTжЈЛеЈізїЖиГЮзЩљи°АзЧЕгАБTеЮЛжЈЛеЈізШ§гАВ
жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄзФ±зЊОеЫљиКЭеК†еУ•е§Іе≠¶зІСз†ФеЫҐйШЯеЫЮеЫљеИЫеКЮпЉМжШѓдЄАеЃґдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪгАВиЙЊж≤РиТљзЂЩеЬ®йАВеЇФжАІеЕНзЦЂз≥їзїЯз†Фз©ґзЪДеЙНж≤њпЉМиЗ™дЄїз†ФеПСзЪДеЕНзЦЂеМїе≠¶еє≥еП∞еПѓжП≠з§ЇеТМзњїиѓСйАВеЇФжАІеЕНзЦЂз≥їзїЯзЪДйБЧдЉ†еѓЖз†БпЉМеєґиГљеЇФзФ®дЇОзЩМзЧЗгАБиЗ™иЇЂеЕНзЦЂжАІзЦЊзЧЕгАБдЉ†жЯУжАІзЦЊзЧЕз≠ЙеЕНзЦЂдїЛеѓЉжАІзЦЊзЧЕзЪДиѓКжЦ≠гАБзЫСжµЛеТМж≤їзЦЧдЄ≠гАВ

