Immun-Traq®
信心源自于您知道您的治疗有效
癌症的治疗
目前有很多治疗癌症的方法和手段,如外科手术、放射治疗、化学药物治疗、靶向治疗、免疫治疗等,都有一定的疗效,而且各有优势。如免疫治疗(如PD-1,CAR-T和癌症疫苗等)作为新型癌症治疗方法,是未来癌症治疗发展的方向,被认为是对癌症有明确效果的又一重要治疗方法。但免疫治疗目前并不能使所有病人都获益,且其治疗费用高昂,因此如何预测癌症免疫治疗效果,即精准地筛选患者使其产生更好的临床获益是在治疗前和过程中非常重要的。
癌症治疗中的重要成员:T细胞
免疫系统保护我们的身体免受细菌,病毒和包括癌症在内的各种疾病的影响,并且具有治疗效果。 二代测序技术使我们能够全面研究T细胞组库。 我们对TCR 免疫组图谱的深度剖析扩展了我们对癌症免疫治疗反应的理解。
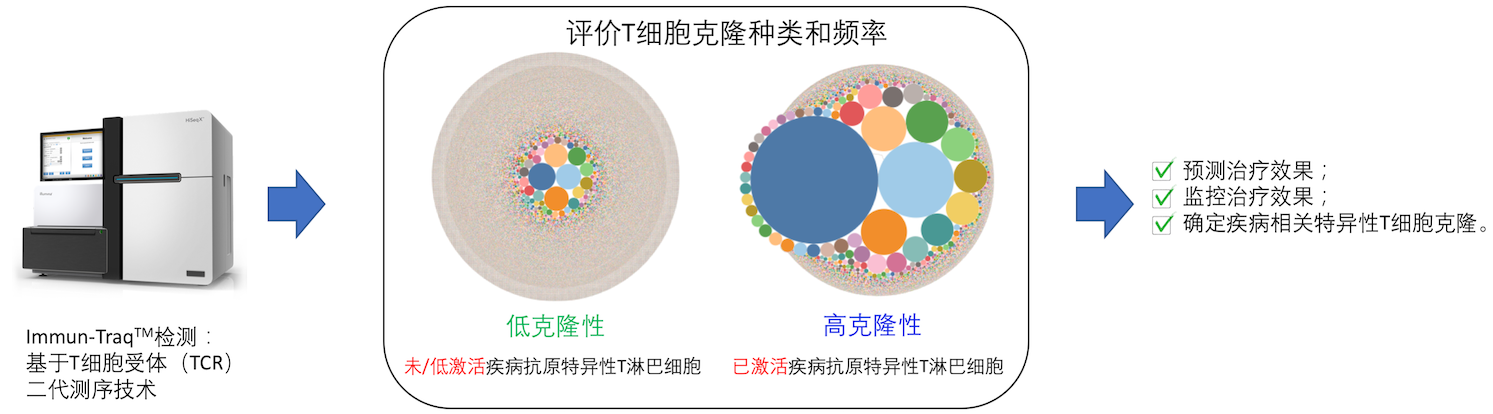
癌症治疗效果预测、评估
Immun-Traq® 可以为广大接受癌症治疗的患者提供一个快速的、非侵入性的免疫系统评估。我们通过二代测序对病患血液里的T细胞受体(TCR)基因进行多样性和克隆性分析,同时结合病患所使用的治疗方法综合评估,来帮助医疗工作者和癌症病人预测和评估治疗的效果,让病患能在对抗癌症的斗争中更有效地选择治疗手段,并且避免浪费癌症病人治疗的时间和金钱。
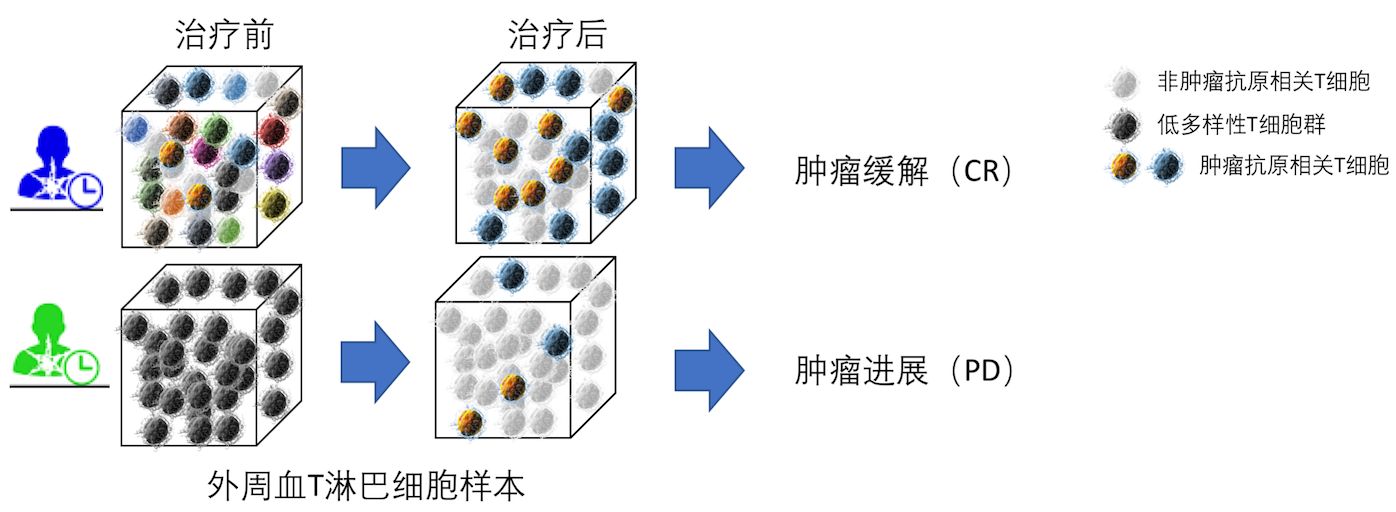
一种无创的非侵入式检测
Immun-Traq®是一种从病患的外周血单核细胞中分离出T细胞并检测其T细胞受体(TCR)的多样性和克隆性状态的分子检测手段。该测试提供的免疫学评估,仅仅是通过简单的采集患者治疗前、后的血样来评估和预测整个治疗的效果。Immun-Traq®作为肿瘤免疫治疗伴随检测已被全球很多免疫肿瘤学者验证可作为肿瘤免疫治疗病人的预后预测*,并能推动个性化肿瘤免疫治疗。与大多数其他伴随检测不同,Immun-Traq®是患者特异性的,而不是药品或疾病特异性的,因为它是从患者自身的免疫系统的角度了解疾病情况的真相。Immun-Traq®根据病人复杂的免疫系统情况来评估治疗效果。
预测和评估癌症治疗效果
随着肿瘤治疗的方法及其批准药物数量的迅速扩大,对肿瘤免疫学时代抗肿瘤疗效的评估和认识变得愈发重要。大多数对肿瘤治疗的疗效采用RECIST1.1进行评估,但我们仍然需要采用更准确的一种方法。Immun-Traq®旨在帮助肿瘤病人脱离效果不明显的治疗手段、减少不必要的治疗副作用,同时节约昂贵的费用和宝贵的治疗时间。Immun-Traq®让医生和患者能检测治疗前、后 T 细胞免疫组库的动态,这样可以帮助医生和患者更好地了解正在使用的治疗手段的疗效。我们根据治疗前的样本出具报告以判断患者是否可能会从肿瘤治疗中获益;根据治疗前+后的样本出具报告以判断患者目前正在使用的肿瘤治疗方法是否有效。
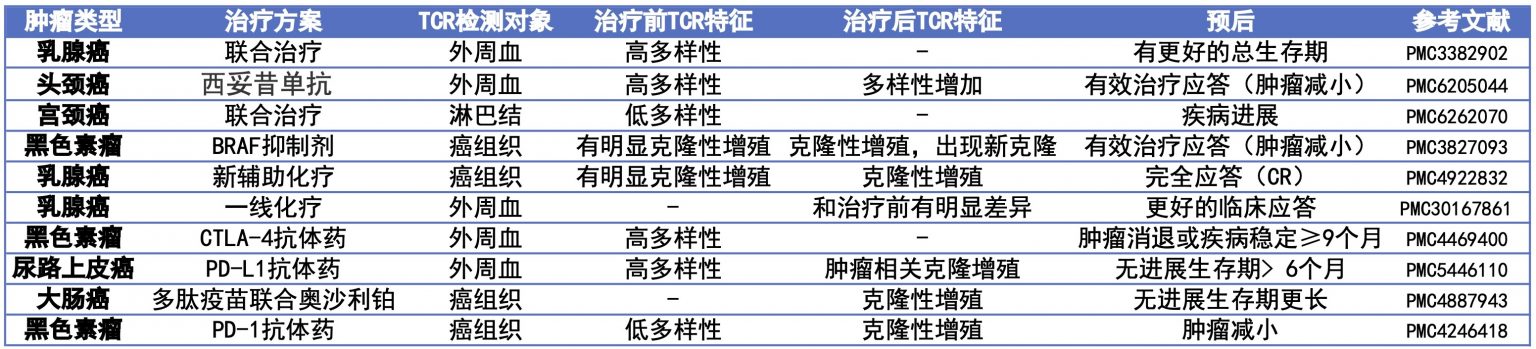
临床研究数据
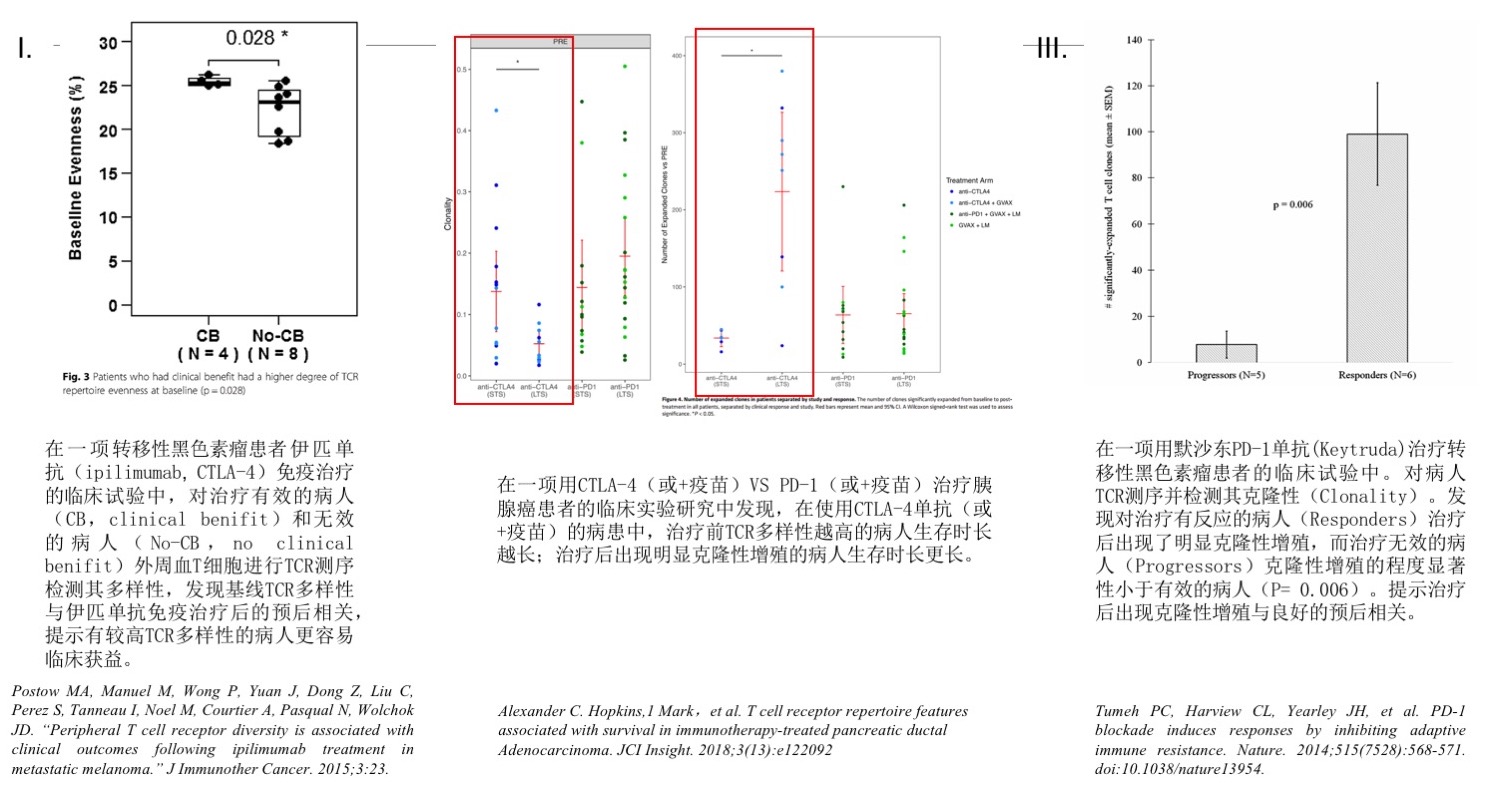
更多临床研究数据总结
关于Immun-Traq®技术
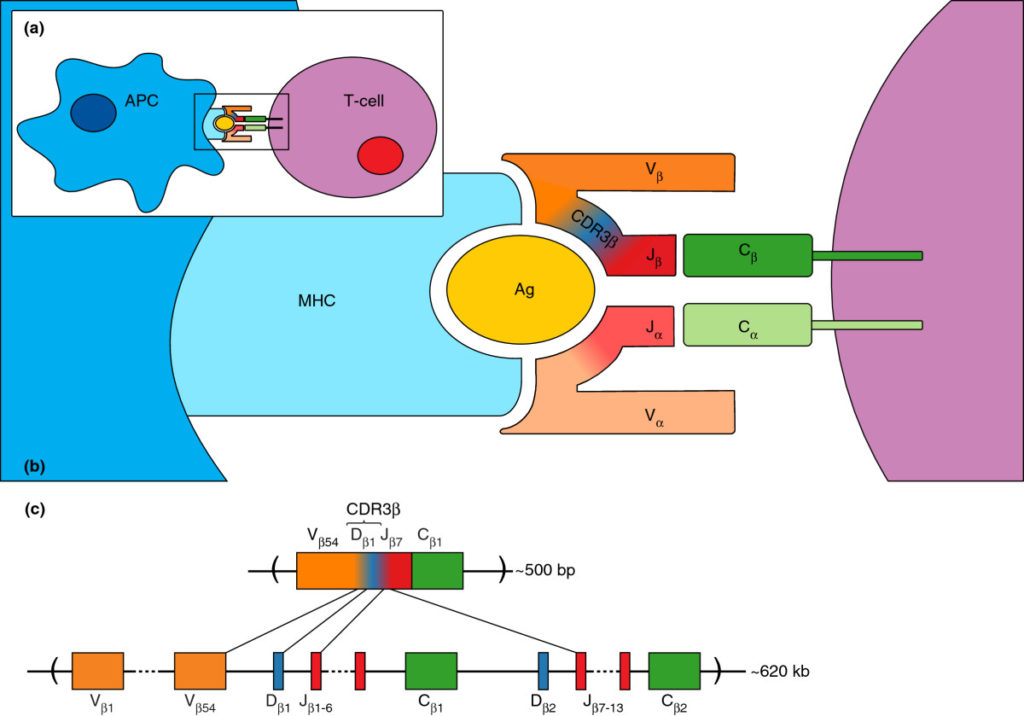
Immun-Traq®分子检测手段是基于ImmuHub®技术平台,利用从外周血分离后的T细胞的受体(下图b)RNA作为模板,配合高通量基因测序技术来检测有功能的T细胞受体(TCR)基因情况(下图c),并使用世界领先的生物信息学分析算法对测序结果进行分析,给患者和医生出具一个有指导意义的免疫系统状态报告。
Immun-Traq®的主要特点
通过治疗前后T细胞的多态性和克隆性变化来评估患者的免疫情况;
使用无创的样本收集方式 --- 血液样本采集(也可针对肿瘤组织活检样本);
先进且成熟的技术 --- 二代基因测序;
通过世界领先的生物信息学分析算法诠释临床信息。
检测样本要求
样本种类:外周血或肿瘤组织样本(治疗前后)
样本量:血液样本5~10毫升、活检样本2-3厘米
运输:血液存放在ACD或者EDTA抗凝管内,在24-48小时内通过冷藏运输方式送达艾沐蒽实验室。
Immun-Traq®检测流程

参考文献:
- PD-1 blockade induces responses by inhibiting adaptive immune resistance. Nature. 2014;515(7528):568–571
- CTLA4 blockade broadens the peripheral T-cell receptor repertoire. Clin Cancer Res 2014;20:2424–32.
- A liquid biopsy for cancer immunotherapy. Nat Med. 2016 Apr 6;22(4):340-1. doi: 10.1038/nm.4074.
- Prospective identification of neoantigen-specific lymphocytes in the peripheral blood of melanoma patients. Nat. Med. doi:10.1038/nm.4051
- Cancer immunotherapy based on mutation-specific CD4+ T cells in a patient with epithelial cancer. Science 344, 641–645 (2014)
- Quantitative T cell repertoire analysis by deep cDNA sequencing of T cell receptor α and β chains using next-generation sequencing (NGS). OncoImmunology 2014.
- Highly Clonal Regulatory T cell population in Follicular Lymphoma – Inverse Correlation with the diversity of CD8+ T cells. Oncoimmunology, 2015.
- Quantitative characterization of T cell repertoire in allogeneic hematopoietic stem cell transplant recipients. Bone Marrow Transplantation, 2015.
- Improved Survival with T Cell Clonotype Stability After Anti–CTLA-4 Treatment in Cancer Patients. Science Translational Medicine 28 May 2014: Vol. 6, Issue 238, pp. 238ra70 DOI: 10.1126/scitranslmed.3008211
- Peripheral T cell receptor diversity is associated with clinical outcomes following ipilimumab treatment in metastatic melanoma. Journal for immunotherapy of cancer 12/2015; 3(1):23. DOI: 10.1186/s40425-015-0070-4 Source: PubMed
- TCR Sequencing Can Identify and Track Glioma-Infiltrating T Cells after DC Vaccination. Cancer Immunol Res. 2016 Mar 11
