
дЄАгАБCAR-TзЦЧж≥Х
CAR-TзїЖиГЮзЦЧж≥ХжШѓдЄАзІНеЯЇдЇОдЇЇеЈ•дњЃй•∞зЪДTзїЖиГЮж≤їзЦЧпЉМеПѓдї•йАЪињЗCARпЉИchimeric antigen receptorпЉЙеИЖе≠РйЭґеРСиѓЖеИЂиВњзШ§зїЖиГЮи°®йЭҐжКЧеОЯпЉМињЫиАМжЭАдЉ§зЩМзїЖиГЮгАВ
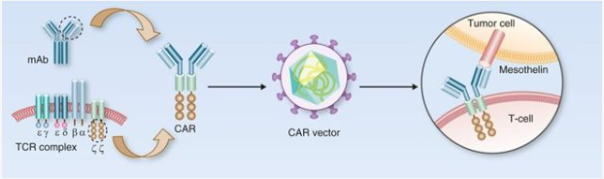
Fig. CAR-T¬†зїЖиГЮеЕНзЦЂзЦЧж≥ХеОЯзРЖз§ЇжДПеЫЊ
зЫЃеЙНпЉМCAR-TеЬ®зЩљи°АзЧЕгАБжЈЛеЈізШ§гАБе§ЪеПСжАІй™®йЂУзШ§ж≤їзЦЧдЄ≠еЊЧеИ∞еєњж≥ЫеЇФзФ®пЉМдљЖжШѓCAR-TзїЖиГЮж≤їзЦЧзЪДеПНеЇФзОЗеТМжМБзї≠жАІдїНзДґе≠ШеЬ®жМСжИШгАВ
TзїЖиГЮеПЧдљУпЉИTCRпЉЙжµЛеЇПиГље§ЯжЬЙжХИеЬ∞иѓДдЉ∞CAR-TзїЖиГЮзЪДзЙєеЊБпЉМжМБзї≠ињљиЄ™еЫЮиЊУдљУеЖЕеРОзЪДеПШеМЦгАВдЄЇдЇЖжПРйЂШCAR-TзїЖиГЮж≤їзЦЧзЪДзЦЧжХИеТМеЃЙеЕ®жАІпЉМдљњзФ®еЕНзЦЂзїДTCR NGSжКАжЬѓеЈ≤зїП襀府ж≥ЫеЬ∞еЇФзФ®дЇОCAR-TзїЖиГЮж≤їзЦЧдЄ≠пЉМеРМжЧґеЕНзЦЂзїДIg NGSжКАжЬѓиГљжЬЙжХИиѓДдЉ∞CAR-Tж≤їзЦЧеРОзЪДеЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж∞іеє≥гАВ ¬† жЬђжЦЗе∞ЖзїЉеРИдїЛзїНеЕНзЦЂзїДеЇУйЂШйАЪйЗПжµЛеЇПжКАжЬѓе¶ВдљХеК©еКЫCAR-TзїЖиГЮж≤їзЦЧеЬ®Bз≥їи°Ажґ≤зЩМзЧЗдЄ≠зЪДеЉАеПСеТМзЫСжµЛгАВ
дЇМгАБTCRжµЛеЇПеК©еКЫCAR-Tз†ФеПСеТМдЉійЪПзЫСжОІ TзїЖиГЮеЕНзЦЂзїДеЇУжµЛеЇПдї•TзїЖиГЮдЄЇз†Фз©ґзЫЃж†ЗпЉМиЙЊж≤РиТљеЯЇдЇОImmuHub¬ЃжКАжЬѓеє≥еП∞пЉМжЙ©еҐЮTCR ќ≤йУЊ VDJйЗНжОТеЯЇеЫ†еЕ®еЇПеИЧпЉМеЖНињЫи°МйЂШйАЪйЗПжµЛеЇПпЉМдїОиАМиѓДдЉ∞TзїЖиГЮеЕЛйЪЖжЮДжИРеТМе§Ъж†ЈжАІгАВињСеєіжЭ•пЉМTCRжµЛеЇП襀府ж≥ЫеЇФзФ®еЬ®CAR-TзїЖиГЮж≤їзЦЧйҐЖеЯЯгАВ
1гАБCAR-TзїЖиГЮзЪДеЕЛйЪЖжАІж£АжµЛеТМжМБдєЕжАІж£АжµЛ вС†CAR-TзїЖиГЮзЪДеЕЛйЪЖжАІж£АжµЛ FDAиНЙж°ИдЄ≠жПРеПКдЄіеЇКеЙНеЕИйЬАиѓДдЉ∞CAR-TзЪДTCRеЕЛйЪЖжЮДжИРеТМеЕЛйЪЖжАІпЉМдї•йШ≤ж≠ҐдЄНеПЧжОІеИґзЪДеҐЮжЃЦеТМжѓТжАІгАВеЕ≥дЇОCAR-TдЇІеУБзЪДиі®жОІжШѓйЭЮеЄЄйЗНи¶БзЪДзОѓиКВгАВ
CAR-TеКЯиГљжАІж£АжµЛжЦєж≥ХдЄїи¶Бж£АжµЛCAR-TзїЖиГЮзЪДзФЯзЙ©е≠¶еКЯиГљпЉМеМЕжЛђзїЖиГЮжЭАдЉ§жіїжАІгАБзїЖиГЮеЫ†е≠РйЗКжФЊгАБзїЖиГЮињБзІїиГљеКЫз≠ЙпЉМеЄЄзФ®зЪДжЦєж≥ХеМЕжЛђзїЖиГЮжЭАдЉ§еЃЮй™МгАБELISAз≠ЙгАВиАМињЩдЇЫжЦєж≥ХдЄНиґ≥дї•иѓДдЉ∞CAR-TзїЖиГЮдЄ≠зЪДTзїЖиГЮеПЧдљУзЙєзВєпЉМTCRеЕЛйЪЖжАІеТМе§Ъж†ЈжАІиГљеПНжШ†CAR-TзїЖиГЮеИґе§ЗињЗз®ЛдЄ≠зЪДеЕЛйЪЖжЮДжИРеТМеКЯиГљпЉМињЫиАМиѓДдЉ∞CAR-TзїЖиГЮдЇІеУБзЪДиі®йЗПеТМеКЯиГљгАВ
еЕЛйЪЖжАІжМЗзЪДжШѓCAR-TзїЖиГЮдЄ≠еЕЛйЪЖзЪДз®ЛеЇ¶пЉМTCRеЕЛйЪЖеЇ¶ињЗйЂШдЉЪеѓЉиЗіеЕНзր姱и∞ГеТМеЕЛйЪЖжАІзЦЊзЧЕзЪДеПСзФЯпЉЫTCRе§Ъж†ЈжАІеИЩжМЗCAR-TзїЖиГЮдЄ≠зЪДTзїЖиГЮеПЧдљУпЉИTCRпЉЙеЇПеИЧзЪДе§Ъж†ЈжАІпЉМе§Ъж†ЈжАІиґКйЂШпЉМCAR-TзїЖиГЮеЬ®жЭАдЉ§иВњзШ§зїЖиГЮзЪДжХИжЮЬиґКе•љгАВ ¬† жХ∞жНЃе±Хз§Ї¬†¬† Fig. TCRVќ≤ distribution in CD8вИТ (left) and CD8+ (right) CAR T cells in the cellular infusion product of Patient-10.
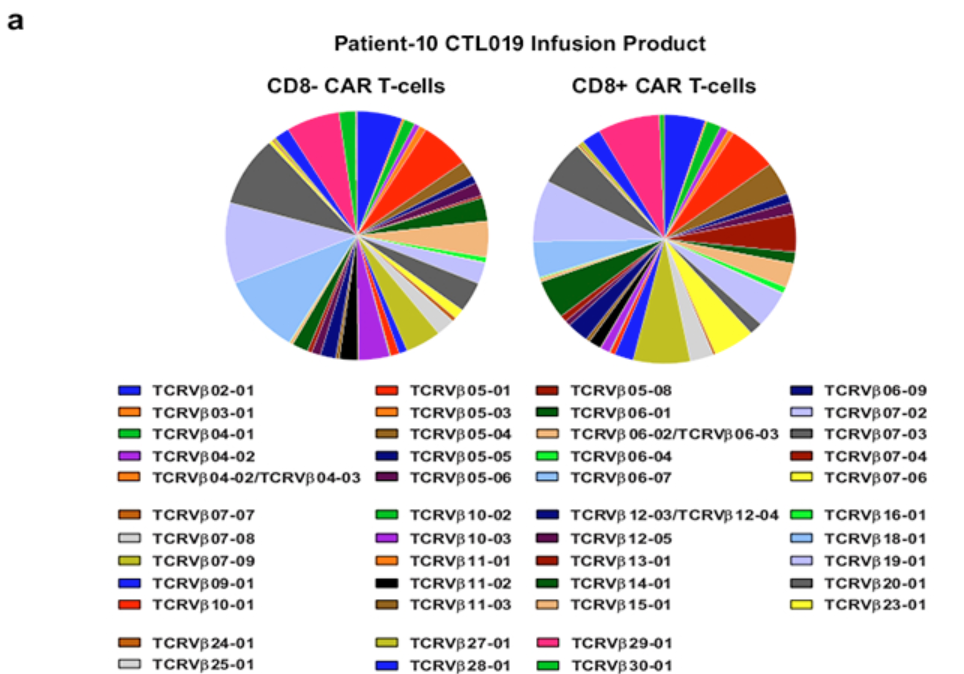
Fig. Frequency of TCRVќ≤¬†gene segment usage in the blood of Patient-10 one month (left) and¬†two months (middle) after the second CAR T cell infusion. Joseph, F. et al.еЬ®NatureдЄКеПСи°®зЫЄеЕ≥жИРжЮЬпЉМжХ∞жНЃи°®жШОйАЪињЗTCR NGSжµЛеЇПеѓє CAR-TзїЖиГЮдЇІеУБж£АжµЛеЕЛйЪЖжЮДжИРпЉМTCRVќ≤еЕЈжЬЙйЂШеЇ¶е§Ъж†ЈжАІпЉМиЊУж≥®еРОCAR-T TCRVќ≤5.1еЕЛйЪЖйЂШеЇ¶еҐЮжЃЦеєґжМБдєЕе≠ШеЬ®дїОиАМеѓєжКЧиВњзШ§гАВ
дї•дЄКиѓіжШОпЉМйАЪињЗеѓєCAR-TзїЖиГЮдЄ≠зЪДTзїЖиГЮеПЧдљУпЉИTCRпЉЙињЫи°МжµЛеЇПеИЖжЮРпЉМеПѓдї•з°ЃеЃЪCAR-TзїЖиГЮзЪДеЕЛйЪЖжЮДжИРеТМе§Ъж†ЈжАІпЉМињЩеПѓдї•дЄЇCAR-Tж≤їзЦЧзЪДзЫСжµЛеТМйҐДеРОиѓДдЉ∞жПРдЊЫйЗНи¶Бдњ°жБѓгАВж≠§е§ЦпЉМTCRжµЛеЇПињШеПѓдї•зФ®дЇОж£АжµЛCAR-TзїЖиГЮзЪДеҐЮжЃЦеТМзФЯе≠ШиГљеКЫпЉМдї•еПКCAR-TзїЖиГЮдЄОиВњзШ§зїЖиГЮзЪДзЫЄдЇТдљЬзФ®ж®°еЉПгАВйАЪињЗеѓєTCRжµЛеЇПжХ∞жНЃзЪДеИЖжЮРпЉМеПѓдї•еЄЃеК©дЉШеМЦCAR-Tж≤їзЦЧзЪДиЃЊиЃ°еТМдЉШеМЦCAR-TзїЖиГЮзЪДзФЯдЇІињЗз®ЛпЉМдї•жПРйЂШCAR-Tж≤їзЦЧзЪДзЦЧжХИеТМеЃЙеЕ®жАІгАВ вС°CAR-TеЫЮиЊУеРОжМБдєЕжАІж£АжµЛ FDAеїЇиЃЃзЫСжµЛеРЂжЬЙжХіеРИиљђеЯЇеЫ†зЪДCAR – TзїЖиГЮзЪДжМБдєЕжАІгАВеЄЄзФ®жЦєж≥Хе¶ВпЉЪдљњзФ®жµБеЉПзЪДCARи°®иЊЊж£АжµЛпЉМеЯЇдЇОPCRзЪДиљљдљУжЛЈиіЭжХ∞ж£АжµЛпЉМеЯЇдЇОNGSзЪДжХіеРИдљНзВєеИЖжЮРпЉМињЩдЇЫжЦєж≥ХиЩљзДґеПѓдї•жПРдЊЫеПѓйЭ†еТМеПѓйЗНе§НзЪДжХ∞жНЃдї•з°ЃдњЭзїУжЮЬзЪДеЗЖз°ЃжАІпЉМдљЖTCRжµЛеЇПжЦєж≥ХзЫЄжѓФињЩдЇЫпЉМеПѓдї•дЄНеПЧйЩРдЇОжіїзїЖиГЮпЉМж£АжµЛзЪДзБµжХПеЇ¶и¶БжЫійЂШпЉМиГљеЃЪйЗПж£АжµЛеИ∞еЈ•з®ЛеМЦзЪДTзїЖиГЮеЕЛйЪЖгАВ
TCRжµЛеЇПеПѓзФ®дЇОеѓєCAR-Tж≤їзЦЧеРОжВ£иАЕзЪДе§ЦеС®и°АеТМй™®йЂУж†ЈжЬђињЫи°Мж£АжµЛпЉМдї•иѓДдЉ∞CAR-TзїЖиГЮеЬ®дљУеЖЕзЪДжМБдєЕжАІеТМжЙ©еҐЮжГЕеЖµпЉИAlyssa, S. et al.пЉЙгАВ
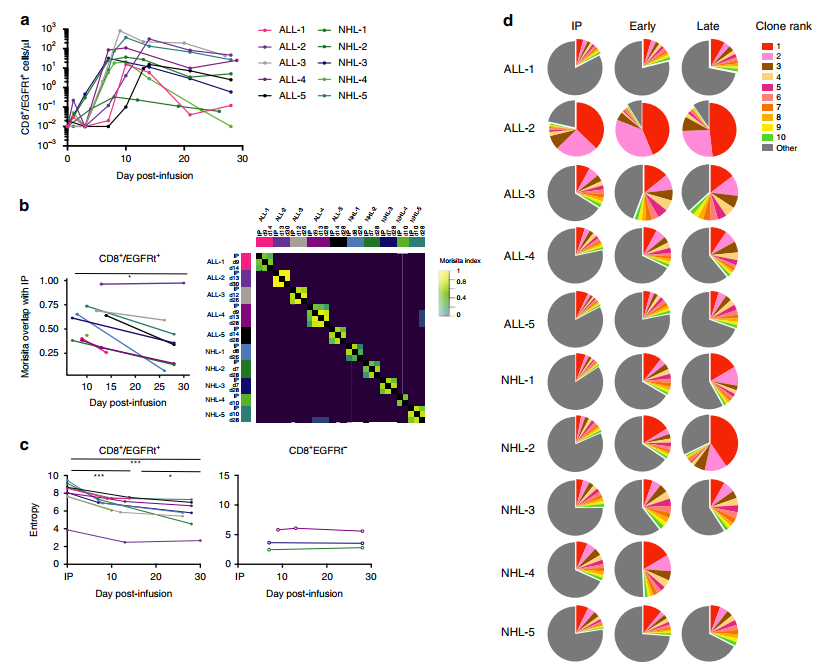
еЕЈдљУжЭ•иѓіпЉМйАЪињЗеѓєжВ£иАЕе§ЦеС®и°АеТМй™®йЂУдЄ≠TзїЖиГЮзЪДTCRињЫи°МжµЛеЇПпЉМеПѓдї•йЙіеЃЪеЗЇCAR-TзїЖиГЮзЪДTCRеЇПеИЧпЉМеєґињЫи°МеЃЪйЗПеИЖжЮРпЉМдї•з°ЃеЃЪCAR-TзїЖиГЮзЪДжЙ©еҐЮеТМзФЯе≠ШжГЕеЖµгАВж≠§е§ЦпЉМTCRжµЛеЇПеПѓдї•еПСзО∞ж≤їзЦЧеРОеЗЇзО∞зЪДжЦ∞зЪДTзїЖиГЮеЕЛйЪЖжИЦиАЕеЕЛйЪЖзїДжИРзЪДеПШеМЦпЉМињЩдЇЫеПШеМЦеПѓиГљдЄОж≤їзЦЧзЦЧжХИгАБзЦЊзЧЕе§НеПСеТМйҐДеРОеѓЖеИЗзЫЄеЕ≥гАВ ¬† жХ∞жНЃе±Хз§Ї¬†¬† Fig.Clonal diversity of CD8+ CAR-T cells decreases after infusion. е¶ВдЄКжХ∞жНЃи°®жШОпЉМCAR-TзїЖиГЮеЬ®дљУеЖЕе≠ШеЬ®е§ЪзІНеЕЛйЪЖпЉМеєґдЄФеЕЛйЪЖзїДжИРеЬ®дЄНеРМжЧґйЧізВєеТМдЄНеРМжВ£иАЕдєЛйЧіе≠ШеЬ®еЈЃеЉВпЉМињЩи°®жШОCAR-TзїЖиГЮеЕЛйЪЖзЪДеК®еКЫе≠¶жШѓе§НжЭВзЪДпЉМеПѓиГљдЄОжВ£иАЕзЪДдЄ™дљУеЈЃеЉВгАБж≤їзЦЧжЦєж°ИеТМCAR-TзїЖиГЮзЪДиі®йЗПз≠ЙеЫ†зі†жЬЙеЕ≥гАВ
еЬ®CAR-Tж≤їзЦЧеРОзЪДжЧ©жЬЯйШґжЃµпЉМCAR-TзїЖиГЮзЪДжЙ©еҐЮйАЯеЇ¶еЊИењЂпЉМдљЖжШѓеЬ®ж≤їзЦЧеРОзЪДеРОжЬЯйШґжЃµпЉМCAR-TзїЖиГЮзЪДжЙ©еҐЮйАЯеЇ¶йАРжЄРеЗПжЕҐпЉМеєґдЄФеЕЛйЪЖзїДжИРеЉАеІЛеПСзФЯеПШеМЦгАВ
еЬ®CAR-Tж≤їзЦЧеРОзЪДдЄНеРМжЧґйЧізВєпЉМCAR-TзїЖиГЮеЕЛйЪЖзЪДе§Ъж†ЈжАІеТМеЭЗеМАжАІе≠ШеЬ®еЈЃеЉВгАВеЬ®ж≤їзЦЧеРОзЪДжЧ©жЬЯйШґжЃµпЉМCAR-TзїЖиГЮеЕЛйЪЖзЪДе§Ъж†ЈжАІеТМеЭЗеМАжАІиЊГйЂШпЉМдљЖжШѓеЬ®ж≤їзЦЧеРОзЪДеРОжЬЯйШґжЃµпЉМCAR-TзїЖиГЮеЕЛйЪЖзЪДе§Ъж†ЈжАІеТМеЭЗеМАжАІйАРжЄРйЩНдљОгАВ
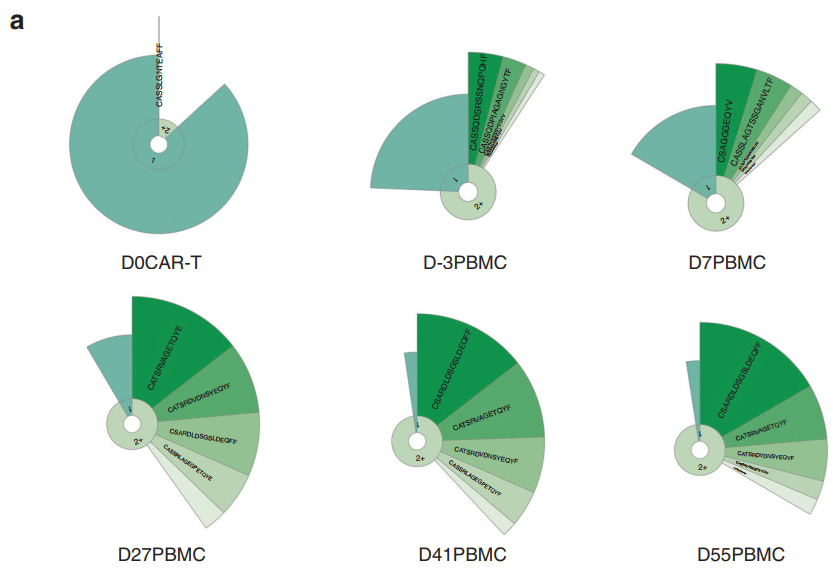
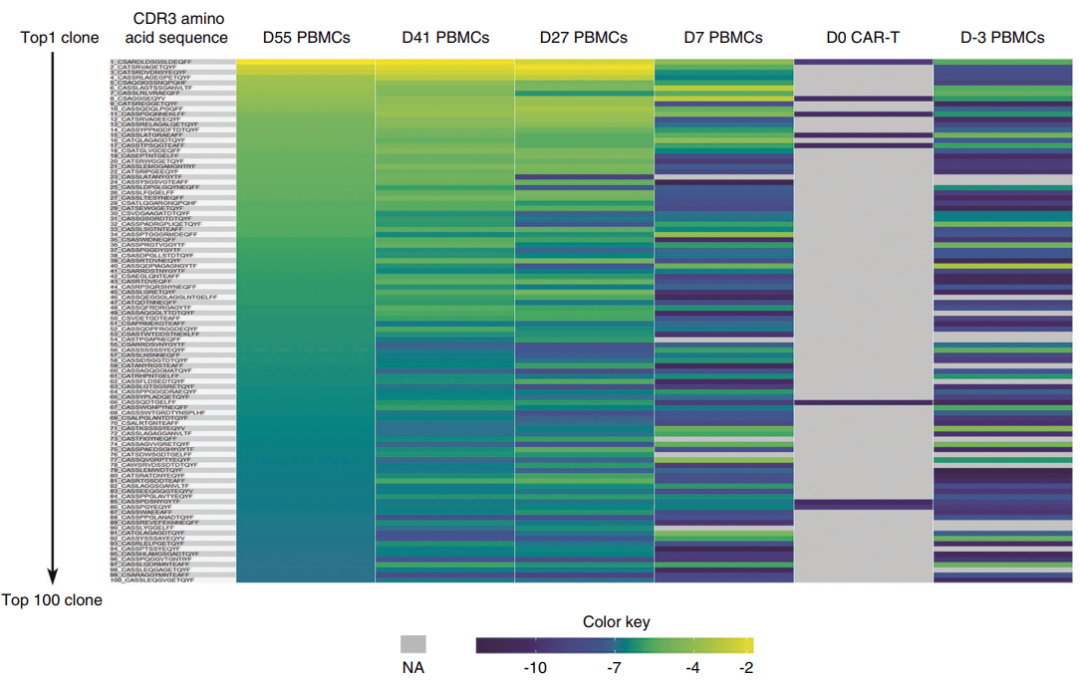
2гАБImmun-Traq¬Ѓ иѓДдЉ∞CAR-TиЊУж≥®еЙНеРОзЪДж≤їзЦЧжХИжЮЬ Immun-Traq¬ЃжШѓеЯЇдЇОиЙЊж≤РиТљиЗ™дЄїз†ФеПСзЪДдЄУеИ©жКАжЬѓImmuhub¬Ѓеє≥еП∞TCR NGSжКАжЬѓжЭ•еК®жАБзЫСжµЛињљиЄ™жВ£иАЕж≤їзЦЧеЙНеТМеРОзЪДTCRе§Ъж†ЈжАІеТМеЕЛйЪЖжАІжГЕеЖµпЉМињЫиАМеѓєеЕНзЦЂз≥їзїЯзКґеЖµињЫи°МиѓДдЉ∞пЉМдї•еПКйҐДжµЛеТМиѓДдЉ∞ж≤їзЦЧжХИжЮЬгАВ ¬† жХ∞жНЃе±Хз§Ї¬†¬† Fig. Clonal proliferation of T cells was detected post-infusion. a A¬†representative donut chart of the blood sample from patient 2 displays¬†the clonal expansion after CAR-T transfer. Fig. The exclusive treatment-related T cell clones originated from pre-treatment autologous non-CAR T cell pool in peripheral blood.¬† The representative graph of clone-tracking heat map from patient 2. иЙЊж≤РиТљйАЪињЗTCRжµЛеЇПеѓєдЄ≠еЫљB-ALLжВ£иАЕCAR-Tж≤їзЦЧеЙНеТМж≤їзЦЧеРОе§ЪдЄ™жЧґйЧізВєзЪДе§ЦеС®и°АеТМй™®йЂУж†ЈжЬђињЫи°Мз†Фз©ґпЉИWang X. et al.пЉЙгАВ
з†Фз©ґзїУжЮЬи°®жШОпЉМCAR-TзїЖиГЮзЦЧж≥ХеѓєTCRзЪДеЕЛйЪЖжАІеТМе§Ъж†ЈжАІжЬЙеЈ®е§Іељ±еУНпЉМж≤їзЦЧеРОдЉЪеЗЇзО∞жШОжШЊзЪДTзїЖиГЮеЕЛйЪЖжАІеҐЮжЃЦпЉМжПРз§ЇCAR-TзїЖиГЮеѓєиВњзШ§зЪДжЭАдЉ§дЉЪдљњжЫіе§ЪзЪДзЩМзїЖиГЮжКЧеОЯйЗКжФЊпЉМеПѓдї•дњГињЫиВњзШ§жКЧеОЯзЙєеЉВжАІTзїЖиГЮзЪДеЕЛйЪЖжАІеҐЮжЃЦгАВзїУжЮЬеПСзО∞жВ£иАЕиВњзШ§жКЧеОЯзЙєеЉВжАІTзїЖиГЮжЭ•иЗ™жВ£иАЕиЗ™иЇЂдљУеЖЕпЉМиАМйЭЮжЭ•иЗ™CAR-TзїЖиГЮгАВжПРз§ЇCAR-TеЫЮиЊУеРОпЉМеѓєиВњзШ§жЭАдЉ§еЉХиµЈзЩМзїЖиГЮжКЧеОЯйЗКжФЊпЉМеЉХиµЈдљУеЖЕиВњзШ§жКЧеОЯзЙєеЉВжАІTзїЖиГЮзЪДеҐЮжЃЦпЉМдїОиАМиµЈеИ∞жЫіе§ІзЪДиВњзШ§зїЖиГЮжЭАдЉ§жХИеЇФгАВ
жЦЗзЂ†жП≠з§ЇдЇЖCAR-TзЦЧж≥ХеПѓдї•дњГињЫиВњзШ§жКЧеОЯзЙєеЉВжАІTзїЖиГЮзЪДеҐЮжЃЦпЉМеєґдЄФињЩдЇЫTзїЖиГЮеЕЛйЪЖзЪДеЗЇзО∞жШѓйЪПзЭАзЩМзїЖиГЮзЪДеЗЛдЇ°иАМеЗЇзО∞зЪДпЉМжПРз§ЇеЃГдїђжЬАеПѓиГљжШѓиВњзШ§жКЧеОЯзЙєеЉВжАІзЪДTзїЖиГЮгАВ
иЙЊж≤РиТљзФЯзЙ©иЗ™дЄїеЉАеПСзЪДImmun-Traq¬ЃжКАжЬѓеє≥еП∞еЬ®еЃЮй™МдЄ≠иѓБеЃЮиГљйАЪињЗзЫСжµЛTзїЖиГЮдї•еПКеИЖжЮРжВ£иАЕдЄ™дљУзЪДжХідљУеЕНзЦЂеКЯиГљзЙєеЊБпЉМжЭ•иѓДдЉ∞CAR-Tж≤їзЦЧжХИжЮЬпЉМдїОиАМжЫіе•љеЬ∞еИЖжЮРжВ£иАЕеѓєдЇОзЩМзЧЗеЕНзЦЂзЦЧж≥ХзЪДж≤їзЦЧеПНеЇФпЉМжПРжЧ©йҐДжµЛеМЕжЛђзїЖиГЮеЕНзЦЂзЦЧж≥ХеЬ®еЖЕзЪДжКЧзЩМеЕНзЦЂзЦЧжХИгАВ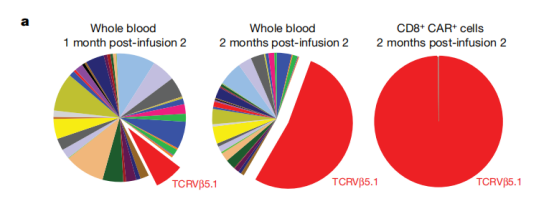
дЄЙгАБSeq-MRD¬ЃжКАжЬѓиГљињљиЄ™CAR-Tж≤їзЦЧеРОзЪДMRDж∞іеє≥ зЫЃеЙНпЉМCAR-Tж≤їзЦЧеЈ≤жШЊз§ЇеЗЇиЙѓе•љзЪДзЦЧжХИпЉМзДґиАМCAR-TзїЖиГЮж≤їзЦЧеРОдїНзДґе≠ШеЬ®йЂШе§НеПСзОЗпЉМдЉ†зїЯжКАжЬѓзЪДеЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙзЫСжµЛжЧ†ж≥ХеЗЖз°ЃйЗПеМЦзЦЊзЧЕиіЯжЛЕпЉМдєЯжЧ†ж≥ХињЫи°МйЂШзБµжХПеЇ¶зЪДжЈ±еЇ¶зЫСжµЛгАВе∞§еЕґCAR-Tж≤їзЦЧеИЭжЬЯиГљдЄЇжВ£иАЕеЄ¶жЭ•жЈ±еЇ¶зЉУиІ£пЉМдљЖжµБйЩРдЇОжµБеЉПзїЖиГЮжЬѓ (FC) зБµжХПеЇ¶пЉМжЧ†ж≥Хж£АжµЛеИ∞MRDеЬ®10-4дї•дЄЛжШѓеР¶дїНзДґе≠ШеЬ®иВњзШ§еЕЛйЪЖпЉМињЩе∞±йЬАи¶БжЫійЂШзЪДзБµжХПеЇ¶жЦєж≥ХињЫи°Мж£АжµЛпЉМињЫиАМдЄЇжМЗеѓЉдЄіеЇКеє≤йҐДж≤їзЦЧеПВиАГгАВ
Seq-MRD¬ЃеЯЇдЇОNGSеє≥еП∞пЉМйАЪињЗзЙєеЉВжАІж£АжµЛTжИЦBжЈЛеЈізїЖиГЮзЪДTзїЖиГЮеПЧдљУпЉИTCRпЉЙTRB/TRGеЯЇеЫ†жИЦBзїЖиГЮеПЧдљУпЉИBCRпЉЙIgH/K/LеЯЇеЫ†зЪДCDR3еМЇеЯЯеЇПеИЧпЉМз≠ЫйАЙеЗЇжВ£иАЕдљУеЖЕиВњзШ§зїЖиГЮжШЊиСЧиАМзЙєеЉВжАІзЪДеЕЛйЪЖйЗНжОТ嚥еЉПпЉМеПѓеЬ®ж≤їзЦЧеРОеѓєињЩдЇЫиВњзШ§зїЖиГЮињЫи°МиЈЯиЄ™пЉМеН≥ињЫи°МMRDзЪДж£АжµЛпЉМдїОиАМдЄЇзЩМзЧЗеєЄе≠ШиАЕеРОзї≠ж≤їзЦЧжЦєж°ИжПРдЊЫеПВиАГгАВ
Seq-MRD¬Ѓж£АжµЛдЉШеКње¶ВдЄЛпЉЪ [1]зБµжХПеЇ¶йЂШиЊЊ10-6 [2]зЙєеЉВжАІйЂШпЉМеПѓйБњеЕНзФ±жЦ∞зЪДжКЧдљУйЭґеРСж≤їзЦЧжЦєеЉПеТМзЩМзїЖиГЮз™БеПШжЙАеЉХиµЈзЪДж£АжµЛиѓѓеЈЃ [3]ињљиЄ™жЦ∞еЕЛйЪЖеПСзО∞еЕЛйЪЖжЉФеПШпЉМзїЩдЇИжВ£иАЕжЫіеПѓйЭ†зЪДж£АжµЛзїУжЮЬ [4]еҐЮеК†еѓєCLL/SLLзЪДIGHVз™БеПШж£АжµЛзЪДSeq-SHM¬ЃеКЯиГљ
жХ∞жНЃи°®жШОпЉМFCж£АжµЛжЙАжЬЙжВ£иАЕзЪД¬†MRDзїУжЮЬеЭЗдЄЇйШіжАІпЉМиАМSeq-MRD¬ЃиГљж£АжµЛеИ∞CAR-Tж≤їзЦЧеРОMRD ж∞іеє≥ > 0.01%жВ£иАЕзЪД LFS еТМ OS еЭЗдљОдЇОMRD пЉЬ 0.01% зЪДжВ£иАЕгАВиѓіжШОSeq-MRD¬ЃзЫЄжѓФFCпЉМжЫійАВеРИеЇФзФ®дЇОCAR-Tж≤їзЦЧзЪДMRDж£АжµЛпЉМиГљжЫіеЗЖз°ЃйҐДжµЛжВ£иАЕйҐДеРОпЉИFigure b&cпЉЙгАВ
зїУжЮЬи°®жШОпЉМзїПињЗCAR-Tж≤їзЦЧеРОзЪДMRDж∞іеє≥иЊГдљОпЉМFCдЄНжШУж£АжµЛеИ∞гАВиАМSeq-MRD¬ЃиГљжМБзї≠еК®жАБзЫСжµЛеИ∞CAR-TиЊУж≥®еРОзЪДMRDж∞іеє≥еПШеМЦпЉМж†єжНЃSeq-MRD¬ЃзїУжЮЬжПРз§ЇдЄіеЇКеПѓдї•ињЫи°МжЧ©жЬЯеє≤йҐДгАВ еЫЫгАБж£АжµЛжµБз®Л еѓєдЇОCAR-Tж≤їзЦЧеРОзЪДCAR-TжМБдєЕжАІиѓДдЉ∞пЉМж≤їзЦЧеРОжХИжЮЬиѓДдЉ∞пЉМеЕНзЦЂйЗНеїЇж∞іеє≥зЪДзЫСжОІйЭЮеЄЄйЗНи¶БгАВ ¬† иЙЊж≤РиТљзїУеРИиЗ™иЇЂдЇІеУБпЉМеМЕжЛђSeq-MRD¬ЃпЉМImmun-Traq¬ЃпЉМеТМImmuHub¬ЃзЪДжКАжЬѓдЉШеКњпЉМжХіеРИдЇЖдЄАе•ЧдЄУдЄЇCAR-TзЪДз†ФеПСеТМзЫСжОІзЪДдЉійЪПиІ£еЖ≥жЦєж°ИгАВ ¬† CAR-Tз†ФеПСеТМдЉійЪПзЫСжОІиІ£еЖ≥жЦєж°Иж£АжµЛжµБз®Л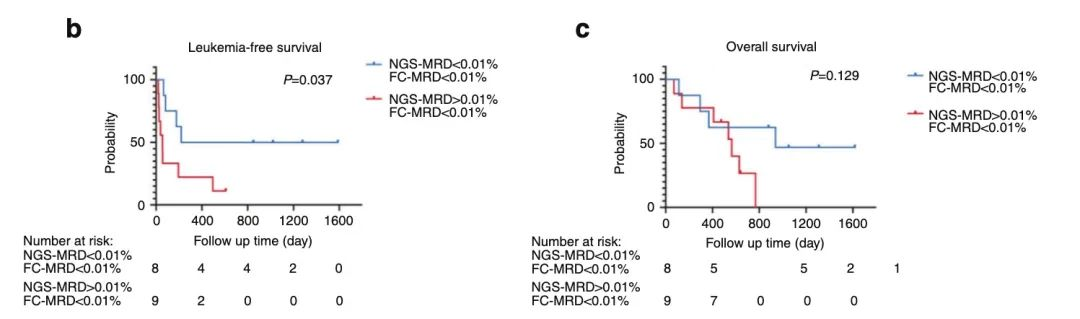

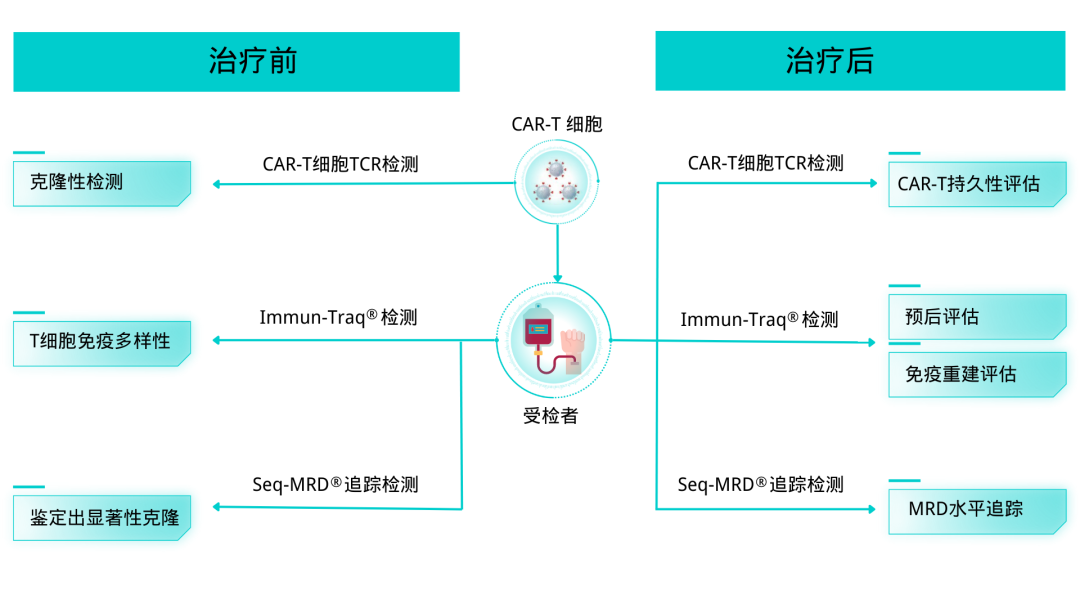
еЬ®CAR-Tз†ФеПСдЄ≠пЉМжЬђиІ£еЖ≥жЦєж°ИеПѓдї•зФ®жЭ•ж£АжµЛCAR-TзїЖиГЮзЪДеЕЛйЪЖжАІеТМжМБдєЕжАІпЉМеПѓдї•еЄЃеК©дЉШеМЦCAR-Tж≤їзЦЧзЪДиЃЊиЃ°еТМдЉШеМЦCAR-TзїЖиГЮзЪДзФЯдЇІињЗз®ЛпЉМдї•жПРйЂШCAR-Tж≤їзЦЧзЪДзЦЧжХИеТМеЃЙеЕ®жАІпЉЫеРМжЧґйАЪињЗSeq-MRD¬Ѓж£АжµЛиѓДдЉ∞CAR-Tж≤їзЦЧеРОMRDж∞іеє≥пЉМеЄЃеК©з†Фз©ґдЇЇеСШиѓДдЉ∞CAR-TзЦЧжХИпЉМеєґдЄФеЬ®ж≤їзЦЧеРОзЪДйЪПиЃњињЗз®ЛдЄ≠иѓДдЉ∞еЕНзЦЂз≥їзїЯзЪДйЗНеїЇжГЕеЖµпЉЫеєґеПѓдї•еК®жАБињљиЄ™CAR-TжМБдєЕжАІжГЕеЖµпЉМеПѓдї•еЄЃеК©з†Фз©ґдЇЇеСШдЇЖиІ£зЦЧж≥ХзЪДжХИжЮЬпЉМжЫіе•љеЬ∞иѓДдЉ∞зЦЧжХИпЉМеєґжЬЙжХИеЬ∞зЫСжОІж≤їзЦЧеРОзЪДжГЕеЖµгАВ дЇФгАБйАБж£Аи¶Бж±В


Immun-Traq¬ЃйГ®еИЖеПВиАГжЦЗзМЃ: [1]Wang, X. et al. Quantitative characterization of T-cell repertoire alteration in Chinese patients with B-cell acute lymphocyte leukemia after CAR-T therapy. Bone Marrow Transplantation (2019). https://www.nature.com/articles/s41409-019-0625-y
Seq-MRD¬ЃйГ®еИЖеПВиАГжЦЗзМЃ: [1]Huang, Y. et al. Predictive value of next-generation sequencing-based minimal residual disease after CAR-T cell therapy. BMT (2022).¬†https://www.nature.com/articles/s41409-022-01699-2
ImmuHub¬ЃжКАжЬѓеє≥еП∞еПВиАГжЦЗзМЃ:
еЕґеЃГйГ®еИЖеПВиАГжЦЗзМЃ: [1]Joseph, F. et al. Disruption of TET2 promotes the therapeutic efficacy of CD19-targeted T cells.Nature(2018). https://www.nature.com/articles/s41586-018-0178-z [2]Alyssa, S. et al. Clonal kinetics and single-cell transcriptional profiling of CAR-T cells in patients undergoing CD19 CAR-T immunotherapy.¬†Naturecommunications(2020). https://www.nature.com/articles/s41467-019-13880-1

