еЊЃе∞ПжЃЛзХЩзЧЕMRDпЉИMinimal/Measurable Residual DiseaseпЉЙзЪДж¶ВењµжЇРиЗ™дЇОи°Ажґ≤иВњзШ§пЉМжШѓжМЗиВњзШ§жВ£иАЕзїПињЗж≤їзЦЧеРОдљУеЖЕжЃЛзХЩе∞СйЗПзЩМзїЖиГЮзЪДзКґжАБгАВжЃЛзХЩзЪДе∞СйЗПзЩМзїЖиГЮеПѓиГљжЪВжЧґж≤°жЬЙеЉХиµЈдїїдљХдљУеЊБжИЦзЧЗзКґпЉМдљЖеЃГдїђеПѓиГљеѓЉиЗіжЬ™жЭ•иВњзШ§зЪДињЫе±ХжИЦе§НеПСиљђзІїгАВеЫ†ж≠§MRDж∞іеє≥зЪДзЫСжµЛеНБеИЖйЗНи¶БпЉМеЃГеПѓдї•жФєеЦДеН±йЩ©еЇ¶еИЖе±ВгАБиѓДдЉ∞ж≤їзЦЧжХИжЮЬгАБзЫСжµЛе§НеПСгАБйҐДжµЛйҐДеРОз≠ЙпЉМ襀зЇ≥еЕ•еРДдЄ™и°Ажґ≤иВњзШ§иѓКзЦЧжМЗеНЧдЄ≠гАВ
MRDж£АжµЛжЙЛжЃµзїПињЗжХ∞еНБеєізЪДеПСе±ХпЉМзБµжХПеЇ¶дЄНжЦ≠еНЗзЇІгАВзБµжХПеЇ¶иґКйЂШпЉМиґКиГљж£АжµЛеИ∞жЈ±е±Вжђ°зЪДMRDпЉМдЄОйҐДеРОзЫЄеЕ≥жАІдєЯиґКйЂШгАВеЫ†ж≠§йЂШзБµжХПеЇ¶зЪДдЇМдї£жµЛеЇПпЉИNGSпЉЙMRDж£АжµЛжКАжЬѓеЊЧеИ∞иґКжЭ•иґКеєњж≥ЫзЪДеЇФзФ®гАВжЬђжЦЗе∞ЖдЄЇе§ІеЃґиѓ¶зїЖдїЛзїНи°Ажґ≤иВњзШ§NGS MRDж£АжµЛжКАжЬѓпЉМеєґйТИеѓєдЄіеЇКеЇФзФ®дЄ≠зЪДеЄЄиІБйЧЃйҐШињЫи°МиІ£з≠ФгАВ
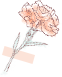

зЫЃеЙНдЄїжµБзЪДMRDж£АжµЛжЦєж≥ХдЄїи¶БжЬЙMFCгАБBCR::ABL1ж£АжµЛгАБдЇМдї£жµБеЉПпЉИNGFпЉЙгАБеЃЮжЧґеЃЪйЗПPCRпЉИASO-PCRпЉЙгАБIG/TRеЯЇеЫ†йЗНжОТзЪДNGSж£АжµЛз≠ЙгАВжѓПзІНж£АжµЛжЦєж≥ХеРДжЬЙеЕґдЉШзЉЇзВєпЉМеЕЈдљУиІБдЄЛи°®пЉМеПѓж†єжНЃйЬАи¶БйАЙжЛ©еРИйАВзЪДжЦєж≥ХпЉМдєЯеПѓе§ЪзІНж£АжµЛжЦєж≥ХзїЉеРИиѓДдЉ∞MRDзКґжАБгАВ
дЄАзѓЗеПСи°®дЇОblood advancesдЄКзЪДзЊОеЫљдЄУеЃґе∞ПзїДеЕ±иѓЖ[1]пЉИеПѓзВєеЗїйУЊжО•жЯ•зЬЛиѓ¶зїЖиІ£иѓїпЉЙйЗМеїЇиЃЃпЉЪеѓєдЇОB-ALLжВ£иАЕпЉМеЯЇдЇОNGSзЪДзЩљи°АзЧЕзЙєеЉВжАІIG/TRеЕЛйЪЖеЮЛMRDеЃЪйЗПжШѓдЄіеЇКеЖ≥з≠ЦзЪДй¶ЦйАЙпЉМеЫ†дЄЇиѓ•жЦєж≥ХжѓФеЕґдїЦж£АжµЛеЕЈжЬЙжЫійЂШзЪДзБµжХПеЇ¶еТМеѓєе§НеПСзЪДйЙіеИЂеКЫгАВеѓєдЇОTпЉНALLжВ£иАЕпЉМIG/TRзЪДNGSж£АжµЛеТМеЕґдїЦMRDж£АжµЛжШѓMRDиѓДдЉ∞зЪДи°•еЕЕжЦєж≥ХгАВ

жЈЛз≥їи°Ажґ≤иВњзШ§жШѓT/BжЈЛеЈізїЖиГЮеПСзФЯзЩМеПШиАМеѓЉиЗіпЉМељУT/BжЈЛеЈізїЖиГЮеПСзФЯзЩМеПШжЧґпЉМдЉЪе§ІйЗПе§НеИґеҐЮжЃЦгАВиАМеЕґи°®йЭҐзЪДзФЯзЙ©ж†ЗењЧзЙ©TCR/BCRжШѓдЄНеПСзФЯжФєеПШзЪДпЉМйАЪињЗйЂШйАЪйЗПжµЛеЇПжЙЊеИ∞ињЩдЇЫеЗЇзО∞йҐСзОЗеЊИйЂШзЪДзЩМзїЖиГЮеПЧдљУVDJеЯЇеЫ†еЇПеИЧпЉМеЬ®ж≤їзЦЧеРОеѓєж≠§еЯЇеЫ†еЇПеИЧињЫи°МињљиЄ™пЉМжЯ•жЙЊеЕґеЕЛйЪЖжГЕеЖµпЉМеЊЧеИ∞MRDеАЉгАВ
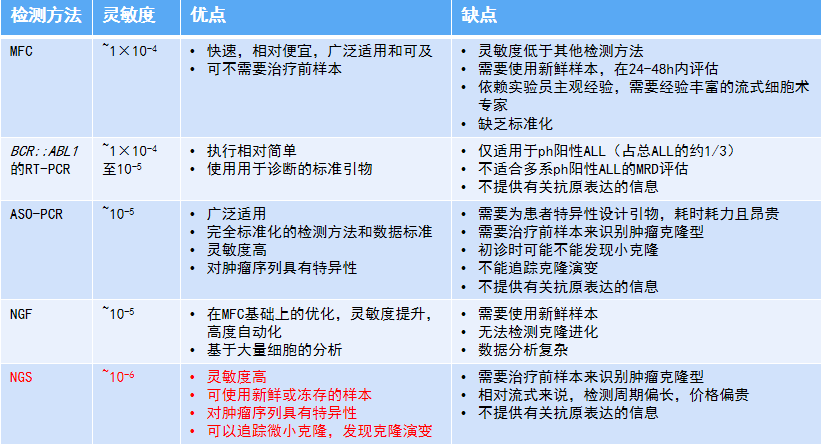
еЫЊ1
ињЩдЄНеРМдЇОеЯЇеЫ†з™БеПШж£АжµЛз≠ЙеЕґеЃГеЯЇеЫ†жµЛеЇПпЉМеЯЇеЫ†з™БеПШж£АжµЛжШѓеИЖжЮРDNAжЮДи±°жИЦиІ£йУЊзЙєжАІпЉМжИЦиАЕеИ©зФ®DNAеПШжАІеТМе§НжАІз≠ЙзЙєжАІпЉМињЫи°МDNAз™БеПШзЪДеИЖжЮРпЉМдєЯе∞±жШѓйАЪињЗдЄАдЇЫеЯЇеЫ†з™БеПШдњ°жБѓжЭ•йЙіеЃЪзЩМзїЖиГЮгАВиАМNGS MRDжШѓеЯЇдЇОжµЛеИ∞зЪДеПѓеПШеМЇеЇПеИЧ( еЕЛйЪЖ)йҐСзОЗйЂШдљОжЭ•йЙіеЃЪзЩМзїЖиГЮпЉМдЄ§иАЕж£АжµЛеОЯзРЖдЄНеРМгАВеН≥дЊњзЩМзїЖиГЮDNAеПСзФЯдЇЖз™БеПШпЉМTCR/BCRйАЪеЄЄжШѓз®≥еЃЪдЄНеПШзЪДпЉМдЊЭзДґеПѓдї•ињЫи°МињљиЄ™гАВ

жЬЙеИЂдЇОMFCгАБNGFгАБBCR::ABL1ж£АжµЛзЪДжШѓпЉМNGS MRDж£АжµЛењЕй°їеЊЧжЬЙж≤їзЦЧеЙНж†ЈжЬђињЫи°МеЯЇзЇњж£АжµЛпЉМйЙіеЃЪеЗЇзЩМзїЖиГЮеЕЛйЪЖеЇПеИЧдєЛеРОпЉМжЙНиГљињЫи°Мж≤їзЦЧеРОзЪДзЩМзїЖиГЮеЕЛйЪЖињљиЄ™пЉМиѓДдЉ∞MRDж∞іеє≥гАВйЬАи¶Бж≥®жДПзЪДжШѓпЉМељУж≤°жЬЙеПѓзФ®зЪДеИЭиѓКж†ЈжЬђжЧґпЉМдЄНеїЇиЃЃзФ®ж≤їзЦЧеРОж†ЈжЬђдї£жЫњињЫи°МеЯЇзЇњж£АжµЛпЉМеЫ†дЄЇйЙіеЃЪдЄНеЗЇеПѓдЊЫињљиЄ™зЪДзЩМзїЖиГЮеЕЛйЪЖзЪДй£ОйЩ©жѓФиЊГйЂШпЉМдЄФж≤їзЦЧеРОзЪДжШЊиСЧжАІеЕЛйЪЖдЄНдЄАеЃЪжЭ•иЗ™зЩМзїЖиГЮпЉМдєЯеПѓиГљжШѓеЇФжњАеПНеЇФжАІеЕЛйЪЖгАВ
еЯЇзЇњж£АжµЛдєЛеРОзЪДMRDж£АжµЛжЧґжЬЇеТМйҐСзОЗеПѓж†єжНЃжВ£иАЕзЧЕжГЕеПШеМЦеТМж≤їзЦЧжГЕеЖµеЖ≥еЃЪпЉМдєЯеПѓеПВиАГеРДиѓКзЦЧжМЗеНЧдЄ≠еЕ≥дЇОMRDж£АжµЛжЧґжЬЇзЪДеїЇиЃЃпЉИиѓ¶иІБвАЬеП≤дЄКжЬАеЕ®жЈЛз≥їи°Ажґ≤иВњзШ§MRDж£АжµЛжЧґжЬЇжАїзїУвАЭпЉЙпЉМдЄАиИђжШѓеРДдЄ™ж≤їзЦЧйШґжЃµзїУжЭЯеРОињЫи°МMRDж£АжµЛпЉМзїіжМБж≤їзЦЧжЬЯеТМйЪПиЃњжЬЯйЧіж†єжНЃзЦЊзЧЕзЉУиІ£жГЕеЖµеИґеЃЪMRDзЫСжµЛжЦєж°ИпЉМиЛ•ињЮзї≠е§Ъжђ°зїУжЮЬдЄЇйШіжАІпЉМж£АжµЛйЧійЪФжЧґйЧіеПѓйАРжЄРеїґйХњгАВ
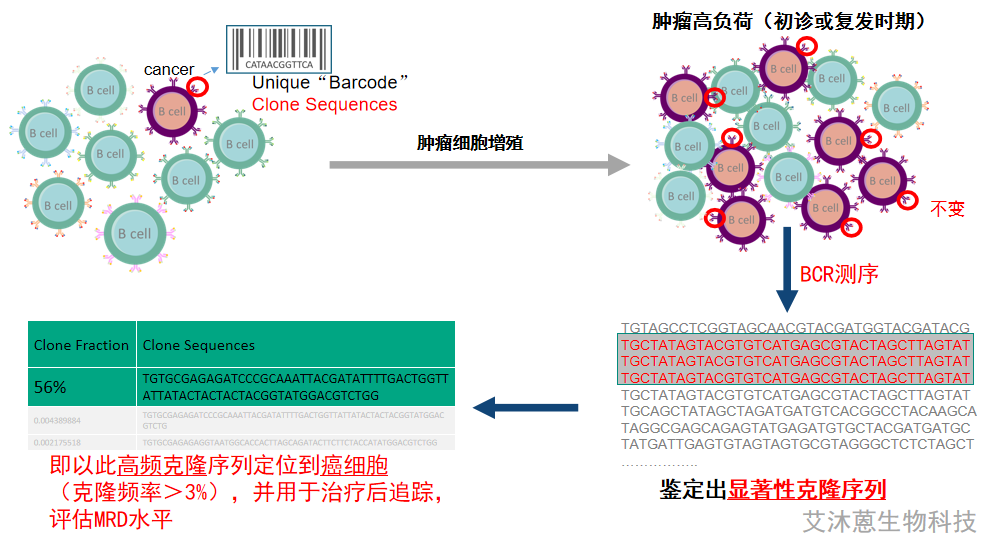
еЫЊ2

еѓєдЇОжЈЛз≥їзЩљи°АзЧЕеТМе§ЪеПСжАІй™®йЂУзШ§пЉИMMпЉЙжЭ•иѓіпЉМй¶ЦеЕИжЦ∞й≤Ьй™®йЂУпЉИBMпЉЙж†ЈжЬђињЫи°МMRDж£АжµЛпЉМдљЖе§ЦеС®и°АпЉИPBпЉЙзЪДMRDзЫСжµЛеЕЈжЬЙйБњеЕНйҐСзєБдЊµеЕ•жАІй™®йЂУйЗЗж†ЈзЪДдЉШзВєгАВжЬЙз†Фз©ґиѓБжШОдЇЖеЯЇдЇОPBеТМBMзЪДNGS MRDж£АжµЛзїУжЮЬеЕЈжЬЙеЊИеЉЇзЪДзЫЄеЕ≥жАІгАВдљЖжШѓPBдЄ≠зЪДзЦЊзЧЕиіЯжЛЕеПѓиГљжѓФBMдљО1еИ∞2дЄ™еѓєжХ∞еАНпЉМеЫ†ж≠§PBзЫСжµЛеПѓиГљжЧ†ж≥Хж£АжµЛеИ∞йЭЮеЄЄдљОж∞іеє≥зЪДMRDгАВ
еѓєж≠§пЉМжЬЙдЄУеЃґеїЇиЃЃпЉЪеѓєдЇОBMеПЧзіѓзЪДжВ£иАЕпЉМеїЇиЃЃиЗ≥е∞СеЬ®иЃ∞ељХеИ∞MRDйШіжАІдєЛеЙНзЫСжµЛBM MRDгАВеЬ®дљњзФ®йЂШиі®йЗПBMж†ЈжЬђиЊЊеИ∞MRDйШіжАІеРОпЉМеПѓдї•иАГиЩСињЫи°МPB MRDзЫСжµЛпЉИеНХзЛђжИЦдЄОеЃЪжЬЯBMиѓДдЉ∞дЇ§жЫњпЉЙпЉМжЬАе•љдљњзФ®йЂШзБµжХПеЇ¶зЪДNGS MRDж£АжµЛпЉМдї•еЗПе∞СдЊµеЕ•жАІBMж£АжЯ•зЪДйҐСзОЗ[1]гАВ
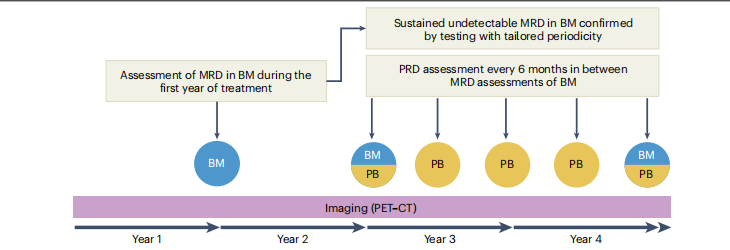
Bruno PaivaжХЩжОИеПСи°®дЇОNature Reviews Clinical OncologyзЪДеЕ≥дЇОMM MRDж£АжµЛзЪДйЗНз£ЕзїЉињ∞пЉИеПѓзВєеЗїйУЊжО•жЯ•зЬЛиѓ¶зїЖиІ£иѓїпЉЙйЗМдєЯжПРеИ∞пЉЪеѓєдЇОеЬ®ж≤їзЦЧеИЭжЬЯеЃЮзО∞MRDйШіжАІзЪДжВ£иАЕпЉМдЄЇдЇЖйБњеЕНеЬ®иЊГзЯ≠жЧґйЧіеЖЕињЫи°Ме§Ъжђ°й™®йЂУз©њеИЇпЉМеїЇиЃЃжѓПдЄ§еєіињЫи°МдЄАжђ°й™®йЂУMRDиѓДдЉ∞еєґзїУеРИжѓП6дЄ™жЬИдЄАжђ°зЪДе§ЦеС®и°АжЃЛзХЩзЧЕпЉИPRDпЉЙиѓДдЉ∞пЉИйАЪињЗMSгАБNGFжИЦNGSпЉЙгАВе¶ВжЮЬPRDжМБзї≠йШіжАІпЉМеИЩеПѓиГљжДПеС≥зЭАMRDдїНе§ДдЇОйШіжАІзКґжАБпЉЫиЛ•PRDеЗЇзО∞еЫЮеНЗпЉМеИЩиЗ™еК®иІЖдЄЇMRDйШіжАІдЄІе§±зЪДж†ЗењЧпЉМжЧ†йЬАеЖНжђ°й™®йЂУз©њеИЇз°ЃиЃ§[2]гАВ
еЫЊ3
йЩ§дЇЖжЦ∞й≤Ьж†ЈжЬђдєЛе§ЦпЉМзїЖиГЮгАБDNAгАБй™®йЂУжґВзЙЗз≠ЙеПѓеВ®е≠Шж†ЈжЬђз±їеЮЛдєЯеПѓзФ®дљЬNGS MRDж£АжµЛпЉМињЩеПѓдї•жї°иґ≥дЄАдЇЫзІСз†ФйЬАж±ВгАВ
gDNAињШжШѓctDNAпЉЯ
еЯЇдЇОIg/TRеЯЇеЫ†еЕЛйЪЖйЗНжОТзЪДNGS MRDж£АжµЛжШѓжПРеПЦж†ЈжЬђдЄ≠зЪДDNAињЫи°Ме§ЪйЗНPCRжЮДеїЇжЦЗеЇУпЉМзДґеРОйЂШйАЪйЗПжµЛеЇПгАВйАЙжЛ©gDNAпЉИgenomic DNAпЉЙињШжШѓctDNAпЉИCirculating Tumor DNAпЉЙжШѓзФ±зЦЊзЧЕз±їеЮЛеЖ≥еЃЪзЪДгАВ
T/Bз≥їзЩљи°АзЧЕгАБе§ЪеПСжАІй™®йЂУзШ§йАЪеЄЄжШѓжПРеПЦй™®йЂУ/е§ЦеС®и°АдЄ≠зЪДgDNAињЫи°Мж£АжµЛгАВиАМеѓєдЇОT/Bз≥їжЈЛеЈізШ§жЭ•иѓіпЉМй™®йЂУеТМе§ЦеС®и°АдЄ≠дЄНдЄАеЃЪжЬЙзЩМзїЖиГЮзіѓеПКпЉМеЕґеИЭиѓКзЪДеЕЛйЪЖжАІж£АжµЛеїЇиЃЃдљњзФ®иВњзШ§зїДзїЗж†ЈжЬђжПРеПЦgDNAињЫи°Мж£АжµЛпЉМMRDињљиЄ™ж£АжµЛпЉИж≤їзЦЧеРОпЉЙйЬАи¶БжПРеПЦе§ЦеС®и°АctDNAпЉИctDNAжШѓиВњзШ§зїЖиГЮDNAзїПиД±иРљжИЦељУзїЖиГЮеЗЛдЇ°еРОйЗКжФЊињЫеЕ•еЊ™зОѓз≥їзїЯзЪДDNAзҐОзЙЗпЉЙињЫи°МжЃЛзХЩж£АжµЛгАВиЛ•жЧ†ж≥ХжПРдЊЫеИЭиѓКзЪДиВњзШ§зїДзїЗж†ЈжЬђпЉМеП™иГљжПРдЊЫй™®йЂУ/е§ЦеС®и°Аж†ЈжЬђзЪДиѓЭпЉМйЬАи¶БдЄіеЇКеМїзФЯз°ЃиЃ§й™®йЂУ/е§ЦеС®и°АдЄ≠жШѓжЬЙзЩМзїЖиГЮзіѓеПКзЪДгАВ
cDNAпЉИcomplementary DNAпЉЙжШѓзФ±RNAйАЖиљђељХиАМжЭ•пЉМдєЯеПѓзФ®дЇОеЕНзЦЂзїДIg/TRжµЛеЇПпЉМе∞§еЕґйАВзФ®дЇОдЄОзЦЊзЧЕжКЧеОЯзЫЄеЕ≥зЪДз†Фз©ґпЉМдљЖдЄНйАВеРИдљЬдЄЇMRDж£АжµЛзЪДж®°жЭњпЉМеОЯеЫ†е¶ВдЄЛпЉЪ
-
зЩМзїЖиГЮеЕЛйЪЖеПѓиГљжШѓеКЯиГљжАІеЇПеИЧпЉМдєЯеПѓиГљжШѓдЄНеПСзФЯRNAиљђељХеТМи°®иЊЊзЪДйЭЮеКЯиГљжАІеЇПеИЧпЉМдљњзФ®RNAйАЖиљђељХзЪДcDNAдљЬдЄЇж®°жЭњжЬЙзЩМзїЖиГЮжЉПж£АзЪДй£ОйЩ©гАВ
-
дЄАдЄ™зїЖиГЮеѓєеЇФе§ЪдЄ™mRNAжЛЈиіЭпЉМиАМеП™еѓєеЇФдЄАдЄ™gDNAжЛЈиіЭпЉМжХЕgDNAжЫійАВеРИзФ®дЇОMRDж£АжµЛдЄ≠ињЫи°МзЩМзїЖиГЮеЃЪйЗПиѓДдЉ∞гАВ


е§ЪеЕЛйЪЖеЮЛжШѓжМЗеИЭиѓКжЬ™ж£АжµЛеИ∞еПѓдЊЫињљиЄ™зЪДжШЊиСЧжАІеЕЛйЪЖпЉМињЩйГ®еИЖжѓФдЊЛе§ІзЇ¶еЬ®4%-9%гАВељУеЯЇзЇњж£АжµЛдЄЇе§ЪеЕЛйЪЖеЮЛжЧґпЉМеПѓдї•дљњзФ®дЄНйЬАи¶БеИЭиѓКж†ЈжЬђзЪДеЕґдїЦMRDиѓДдЉ∞жЫњдї£жЦєж≥ХпЉИе¶ВжµБеЉПз≠ЙпЉЙпЉЫжИЦиАЕиАГиЩСйАБж£АзђђдЇМдЄ™йЂШиі®йЗПж†ЈжЬђињЫи°МйЗНе§НеЯЇзЇњж£АжµЛпЉЫдєЯеПѓдї•иАГиЩСеѓєж≤°жЬЙжШЊиСЧжАІеЕЛйЪЖзЪДB-ALLжВ£иАЕињЫи°МTRеЯЇеЫ†йЗНжОТж£АжµЛпЉМеПѓиГљдЉЪеЬ®жЯРдЇЫжВ£иАЕдЄ≠иѓЖеИЂеЗЇеПѓињљиЄ™зЪДеЇПеИЧгАВ

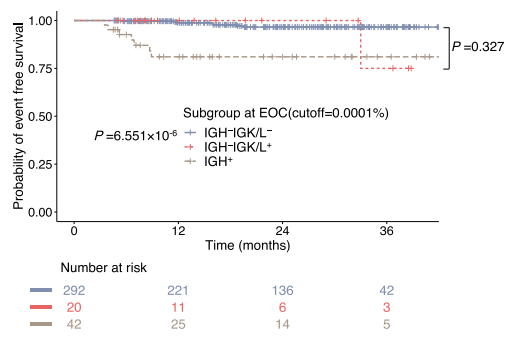
йҐДеРОдїЈеАЉе§Іе∞ПдЄОйУЊзЛђзЙєжАІжЬЙеЕ≥пЉМзЫЃеЙНзЪДз†Фз©ґжШѓиЃ§дЄЇIGHйУЊзЪДзЛђзЙєжАІжЬАйЂШпЉМжѓФеЕґдїЦйУЊжЫіеЕЈжЬЙйҐДеРОжДПдєЙгАВTCRеРДжЭ°йУЊжШѓеР¶е≠ШеЬ®йҐДеРОдїЈеАЉеЈЃеЉВињШжЬЙеЊЕжЫіе§Ъз†Фз©ґгАВ
еЫЊ4

еЬ®ж≤їзЦЧеРОж†ЈжЬђдЄ≠襀йЙіеЃЪеЗЇзЪДжШЊиСЧжАІеЕЛйЪЖ襀зІ∞дЄЇжЦ∞еПСжШЊиСЧжАІеЕЛйЪЖгАВжЦ∞еПСжШЊиСЧжАІеЕЛйЪЖеЬ®еМЦзЦЧгАБжКЧдљУиНѓеТМзІїж§Нз≠Йж≤їзЦЧињЗз®ЛдЄ≠еЭЗеПѓиГљдЉЪеЗЇзО∞гАВеЬ®зЫЃеЙНзЪДз†Фз©ґдЄ≠пЉМе§Іе§ЪжХ∞жЦ∞еЗЇзО∞зЪДжШЊиСЧжАІеЕЛйЪЖеЇПеИЧеПѓиГљдї£и°®дЄОзЦЊзЧЕжЧ†еЕ≥зЪДеЕЛйЪЖжЙ©еҐЮпЉМеєґдЄФеЊАеЊАдЉЪйЪПзЭАжЧґйЧізЪДжО®зІїйААеМЦеИ∞иГМжЩѓеЕЛйЪЖдЄ≠пЉЫиЊГе∞СжГЕеЖµдЄЛдЄАдЇЫжЦ∞еЗЇзО∞зЪДжШЊиСЧжАІеЕЛйЪЖеЇПеИЧеПѓиГљдЄОе§НеПСе≠ШеЬ®еЕ≥иБФгАВеѓєдЇОдЄНз°ЃеЃЪзЪДзЧЕдЊЛпЉМеїЇиЃЃињЫи°МеѓЖеИЗзЪДињЮзї≠MRDзЫСжµЛдї•иІВеѓЯеЇПеИЧзЪДеК®жАБеПШеМЦгАВ

Michael A. PulsipherжХЩжОИ2024еєіеЬ®bloodжЭВењЧеПСи°®жЦЗзЂ†еИЖдЇЂдЇЖеЕґеЬ®еДњзЂ•еТМжИРдЇЇALLжВ£иАЕдЄ≠еЇФзФ®NGS MRDж£АжµЛжМЗеѓЉйА†и°Аеє≤зїЖиГЮзІїж§НпЉИHCTпЉЙж≤їзЦЧзЪДзїПй™МпЉМеѓєдЄіеЇКеЕЈжЬЙеАЯйЙіжДПдєЙгАВиІ£иѓїиѓ¶иІБBlood|еЕ®йЭҐдЄФжЈ±еЇ¶иІ£иѓїе¶ВдљХеИ©зФ®NGS MRDжФєеЦДALLй£ОйЩ©еИЖе±ВеТМйҐДйШ≤е§НеПСгАВ
NGS MRDеЬ®HCTеЙНеРОеЭЗеПѓжПРдЊЫжЬЙдїЈеАЉдњ°жБѓпЉМжМЗеѓЉдЄіеЇКеЖ≥з≠ЦгАВжЬЙз†Фз©ґи°®жШОпЉМеЬ®HCTдєЛеЙНйАЪињЗNGSж£АжµЛеИ∞дїїдљХж∞іеє≥MRDйГљеПѓдї•йҐДжµЛзІїж§НеРОе§НеПСй£ОйЩ©еҐЮеК†еТМзФЯе≠ШжЬЯиЊГеЈЃгАВNGS MRDзїУжЮЬињШеПѓдї•еЬ®дЄАеЃЪз®ЛеЇ¶дЄКжМЗеѓЉзІїж§НйҐДе§ДзРЖгАБзІїж§НзЙ©жКЧеЃњдЄїзЧЕпЉИGVHDпЉЙйҐДйШ≤еТМзІїж§НеРОзїіжМБж≤їзЦЧжЦєж°ИпЉМжѓФе¶ВеѓєдЇОзІїж§НеРОжМБзї≠жИЦжЦ∞еЗЇзО∞NGS MRDйШ≥жАІжВ£иАЕпЉМеЬ®зІїж§НеРОжЧ©жЬЯеЗПе∞СжИЦжТ§йФАеЕНзЦЂжКСеИґдї•иѓ±еѓЉзІїж§НзЙ©жКЧзЩљи°АзЧЕжХИеЇФпЉИGVLпЉЙжШѓдЄАзІНжЬЙдїЈеАЉзЪДз≠ЦзХ•гАВHCTеРОйХњжЬЯзЫСжµЛNGS MRDеПѓдї•дЄЇMRDйШ≥жАІжВ£иАЕжПРжЧ©еПСеЗЇи≠¶жК•пЉМдї•жПРдЊЫжЧ©жЬЯеє≤йҐДзЪДжЬЇдЉЪгАВ

иЙЊж≤РиТљдЄУж≥®дЇОеЕНзЦЂзїДдЇМдї£жµЛеЇПйҐЖеЯЯе§ЪеєіпЉМжШѓеЕ®еЫљй¶ЦеЃґжО®еЗЇи°Ажґ≤иВњзШ§NGS MRDж£АжµЛдЇІеУБSeq-MRD¬ЃзЪДеЕђеПЄгАВSeq-MRD¬ЃйАВзФ®дЇОB/Tз≥їзЩљи°АзЧЕгАБB/Tз≥їжЈЛеЈізШ§гАБе§ЪеПСжАІй™®йЂУзШ§пЉМиГље§ЯеЄЃеК©дЄіеЇКеМїзФЯйҐДжµЛйХњжЬЯзЦЧжХИгАБиѓДдЉ∞ж≤їзЦЧжХИжЮЬгАБзЫСжµЛзЉУиІ£зКґжАБдї•еПКзЫСжµЛжЧ©жЬЯе§НеПСгАВзїПињЗе§ЪеєізЪДзІѓзіѓеТМеПСе±ХпЉМSeq-MRD¬ЃеЬ®дЄіеЇКж£АжµЛеТМзІСе≠¶з†Фз©ґдЄКеЭЗеПЦеЊЧдЄНе∞СжИРжЮЬпЉМеєґиОЈеЊЧеЫљйЩЕеЄВеЬЇиЃ§еПѓгАВ
иОЈеЊЧжђІзЫЯCEиµДиі®иЃ§иѓБ
Seq-MRD¬ЃиОЈеЊЧжђІзЫЯCEиµДиі®пЉИж≥®еЖМеПЈпЉЪDE/CA20/01-IVD-Luxuslebenswelt-190/22пЉЙпЉМиОЈжЙєзЪДжШѓдЇЇжЈЛеЈіBзїЖиГЮеЊЃе∞ПжЃЛзХЩзЧЕеЯЇеЫ†ж£АжµЛиѓХеЙВзЫТпЉИеПѓйАЖжЬЂзЂѓзїИж≠ҐжµЛеЇПж≥ХпЉЙгАВ¬†

иОЈеЊЧдЄЙй°єеПСжШОдЄУеИ©
иЙЊж≤РиТљжО®еЗЇзЪДSeq-MRD¬Ѓи°Ажґ≤зЩМзЧЗMRDж£АжµЛжШѓжЬАжЧ©жЙєеЃЮзО∞еХЖдЄЪеМЦзЪДдЇІеУБпЉМиЗ™2016еєіз†ФеПСдЄУеИ©жКАжЬѓиЗ≥дїКпЉМиЙЊж≤РиТљSeq-MRD¬ЃеЈ≤зїПиОЈеЊЧ3й°єеЫљеЃґеПСжШОдЄУеИ©пЉЪ
[1]вАЬдЄАзІНеЇФзФ®дЇОйЂШйАЪйЗПжµЛеЇПж£АжµЛTзїЖиГЮзЩљи°АзЧЕеЊЃе∞ПжЃЛзХЩзЧЕзЪДеЉХзЙ©зїДеРИеПКиѓХеЙВзЫТвАЭпЉИдЄУ еИ© еПЈ: 2016 11204857.0пЉМжОИжЭГеЕђеСКеПЈ:CN 106957906 BпЉЙ
[2]вАЬдЄАзІНж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕMRDзЪДиѓХеЙВзЫТвАЭпЉИдЄУ еИ© еПЈ: 2018 1 1550133.0пЉМжОИжЭГеЕђеСКеПЈ: CN 109652518 BпЉЙ
[3]вАЬдЄАзІНж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕMRDзЪДжЦєж≥ХвАЭпЉИдЄУ еИ© еПЈ: 2018 1 1549203.0пЉМжОИжЭГеЕђеСКеПЈ: CN 109680062 BпЉЙ

иОЈеЊЧзЫЄеЕ≥иљѓдїґиСЧдљЬ
[1]вАЬеЕНзЦЂзїДеЇУMRDж£АжµЛиЗ™еК®еМЦжК•еСКз≥їзїЯ[зЃАзІ∞ImmuReport] V1.0вАЭпЉИзЩїиЃ∞еПЈпЉЪ2019SR0916207пЉЙ
[2]вАЬSeq-MRDж£АжµЛиЗ™еК®еМЦеИЖжЮРз≥їзїЯпЉИDiscTermiteпЉЙ[зЃАзІ∞пЉЪDiscTermite]0.4.6вАЬпЉИзЩїиЃ∞еПЈпЉЪ2019SR1131517пЉЙ
[3]вАЬеЯЇдЇОеЕНзЦЂзїДеЇУдЇМдї£жµЛеЇПзЪДеЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛжХ∞жНЃе§ДзРЖз≥їзїЯвАЭпЉИзЩїиЃ∞еПЈпЉЪ2020SR0507594пЉЙ

иОЈеЊЧиН£и™ЙиѓБдє¶
1гАБиЙЊж≤РиТљиБФеРИжµЩе§ІйЩДдЄАйїДж≤≥жХЩжОИеЃМжИРзЪДгАКжЦ∞еЮЛCAR-TзїЖиГЮз†ФеПСеПКеЕґж≤їзЦЧжБґжАІи°Ажґ≤зЧЕдЄіеЇКиљђеМЦеИЫжЦ∞дљУз≥їеїЇзЂЛгАЛиОЈ2023еєіеЇ¶жµЩж±ЯзЬБзІСе≠¶жКАжЬѓињЫж≠•е•ЦдЄАз≠Йе•ЦгАВSeq-MRD¬ЃеЬ®иѓ•жКАжЬѓзЪДеИЫжЦ∞дЄОеЇФзФ®дЄ≠иµЈеИ∞дЇЖеЕ≥йФЃжАІдљЬзФ®гАВ

2гАБиЙЊж≤РиТљзФ≥жК•зЪДвАЬеЕНзЦЂзїДTCR/IgйЂШйАЪйЗПжµЛеЇПжКАжЬѓ/и°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛ/Seq-MRD¬ЃвАЭеЫ†еЕґеИЫжЦ∞жАІгАБеЙНж≤њжАІгАБеЄВеЬЇеЃЮзФ®жАІиН£иОЈвАЬ2022еєіеЇ¶CCTBдЄ≠еЫљиВњзШ§ж†ЗењЧзЙ©дЇІдЄЪеИЫжЦ∞е§ІдЉЪеИЫжЦ∞жКАжЬѓ/дЇІеУБиѓДйАЙвАЭй°єзЫЃдЇМз≠Йе•ЦгАВ

2023еєіиОЈжЙєдЇЖгАРеЕ®и°А/й™®йЂУеЯЇеЫ†зїДDNAжПРеПЦиѓХеЙВзЫТгАСпЉИз¶їењГеРЄйЩДжЯ±ж≥ХпЉЙе§Зж°ИзЉЦеПЈпЉЪжµЩжЭ≠жҐ∞е§З20230798 пЉМиѓХеЙВзЫТеИЖеИЂйАВзФ®дЇОдЇЇе§ЦеС®и°АгАБй™®йЂУж†ЈжЬђзЪДж†ЄйЕЄзЪДжПРеПЦгАВ
еПСи°®зЫЄеЕ≥жЦЗзМЃ
Seq-MRD¬ЃеПСи°®зЫЄеЕ≥жЦЗзМЃ
1гАБHuang Y, Zhao H, Shao M, Zhou L, Li X, Wei G, Wu W, Cui J, Chang AH, Sun T, Hu Y, Huang H.¬†Predictive value of next-generation sequencing-based minimal residual disease after CAR-T cell therapy. Bone Marrow Transplant.¬†2022 Jun 1. doi: 10.1038/s41409-022-01699-2. Epub ahead of print. PMID: 35650329.пЉИзВєеЗїйУЊжО•еПѓжЯ•зЬЛжЦЗзЂ†еЖЕеЃєпЉЙ

2гАБChen H, Gu M, Liang J, Song H, Zhang J, Xu W, Zhao F, Shen D, Shen H, Liao C, Tang Y, Xu X.¬†Minimal residual disease detection by next-generation sequencing of different immunoglobulin gene rearrangements in pediatric B-ALL.¬†Nat Commun. 2023 Nov 17;14(1):7468. doi: 10.1038/s41467-023-43171-9. пЉИзВєеЗїйУЊжО•еПѓжЯ•зЬЛжЦЗзЂ†еЖЕеЃєпЉЙ

3гАБMin’er Gu,Yahong Xia, Jingying Zhang, Yongmin Tang, Weiqun Xu, Hua Song ¬†Xiaojun Xu.¬†The effectiveness of blinatumomab in clearing measurable residual disease in pediatric B-cell acute lymphoblastic leukemia patients detected by next-generation sequencing.¬† Cancer Med. 2023 Dec;12(24):21978-21984. doi:10.1002/cam4.6771. пЉИзВєеЗїйУЊжО•еПѓжЯ•зЬЛжЦЗзЂ†еЖЕеЃєпЉЙ

4гАБYan N, Wang ZL, Wang XJ, etпЉМal.¬†Measurable residual disease testing by next generation sequencing is more accurate compared with multiparameter flow cytometry in adults with B-cell acute lymphoblastic leukemia.¬†Cancer Lett. 2024 Jul 4;598:217104. doi: 10.1016/j.canlet.2024.217104.

иОЈеЊЧеЫљйЩЕеЄВеЬЇиЃ§еПѓ
2023еєіDelveInsightеЕђеПЄеПСеЄГзЪДMRDеЫљйЩЕеЄВеЬЇз†Фз©ґжК•еСКдЄ≠пЉМиЙЊж≤РиТљ/Seq-MRD¬ЃжШѓдЄ≠еЫљеФѓдЄАдЄАеЃґеЕђеПЄ/дЇІеУБињЫеЕ•еЫљйЩЕи∞Гз†ФеЄВеЬЇжК•еСКгАВDelveInsightжШѓдЄАеЃґйҐЖеЕИзЪДеМїзЦЧдњЭеБ•еЄВеЬЇз†Фз©ґеТМеХЖдЄЪеҮ胥еЕђеПЄпЉМдї•еЕґзО∞жИРзЪДиБФеРИеЄВеЬЇз†Фз©ґжК•еСКдї•еПКдЄЇеМїзЦЧдњЭеБ•и°МдЄЪзЪДеЕђеПЄжПРдЊЫзЪДеЃЪеИґиІ£еЖ≥жЦєж°ИиАМйЧїеРНгАВ

1.Short NJ, et al. Clinical use of measurable residual disease in adult ALL: recommendations from a panel of US experts. Blood Adv. 2025 Mar 25;9(6):1442-1451. 
2.Paiva, B., Shi, Q., Puig, N. et al. Opportunities and challenges for MRD assessment in the clinical management of multiple myeloma. Nat Rev Clin Oncol (2025).
3.Chen H, et al. Minimal residual disease detection by next-generation sequencing of different immunoglobulin gene rearrangements in pediatric B-ALL. Nat Commun. 2023 Nov 17;14(1):7468.
4.Muffly L, et al. How I Use Next Generation Sequencing-MRD to Plan Approach and Prevent Relapse after HCT for Children and Adults with ALL. Blood. 2024 May 10:blood.2023023699.
жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄжИРзЂЛдЇО2016еєіпЉМжШѓеЫљйЩЕеЙНж≤њзЪДдЄУж≥®дЇОеЕНзЦЂй©±еК®еМїе≠¶жКАжЬѓзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪгАВеИЫеІЛдЇЇеЫҐйШЯжЭ•иЗ™зЊОеЫљиКЭеК†еУ•е§Іе≠¶пЉМеЬ®2010еєіеЉАеІЛдљњзФ®еЕНзЦЂзїДеЯЇеЫ†йЂШйАЪйЗПжµЛеЇПжКАжЬѓеЉАе±ХеРДзІНзЦЊзЧЕзЫЄеЕ≥з†Фз©ґпЉМдЇО2016еєійАЪињЗиЗ™дЄїз†ФеПСпЉМеЕ®еЫљй¶ЦеЃґжО®еЗЇNGS-MRDи°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛSeq-MRD¬ЃпЉМеєґжОИжЭГж≥ЫзФЯе≠РдљњзФ®гАВеРМжЧґпЉМеЕђеПЄжЛ•жЬЙImmun-Traq¬ЃиВњзШ§ж≤їзЦЧдЉійЪПиѓКжЦ≠гАБImmun-Cheq¬Ѓ¬†еЕНзЦЂеКЫжµЛиѓДдї•еПКImmuHub¬ЃеЕНзЦЂзїДжµЛеЇПзІСз†ФжЬНеК°дЇІеУБпЉМеєґеЄГе±АжЬЙеЯЇдЇОAIжЬЇеЩ®е≠¶дє†зЃЧж≥ХзЪДT-classifier¬ЃиВњзШ§жЧ©з≠ЫгАБеНХзїЖиГЮжµЛеЇПгАБTCR-TеТМжКЧдљУеПСзО∞з≠Йеє≥еП∞зЃ°зЇњгАВзЫЃеЙНдЄЇж≠ҐеПСи°®дЇЖжХ∞еНБзѓЗиЃЇжЦЗпЉМеЕґдЄ≠еМЕжЛђпЉЪThe New England Journal of Medicine(IF:158.5), Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24),¬†Nature Communications¬†(IF:17)з≠Йе§ЪзѓЗйЂШеИЖжЭВењЧгАВеЕђеПЄжЮДеїЇеЗ†еНБй°єеПСжШОдЄУеИ©еТМиљѓдїґиСЧдљЬжЭГдЄЇж†ЄењГзЪДиЗ™дЄїзЯ•иѓЖдЇІжЭГдљУз≥їпЉМдЄЇеМїйЩҐдЄіеЇКгАБзФЯеСљзІСе≠¶з†Фз©ґгАБжЦ∞иНѓеЉАеПСз≠ЙжПРдЊЫиІ£еЖ≥жЦєж°ИеТМдЇІеУБгАВиЙЊж≤РиТљдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХгАВ


