单克隆抗体是现代生物医药、疾病诊断与环境监测的重要工具,其背后的杂交瘤技术自1975年诞生以来,一直是抗体研发的核心手段。然而,长期以来,杂交瘤细胞在培养过程中常出现免疫球蛋白(Ig)链的丢失,导致抗体产量下降、质量不稳定,成为产业界的一大痛点。
最近,一项发表于《Advanced Science》(IF=14.1)的研究,通过艾沐蒽 ImmuHub®BCR测序技术,揭示了Ig链丢失背后的分子机制,通过蛋白组学及CRISPR等技术,构建了一套全新的UPR荧光报告系统,为杂交瘤稳定性和抗体生产监控提供了革命性的工具。

· 研究对象:使用小鼠杂交瘤细胞系BIQ-FS1(分泌抗氯硝胺单克隆抗体)
· 样本设置:通过极限稀释筛选出3个亚克隆:
① 功能正常克隆:BIQ-E2
② 功能部分失调克隆:BIQ-D4、1C10、E7
③ 完全失能克隆:BIQ-B7
阴性对照选择骨髓瘤细胞SP2/0
· 测序策略:通过艾沐蒽ImmuHub®平台构建VH与VL文库,采用Illumina HiSeq PE150双端测序
· 功能正常细胞中,目标VH(重链可变区)与VL(轻链可变区)克隆数分别高达11,619和16,350,表达稳定;
· 功能失调细胞中,尽管VL仍可检测(克隆数5,427–15,142),但VH表达显著降低甚至消失;
· 完全失能细胞几乎无功能性Ig转录本。
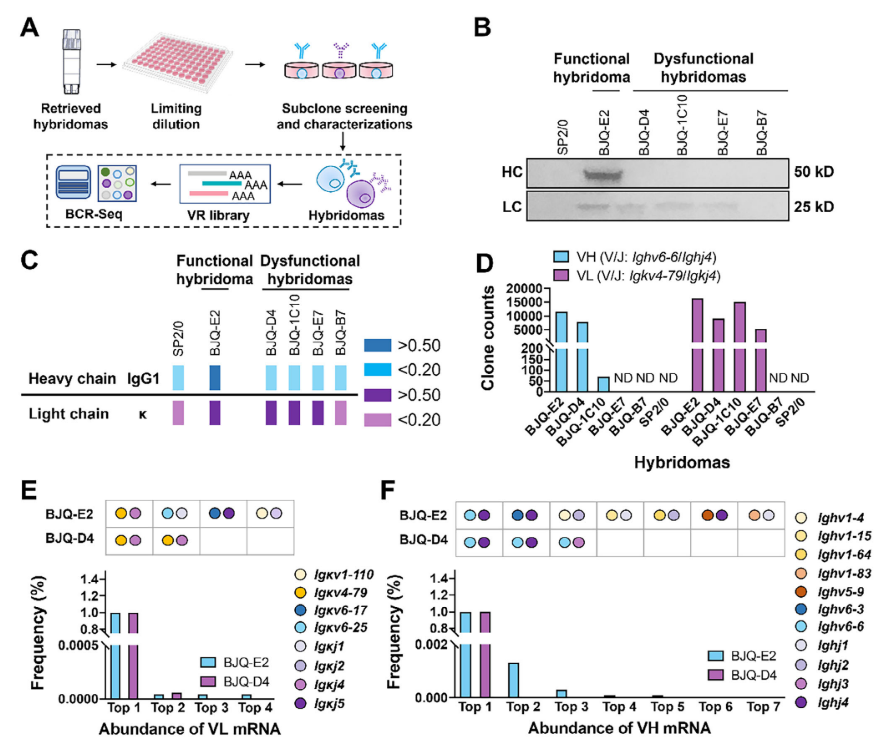
fig. 1 BCR-Seq与蛋白水平分析共同揭示,Ig链的丢失始于转录层面,并直接导致抗体功能丧失。
通过对BIQ-E2(功能正常)与BIQ-D4(功能失调)的定量蛋白质组比较:
· 发现内质网(ER)与高尔基体相关蛋白在失调细胞中显著下调
· 基因集富集分析(GSEA)显示未折叠蛋白响应(UPR)通路显著抑制
· 敲除UPR关键转录因子Xbp1s后,杂交瘤Ig表达量下降超过60%
· 通过基因回补恢复Xbp1s表达后,抗体生产功能显著恢复
· 证实UPR通路是维持杂交瘤Ig合成的核心调控枢纽
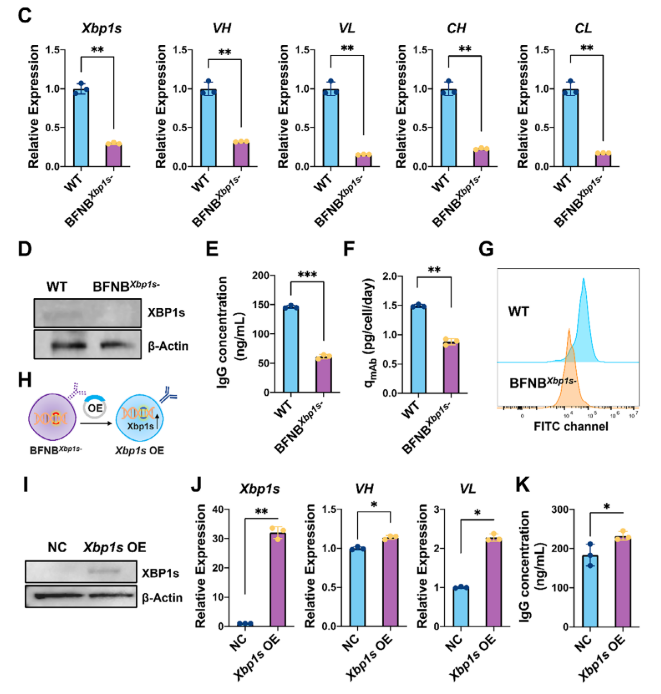
fig. 2 通过CRISPR/Cas9进行基因敲除与回补,直接验证了转录因子Xbp1s正向调控抗体生产
利用CRISPR/HRD同源重组技术,将mGFP荧光蛋白精准插入内质网伴侣蛋白 BiP(Hspa5) 基因的C端,构建BFNB-BiP-mGFP报告细胞系。
· mGFP荧光强度与内质网应激强度正相关
· 荧光信号与IgG表达水平呈强负相关(R²=0.86)
· 通过流式分选高荧光细胞群体,可高效识别即将失能的杂交瘤亚克隆
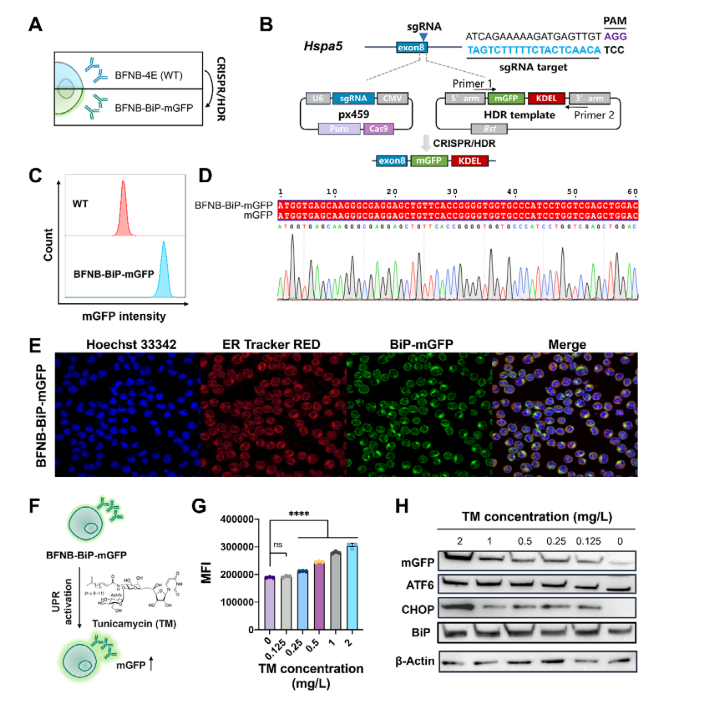
该研究通过BCR-Seq技术为核心驱动,成功串联蛋白质组学、CRISPR基因编辑与合成生物学多个技术平台,不仅揭示了杂交瘤Ig丢失的分子机制,更开发出一套可用于工业化抗体生产的实时监控系统,该系统首次实现非侵入式、实时监测杂交瘤生产状态,并能提前预警抗体生产衰竭,为高产稳定细胞株筛选提供可视化工具,为下一代智能化、高稳定性抗体生产平台的开发奠定了关键基础。
艾沐蒽专注于免疫驱动医学领域多年,开发的ImmuHub®技术平台方法全面,检测物种多样,建库方法具有灵活性,致力于为各大高校、医院、科研机构、企业等提供优良的科研服务。

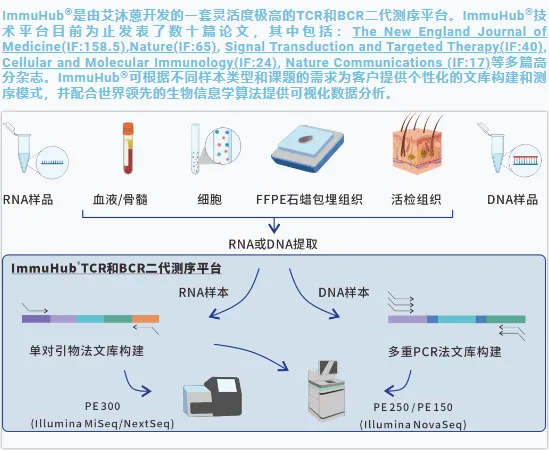
ImmuHub®部分科研方向

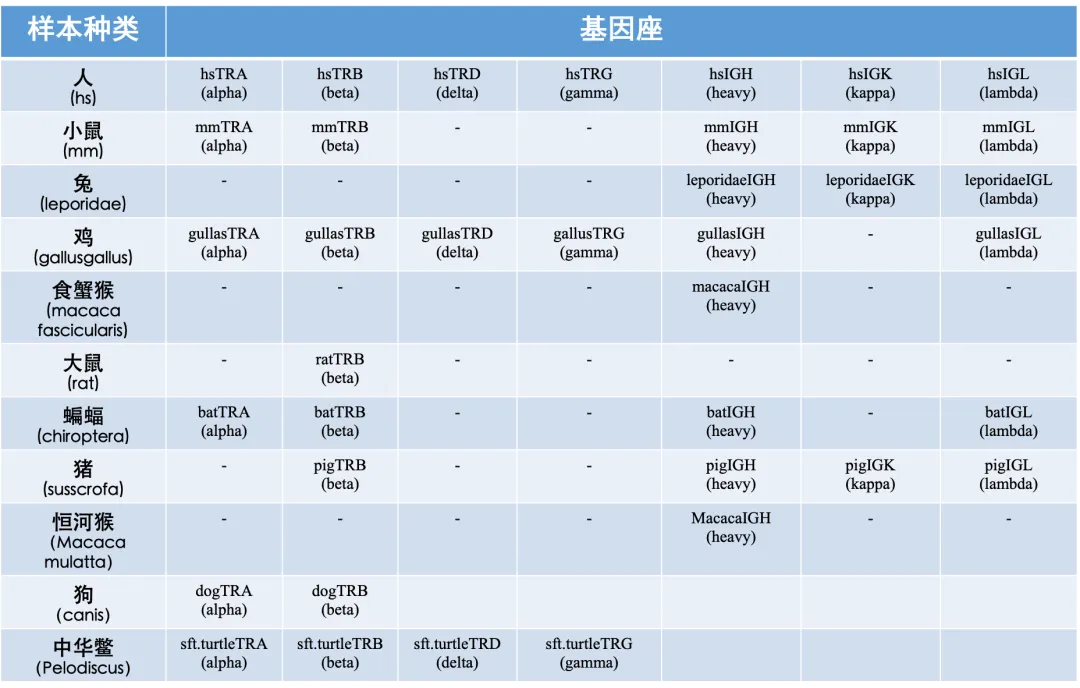
ImmuHub®适用基因座
部分数据分析结果展示
杭州艾沐蒽生物科技有限公司成立于2016年,是国际前沿的专注于免疫驱动医学技术的国家高新技术企业和专精特新企业。创始人团队来自美国芝加哥大学,在2010年开始使用免疫组基因高通量测序技术开展各种疾病相关研究,于2016年通过自主研发,全国首家推出NGS-MRD血液肿瘤微小残留病(MRD)检测Seq-MRD®,并授权泛生子使用。同时,公司拥有Immun-Traq®肿瘤治疗伴随诊断、Immun-Cheq® 免疫力测评以及ImmuHub®免疫组测序科研服务产品,并布局有基于AI机器学习算法的T-classifier®肿瘤早筛、单细胞测序、新抗原、TCR和抗体发现等平台管线。目前为止发表了50余篇论文,其中包括:The New England Journal of Medicine(IF:158.5), The Lancet(IF:98.4), Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24), Nature Communications (IF:17)等多篇高分杂志。公司构建几十项发明专利和软件著作权为核心的自主知识产权体系,为医院临床、生命科学研究、新药开发等提供解决方案和产品。艾沐蒽专注于通过解码适应性免疫系统来改变疾病的诊断和治疗,并致力于推进免疫驱动医学领域发展。


