
дЇЇдє≥е§ізШ§зЧЕжѓТпЉИhuman papillomavirusesпЉМHPVпЉЙпЉМжШѓдЄАзІНжЧ†еМЕиЖЬе∞ПDNAзЧЕжѓТпЉМHPVжДЯжЯУжШѓжЬАеЄЄиІБзЪДзФЯжЃЦйБУзЧЕжѓТжДЯжЯУгАВзЇ¶40дЄ™HPVдЇЪеЮЛжДЯжЯУиВЫйЧ®зФЯжЃЦйБУпЉИеЃЂйҐИгАБйШійБУгАБиВЫйЧ®пЉЙеТМеП£иЕФйїПиЖЬдЄКзЪЃгАВдљОеН±еЮЛHPVпЉИе¶В6гАБ11еЮЛз≠ЙпЉЙеЉХиµЈ90%зФЯжЃЦеЩ®зЦ£еТМеТљеЦЙйГ®дє≥е§ізШ§гАВжМБзї≠жДЯжЯУйЂШеН±еЮЛHPVпЉИе¶В16гАБ18еЮЛз≠ЙпЉЙеПѓеѓЉиЗі96%еЃЂйҐИзЩМгАБ93%иВЫйЧ®зЩМгАБ64%йШійБУзЩМгАБ51%е§ЦйШізЩМгАБ36%йШіиМОзЩМеТМ63%еП£еТљзЩМгАВзО∞жЬЙзЪДйҐДйШ≤жАІзЦЂиЛЧеѓєйҐДйШ≤HPVжДЯжЯУжШѓжЬЙжХИзЪДпЉМдљЖеЃГдїђдЄНиГљжґИйЩ§еЈ≤еїЇзЂЛзЪДжДЯжЯУпЉЫж≤їзЦЧжАІзЦЂиЛЧеПѓдї•жї°иґ≥ињЩдЄАйЬАж±ВгАВзДґиАМHPVж≤їзЦЧжАІзЦЂиЛЧз†Фз©ґжХ∞еНБеєіпЉМж≥®еЖМзЪДдЄіеЇКиѓХй™М130е§ЪдЄ™пЉМеНіиЗ≥дїКжЬ™жЬЙжЙєеЗЖдЄКеЄВгАВдЄАй°єеѓєдЇОдЄАеРНжО•еПЧдЇЖPepCan HPVж≤їзЦЧжАІзЦЂиЛЧIжЬЯдЄіеЇКз†Фз©ґзЪДе•≥жАІжВ£иАЕзЪДз†Фз©ґжП≠з§ЇдЇЖHPVж≤їзЦЧжАІзЦЂиЛЧжО•зІНеРОдЇІзФЯзЪДTзїЖиГЮзЙєеЉВжАІгАВ
зїУжЮЬпЉЪ
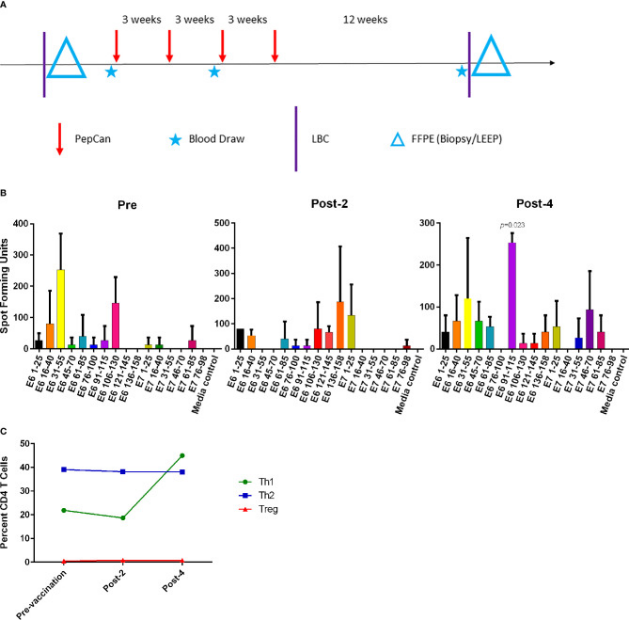
Fig.1 IжЬЯдЄіеЇКиѓХй™МиЃЊиЃ°еТМеЄЄиІДеЕНзЦЂзЫСжµЛеИЖжЮРгАВпЉИAпЉЙIжЬЯз†Фз©ґзЪДдЄіеЇКеЃЮй™МиЃЊиЃ°гАВеѓєзїПжіїж£АиѓБеЃЮжЬЙеЃЂйҐИйЂШеЇ¶й≥ЮзКґдЄКзЪЃзЧЕеПШпЉИHSILsпЉМеН≥CIN2зЇІжИЦ3зЇІпЉЙзЪДжВ£иАЕжѓПйЪФ3еС®ињЫи°МзЦЂиЛЧжО•зІНпЉИPepCanпЉЙгАВеЬ®жО•зІНзЦЂиЛЧеЙНгАБ2жђ°жО•зІНеРОеТМ4жђ°жО•зІНеРОињЫи°МжКљи°АгАВеЬ®жО•зІНеЙНеТМ4жђ°жО•зІНеРОйЗЗйЫЖеЃЂйҐИе±АйГ®ж†ЈжЬђ(LBCеТМFFPE)гАВFFPEж†ЈжЬђжЭ•иЗ™жО•зІНеЙНеЃЂйҐИжіїж£АеТМ4жђ°жО•зІНеРОзОѓзФµеИЗйЩ§жЬѓ(LEEP)жіїж£АгАВпЉИBпЉЙдљњзФ®IFN-g ELISPOTжµЛеЃЪжѓПдЄ™зЦЂиЛЧйШґжЃµзЪДеЕНзЦЂеОЯжАІHPV16 E6еТМE7еМЇеЯЯгАВеЬ®зЦЂиЛЧжО•зІНеЙНйШґжЃµпЉМеЬ®E6 16-40гАБE6 31-55еТМE6 106-130еМЇеЯЯж£АжµЛеИ∞йШ≥жАІеПНеЇФпЉИеН≥иЗ≥е∞СжШѓеЯєеЕїеЯЇеѓєзЕІзЪДдЄ§еАНпЉЙгАВеЬ®2жђ°зЦЂиЛЧжО•зІНеРОж†ЈжЬђдЄ≠зЪДE6 1-25гАБE6 106-130гАБE6 136-158еТМE7 1-25еМЇеЯЯдї•еПК4жђ°зЦЂиЛЧжО•зІНеРОж†ЈжЬђдЄ≠зЪДE6 31-55гАБE6 91-115еТМE7 46-70дЄ≠ж£АжµЛеИ∞йШ≥жАІеПНеЇФгАВ4жђ°зЦЂиЛЧжО•зІНеРОпЉМHPV16 E6 91-115еМЇеЯЯзЪДеПНеЇФеҐЮеК†еЕЈжЬЙзїЯиЃ°е≠¶жДПдєЙпЉИйЕНеѓєtж£Ай™МпЉМp=0.023пЉЙгАВ(C)PBMCиНІеЕЙзїЖиГЮеИЖжЮРжШЊз§ЇпЉМ4жђ°зЦЂиЛЧжО•зІНеРОTh1(CD4+Tbet+)ж∞іеє≥еҐЮеК†пЉМиЃ§дЄЇиѓ•зЦЂиЛЧйАЪињЗеИЇжњАзїЖиГЮдїЛеѓЉзЪДеЕНзЦЂеКЫпЉИдЄїи¶БжШѓTзїЖиГЮпЉЙжЭ•еПСжМ•дљЬзФ®гАВ

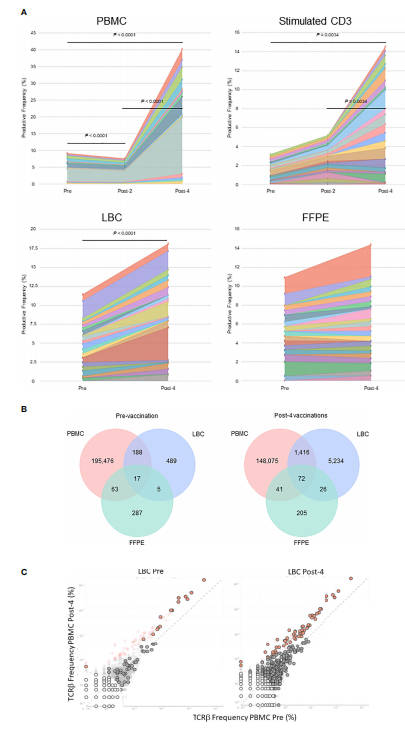
Fig.3 ињљиЄ™е§ЦеС®и°АеТМе≠РеЃЂйҐИдЄ≠зЪДеЕЛйЪЖеЮЛгАВ(A)ињљиЄ™зФ±ж†ЄиЛЈйЕЄеЇПеИЧеЃЪдєЙзЪДеЬ®productive clonalityдЄ≠Top15еЕЛйЪЖеЮЛгАВеЬ®дљњзФ®TзїЖиГЮжХ∞йЗПиЃ°зЃЧзЪДPBMCж†ЈжЬђдЄ≠пЉМTop15еЕЛйЪЖеЮЛеЬ®2жђ°жО•зІНеРОжШЊиСЧйЩНдљОпЉИWilcoxonйЕНеѓєзђ¶еПЈзІ©ж£Ай™МпЉМp=0.0012пЉЙпЉМдљЖеЬ®4жђ°жО•зІНеРОжШЊиСЧеҐЮеК†пЉИp<0.0001пЉЙгАВеѓєдЇОеПЧеИЇжњАзЪДCD3+ TзїЖиГЮж†ЈжЬђпЉМеЬ®жО•зІНзЦЂиЛЧеЙНеТМ4жђ°жО•зІНеРО(p=0.0034)дєЛйЧідї•еПК2жђ°жО•зІНеРОеТМ4жђ°жО•зІНеРО(p=0.0034)дєЛйЧіиІВеѓЯеИ∞жШЊиСЧеҐЮеК†гАВеЬ®LBCж†ЈжЬђдЄ≠иІВеѓЯеИ∞жШЊиСЧеҐЮеК†(p<0.0001)пЉМдљЖеЬ®FFPEж†ЈжЬђдЄ≠ж≤°жЬЙгАВ(B)зФ±зЦЂиЛЧжО•зІНеЙНеТМ4жђ°жО•зІНеРОPBMCгАБLBCеТМFFPEж†ЈжЬђзЪДж†ЄиЛЈйЕЄеЃЪдєЙзЪДеЕЛйЪЖеЮЛзЪДзїіжБ©еЫЊгАВе§Іе§ЪжХ∞еЕЛйЪЖеЮЛдїЕеЗЇзО∞еЬ®дЄАзІНж†ЈжЬђз±їеЮЛдЄ≠пЉМдљЖеЬ®зЦЂиЛЧжО•зІНеЙНPBMCгАБLBCеТМFFPEдЄ≠е≠ШеЬ®17зІНеЕЛйЪЖжАІпЉМиАМеЬ®4жђ°жО•зІНеРОе≠ШеЬ®72зІНеЕЛйЪЖеЮЛгАВ(C)4жђ°зЦЂиЛЧжО•зІНеЙНеРОLBCж†ЈжЬђдЄ≠еБЗиЃЊзЪДзЦЂиЛЧзЙєеЉВжАІеЕЛйЪЖеЮЛгАВйАЪињЗдљњзФ®ќ≤-дЇМй°єеЉПж®°еЮЛпЉИжШЊз§ЇдЄЇеЄ¶жЬЙеТМдЄНеЄ¶жЬЙйїСиЙ≤еЬЖ嚥茺ж°ЖзЪДзЇҐзВєпЉЙжѓФиЊГзЦЂиЛЧжО•зІНеЙНеТМ4жђ°жО•зІНеРОPBMCж†ЈжЬђпЉМйЙіеЃЪдЇЖ70зІНеБЗиЃЊзЪДзЦЂиЛЧзЙєеЉВжАІеЕЛйЪЖеЮЛгАВеЄ¶жЬЙйїСиЙ≤еЬЖ嚥茺ж°ЖзЪДзЇҐзВєдї£и°®ињЩдЇЫеБЗиЃЊзЪДзЦЂиЛЧзЙєеЉВжАІTCRsе≠ШеЬ®дЇОжО•зІНеЙНLBCж†ЈжЬђ(n=15)еТМ4жђ°зЦЂиЛЧжО•зІНеРОLBCж†ЈжЬђ(n=57)дЄ≠гАВжО•зІНеЙНеТМ4жђ°жО•зІНеРОPBMCж†ЈжЬђдєЛйЧізЪДжЈ±зБ∞иЙ≤зВєж≤°жЬЙжШЊиСЧеЈЃеЉВгАВеЄ¶жЬЙйїСиЙ≤еЬЖ嚥茺ж°ЖзЪДжЈ±зБ∞иЙ≤зВєж≤°жЬЙжШЊиСЧеҐЮеК†пЉМдљЖе≠ШеЬ®дЇОзЫЄеЇФзЪДLBC ж†ЈжЬђдЄ≠гАВж≤°жЬЙйїСиЙ≤еЬЖ嚥茺ж°ЖзЪДжµЕзБ∞иЙ≤зВєдЄНе≠ШеЬ®дЇОзЫЄеЇФзЪДLBCж†ЈжЬђдЄ≠гАВ
жАїзїУпЉЪ
HPVйҐДйШ≤жАІзЦЂиЛЧйАЪињЗдЄ≠еТМжКЧдљУиµЈдљЬзФ®пЉМиАМж≤їзЦЧжАІзЦЂиЛЧеИЩжШѓйАЪињЗдїЛеѓЉзїЖиГЮеЕНзЦЂеПНеЇФеПСжМ•дљЬзФ®пЉМеЫ†ж≠§пЉМTзїЖиГЮеЕНзЦЂеЇФз≠ФзЪДиѓДдЉ∞еЇФеМЕжЛђеЬ®дЄіеЇКиѓХй™МзЪДзїИзВєдЄ≠гАВдљЖеЬ®еЃЮйЩЕеЇФзФ®дЄ≠гАВеЕґдїЦз†Фз©ґдљњзФ®еРИеєґзЪДиВљињЫи°МIFN-ќ≥ ELISPOTжµЛеЃЪпЉМзФ±дЇОиІ£еЖїеРОзЪДдЇІйЗПеТМжіїеКЫдљОпЉМе§Іе§ЪжХ∞ж†ЈеУБйГљдЄНйАВеРИпЉМдї•еПКз°ЃеЃЪиЫЛзЩљиі®йВ£дЄАйГ®еИЖеРЂжЬЙжКЧеОЯи°®дљНдњ°жБѓз≠Йз≠ЙгАВиАМж≠§й°єз†Фз©ґзїУеРИдЉ†зїЯзЪДELISPOTеТМTCRжµЛеЇПжКАжЬѓпЉМеПѓдї•йФБеЃЪеЬ®дЄАдЄ™еМЇеЯЯпЉМињЩжШѓеЕ≥йФЃгАВеЬ®ињЩй°єз†Фз©ґдЄ≠пЉМBulk TCRжµЛеЇПеРОдљњзФ®ќ≤-дЇМй°єеЉПж®°еЮЛйЙіеЃЪеЗЇ70зІНеБЗиЃЊзЪДзЦЂиЛЧзЙєеЉВжАІеЕЛйЪЖеЮЛпЉМеЕґдЄ≠жЬЙ60зІНжШѓеИЇжњАеРОеЬ®еНХзїЖиГЮеИЖжЮРдЄ≠з°ЃеЃЪзЪДгАВ
дїАдєИжШѓImmuHub¬ЃжКАжЬѓпЉЯ
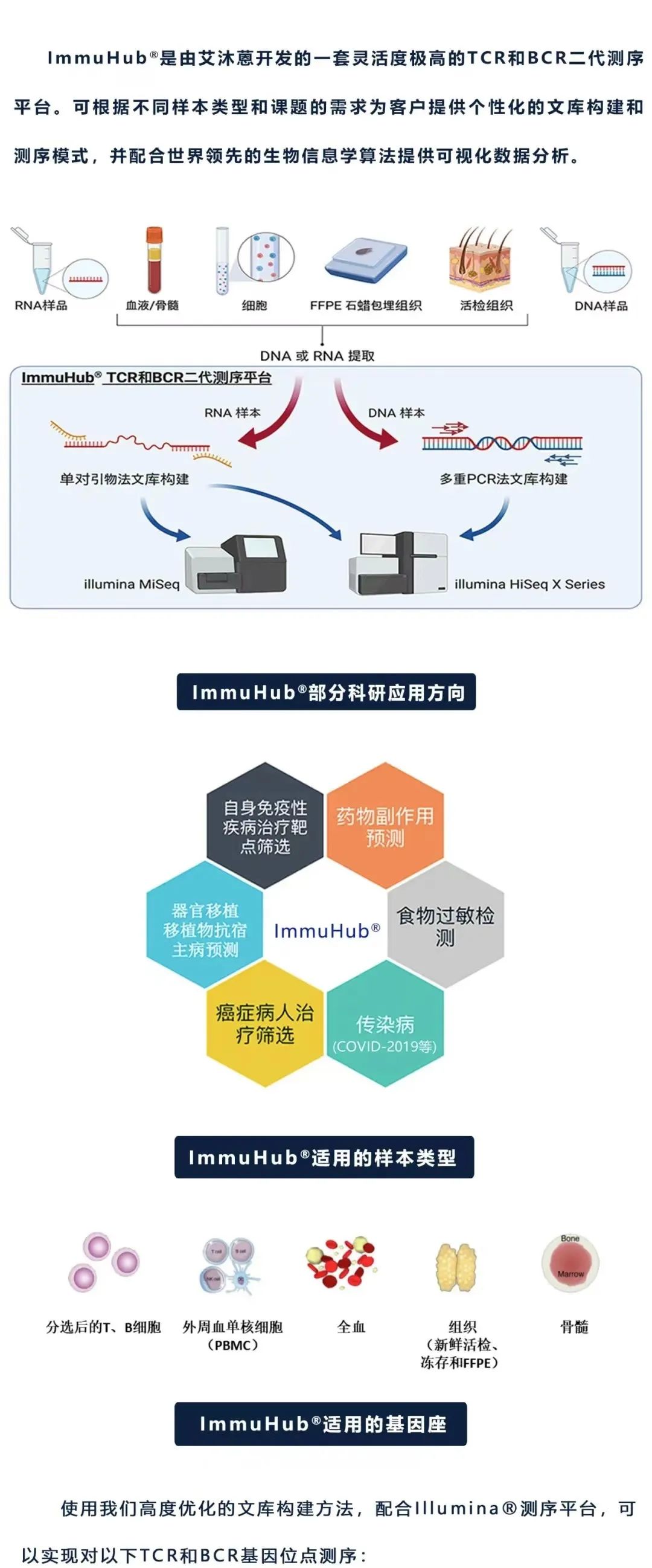
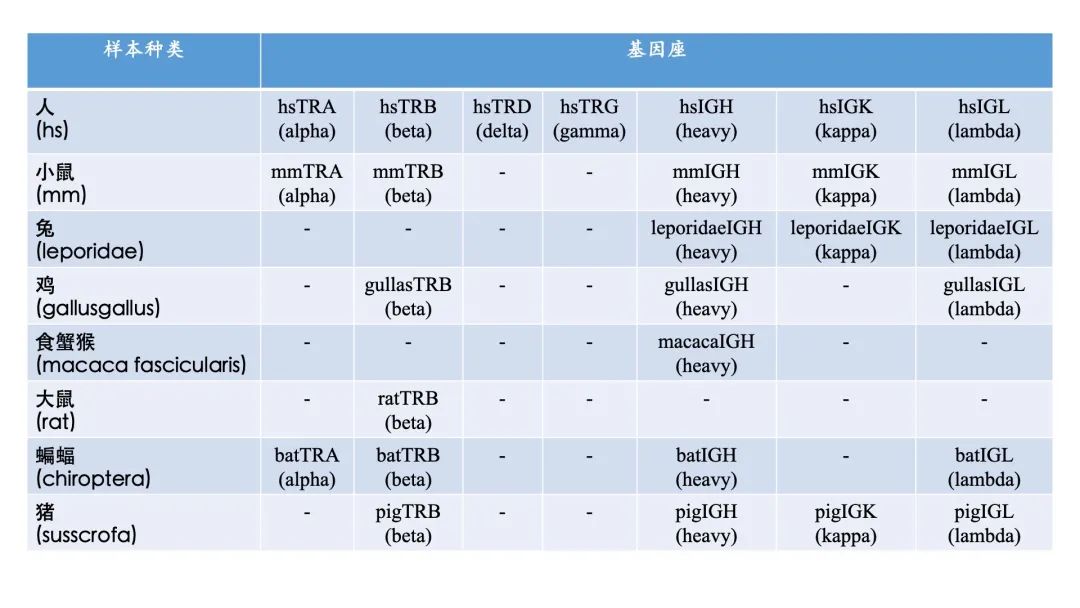
зВєеЗїйШЕиѓїеОЯжЦЗпЉМдЇЖиІ£жЫіе§ЪжЬЙеЕ≥ImmuHub¬Ѓ
еПВиАГжЦЗзМЃпЉЪ
[1]Shibata T, Shah S, Evans T, Coleman H, Lieblong BJ, Spencer HJ, Quick CM, Sasagawa T, Stephens OW, Peterson E, Johann D Jr, Lu YC, Nakagawa M. Expansion of Human Papillomavirus-Specific T Cells in Periphery and Cervix in a Therapeutic Vaccine Recipient Whose Cervical High-Grade Squamous Intraepithelial Lesion Regressed. Front Immunol. 2021 Sep 30;12:645299. doi: 10.3389/fimmu.2021.645299. PMID: 34659195; PMCID: PMC8515132.
жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄзФ±зЊОеЫљиКЭеК†еУ•е§Іе≠¶зІСз†ФеЫҐйШЯеЫЮеЫљеИЫеКЮпЉМжШѓдЄАеЃґдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪгАВиЙЊж≤РиТљзЂЩеЬ®йАВеЇФжАІеЕНзЦЂз≥їзїЯз†Фз©ґзЪДжЬАеЙНж≤њпЉМиЗ™дЄїз†ФеПСзЪДеЕНзЦЂеМїе≠¶еє≥еП∞еПѓжП≠з§ЇеТМзњїиѓСйАВеЇФжАІеЕНзЦЂз≥їзїЯзЪДйБЧдЉ†еѓЖз†БпЉМеєґиГљеЇФзФ®дЇОзЩМзЧЗгАБиЗ™иЇЂеЕНзЦЂжАІзЦЊзЧЕгАБдЉ†жЯУжАІзЦЊзЧЕз≠ЙеЕНзЦЂдїЛеѓЉжАІзЦЊзЧЕзЪДиѓКжЦ≠гАБзЫСжµЛеТМж≤їзЦЧдЄ≠гАВ

