2024年4月12日,第三军医大学叶丽林教授团队联合中国农业大学张国中教授团队、北京大学白凡教授团队、南京医科大学李颜教授团队在顶刊Nature Cancer(影响因子:22.7)杂志发表了题为“An oncolytic virus delivering tumor-irrelevant bystander T cell epitopes induces anti-tumor immunity and potentiates cancer immunotherapy”的文章,该研究主要探讨了利用肿瘤无关旁观者T细胞(tumor-irrelevant bystander T cells,TBYS)来增强癌症免疫疗法的效果,作者设计了一种治疗策略——溶瘤病毒编码旁观者T细胞表位(OV-BYTE),并在多种模型中取得了显著的治疗效果。文中使用我们艾沐蒽的ImmuHub®TCR分析系统,证实了靶向病毒特异性表位的OV-BYTE疗法导致肿瘤特异性抗原的表位扩散,触发T细胞免疫应答,发挥抗肿瘤作用。

虽然肿瘤特异性T细胞在抗肿瘤免疫中起着关键作用,但在肿瘤微环境(TME)中它们的数量稀少且功能耗竭,导致大多数癌症患者的免疫治疗效果不佳。已有研究发现肿瘤微环境中存在大量不识别肿瘤抗原、而特异性识别机体既往感染的各类病毒的旁观者T细胞(TBYS),具有与记忆T细胞(TMEM)相似的转录本特征,可能是潜在的癌症免疫治疗靶标。 因此,研究人员设计了一种基于TBYS的新型免疫治疗方法——OV-BYTE,通过工程化病毒编码TBYS表位来诱导肿瘤细胞表达这些表位,从而激活TBYS发挥抗肿瘤作用。然后在多种模型中验证了该治疗方法的有效性,并通过单细胞转录组测序、单细胞及bulk TCR测序以及经典细胞免疫学实验阐明治疗策略的细胞学作用机制。此外,作者还探究了OV-BYTE策略与PD-1/PD-L1免疫治疗的协同作用。 研究人员将特异性识别淋巴细胞性脉络丛脑膜炎病毒(LCMV)糖蛋白的P14 CD8+T细胞转移到小鼠体内,然后用同基因MC38结肠腺癌细胞和肿瘤浸润性P14 CD8+和SM CD4+T细胞移植小鼠体内,在不同时间点收集到的肿瘤组织中,可以检测到稳定的病毒特异性P14和SM TBYS细胞。与TMEM细胞相比,TBYS细胞具有类似的转录因子表达模式。此外,研究者还通过单细胞RNA测序技术对P14 TBYS细胞进行了深入分析,发现它们在基因表达模式上与TMEM细胞相似,但在一些关键基因上有所不同。总之,这些发现突出了肿瘤微环境中病毒特异性CD8+和CD4+TBYS细胞的功能记忆特征。 研究人员设计了一种基于病毒的治疗策略(OV-BYTE),该策略利用了肿瘤微环境中已经存在的病毒特异性T细胞TBYS来诱导肿瘤细胞的死亡。具体来说,研究人员使用一种能够编码肿瘤抗原的重组病毒(NDV-GP)来感染肿瘤细胞,从而使得肿瘤细胞表面表达出与TBYS细胞所识别的相同抗原。这样,TBYS细胞就能够被激活并攻击肿瘤细胞,进而实现肿瘤的抑制。实验人员利用多种TBYS细胞表位、多种溶瘤病毒类别,在结肠癌、黑色素瘤、胆管癌等多种癌症小鼠模型、人源化小鼠模型中验证了该治疗策略的有效性。这些数据均证明了OV-BYTE疗法的潜在抗肿瘤功能。 接下来作者研究了OV-BYTE疗法的作用机制。研究发现,NDV-GP治疗有利于肿瘤微环境中的CD8+和CD4+T细胞应答。CD8+或CD4+T细胞的耗竭则消除了NDV-GP的治疗效果,导致肿瘤小鼠的长期存活率显著降低。另外还发现,相比于CD4+或CD8+T细胞的单转移,二者的组合转移协同作用可以更好地控制NDV-GP治疗组中的肿瘤生长,说明CD8+和CD4+TBYS细胞之间的相互作用也对OV-BYTE疗法的效果产生了重要影响。 这些结果表明OV-BYTE疗法可以靶向病毒特异性CD8+和CD4+TBYS细胞,并有效地将它们的细胞毒性重定向至肿瘤细胞。 研究发现,与CD8+TBYS细胞相比,NDV-GP处理显著增加了CD4+TBYS细胞的频率和数量。通过单细胞RNA-seq和流式细胞术发现,在CD4+TBYS细胞对携带同源表位的OV的应答中涉及明显的记忆-效应子转变。高表达颗粒酶B(GzmB)基因是参与细胞毒性功能的一个重要基因,CD4+TBYS细胞的GzmB依赖性细胞毒性在实现OV-BYTE疗法的治疗结果中是不可或缺的。 总之,OV-BYTE疗法能够诱导产生具有细胞毒性的CD4+TBYS细胞,这些细胞可以通过多种途径杀伤肿瘤细胞,包括分泌细胞因子、介导抗体依赖性细胞毒性等方式。 从肿瘤引流淋巴结(dLN)迁移的TMEM细胞可能对维持TME中的TBYS细胞十分重要,但是NDV-GP处理可以有效地原位扩增病毒特异性TBYS细胞,即使这些细胞无法从dLN获得补充。且原位扩增的病毒特异性TBYS细胞对OV-BYTE疗法的治疗效果提供主要贡献。 首先通过单细胞TCR测序发现NDV-GP组的肿瘤反应性CD8+T细胞的寡克隆扩增相对于PBS对照组或NDV-WT组明显增强(图a),表明OV-BYTE疗法诱导肿瘤反应性CD8+T细胞的潜在T细胞表位扩散。 然后通过bulk TCR测序发现NDV-GP组的肿瘤特异性CD8+T细胞比PBS或NDV-WT组具有更多样化的TCR克隆(图b),进一步证实了靶向病毒特异性表位的OV-BYTE疗法导致肿瘤特异性抗原的表位扩散,因此,增强了TTST细胞应答。肿瘤浸润病毒特异性TBYS细胞的特征
OV-BYTE疗法增强抗肿瘤应答
OV-BYTE疗法归因于CD8+和CD4+TBYS细胞
OV-BYTE疗法激发并扩大细胞毒性CD4+TBYS细胞功能
OV-BYTE促进原位TBYS细胞抑制肿瘤生长
OV-BYTE通过诱导表位扩散增强肿瘤特异性T细胞(TTST)应答
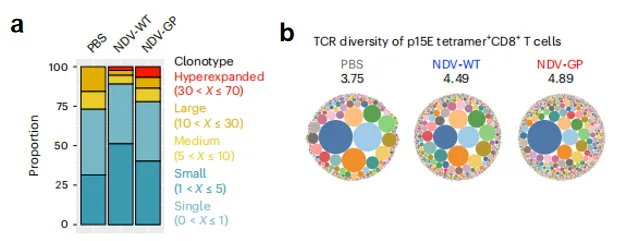
注:a.三个处理组不同频率克隆型占比比较,NDV-GP组的高频克隆占比明显高于另两组。b.三个处理组的TCR香农指数多样性比较,NDV-GP组高于另两组。 研究发现,OV-BYTE与PD-L1免疫检查点阻断(ICB)联合治疗的抗肿瘤效果优于其中一种疗法的单独使用。在所有实验环境中,通过用PD-L1 ICB和NDV-GP同时处理,肿瘤特异性CD8+T细胞应答得到最大程度的增强。表明OV-BYTE可以通过增强TTST细胞应答来加强PD-L1 ICB的抗肿瘤功效。 鉴于全球范围内广泛的SARS-CoV-2感染和COVID-19疫苗免疫,作者考虑该人群癌症患者的SARS-CoV-2特异性TBYS细胞是否可以作为OV-BYTE策略的重要潜在靶点细胞。通过在接种新冠疫苗的肿瘤小鼠模型、人源化小鼠模型等多种模型上验证,均取得了显著的抗肿瘤效果,并且与现有的免疫检查点阻断药物相结合,同样提高了治疗效果。证实了靶向新冠病毒TBYS细胞的OV-BYTE策略的抗肿瘤效力,这具有重要的临床意义,为癌症免疫治疗领域提供了新的视角和思路。 本研究揭示了TBYS细胞在肿瘤微环境中的重要角色,并提出了新的治疗策略——OV-BYTE,且通过实验验证了其有效性。作者运用溶瘤病毒策略巧妙地将肿瘤非相关的、但具备记忆细胞特征的TBYS细胞动员为抗癌增援部队,这突破了传统的癌症免疫治疗策略模式,一定程度规避了肿瘤抗原特异性T细胞的功能耗竭问题,这为肿瘤免疫治疗提供了新思路和方向。 文献来源:Chen X, Zhao J, Yue S, Li Z, Duan X, Lin Y, Yang Y, He J, Gao L, Pan Z, Yang X, Su X, Huang M, Li X, Zhao Y, Zhang X, Li Z, Hu L, Tang J, Hao Y, Tian Q, Wang Y, Xu L, Huang Q, Cao Y, Chen Y, Zhu B, Li Y, Bai F, Zhang G, Ye L. An oncolytic virus delivering tumor-irrelevant bystander T cell epitopes induces anti-tumor immunity and potentiates cancer immunotherapy. Nat Cancer. 2024 Apr 12. doi: 10.1038/s43018-024-00760-x. 近期国家自然基金委员会发布了关于发布免疫力数字解码重大研究计划2024年度项目指南的通告,重点支持免疫组库中国数据队列建立的研究,点击链接可详细了解通告解读➡2024国自然免疫力数字解码重大研究计划关键技术的核心解读。艾沐蒽可以在接下来的国家重大研究计划中,帮助各位专家学者们开展科研工作,助力免疫组研究,助力疾病早筛。 杭州艾沐蒽生物科技有限公司成立于2016年,是国际前沿的专注于免疫驱动医学技术的国家高新技术企业。创始人团队来自美国芝加哥大学,在2010年开始使用免疫组基因高通量测序技术开展各种疾病相关研究,于2016年通过自主研发,全国首家推出NGS-MRD血液肿瘤微小残留病(MRD)检测Seq-MRD®,并授权泛生子(纳斯达克代码:GTH)使用。同时,公司拥有Immun-Traq®肿瘤治疗伴随诊断、Immun-Cheq® |T细胞免疫测评以及ImmuHub®免疫组测序科研服务产品,并布局有基于AI机器学习算法的T-classifier®肿瘤早筛、单细胞测序、TCR-T和抗体发现等平台管线。目前为止发表了数十篇论文,其中包括:Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24), Nature Communications (IF:17)等多篇高分杂志。公司构建几十项发明专利和软件著作权为核心的自主知识产权体系,为医院临床、生命科学研究、新药开发等提供解决方案和产品。艾沐蒽专注于通过解码适应性免疫系统来改变疾病的诊断和治疗,并致力于推进免疫驱动医学领域发展。OV-BYTE和PD-L1协同控制肿瘤进展
OV-BYTE使SARS-CoV-2特异性TMEM细胞发挥抗肿瘤作用成为可能
